(1)含有3.01×1023个H的H2O,其H2O物质的量是________ ;其H2O中含有电子的个数为______________ 。
(2)______ mol H2O中含有的氧原子数与1.5 mol CO2中含有的氧原子数相等。
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为________ 。
(4)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为__________ 。
(5)标准状况下,密度为0.75 g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为__________ ,(注:体积分数即为物质的量分数)
(6)已知a g A和b g B恰好完全反应生成0.4mol C和d g D,则C的摩尔质量为________
(7)同温、同压下等质量的SO2气体和CO2气体,体积之比___________ ,原子数目之比为___________ ,密度比为___________ ,氧元素的质量比为__________ 。
(8)某气态氧化物化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为____________ ;R的相对原子质量为_____________ 。
(9)200mL、2.0mol/L的Al2(SO4)3溶液中含Al3+的物质的量为___________ ;从中取出10mL,将这10mL溶液用水稀释到50mL,所得溶液中溶质的物质的量浓度为______________ 。
(2)
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为
(4)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为
(5)标准状况下,密度为0.75 g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为
(6)已知a g A和b g B恰好完全反应生成0.4mol C和d g D,则C的摩尔质量为
(7)同温、同压下等质量的SO2气体和CO2气体,体积之比
(8)某气态氧化物化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
(9)200mL、2.0mol/L的Al2(SO4)3溶液中含Al3+的物质的量为
更新时间:2017/10/28 14:08:16
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】用NA表示阿伏加 德罗常数的数值。请回答下列问题:
(1)0.5mol SO2共含有约_______ 个原子,它与_______ g SO3所含硫原子数相等。
(2)质量相同的①HCl、②NH3、③CO2、④O2四种气体中,在同温同压条件下,所占体积最小的是(填序号)___________ 。
(3)19g某二价金属氯化物(ACl2)中含有0.4mol Cl-,则ACl2的摩尔质量是__________ 。
(1)0.5mol SO2共含有约
(2)质量相同的①HCl、②NH3、③CO2、④O2四种气体中,在同温同压条件下,所占体积最小的是(填序号)
(3)19g某二价金属氯化物(ACl2)中含有0.4mol Cl-,则ACl2的摩尔质量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据所学知识填写下列空白。
(1)在标准状况下,3.4g氨气与同条件下_______ mol 含有相同的质子数。
含有相同的质子数。
(2)在标准状况下,由CO和 组成的混合气体体积为6.72L,质量为12g,此混合物中CO和
组成的混合气体体积为6.72L,质量为12g,此混合物中CO和 物质的量之比是
物质的量之比是___________ 。
(3)在溶质仅含 、
、 和
和 的混合溶液中,
的混合溶液中, ,
,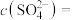
 ,
,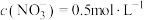 ,则此溶液中
,则此溶液中 为
为___________  。
。
(4)0.2g 、8.8g
、8.8g 组成的混合气体,其密度是同样条件下
组成的混合气体,其密度是同样条件下 的密度的
的密度的_______ 倍。
(5)某元素X的一种含氧酸化学式为 ,属于二元酸,则
,属于二元酸,则 与过量氢氧化钠溶液反应生成的产物为
与过量氢氧化钠溶液反应生成的产物为 和
和___________ (写化学式)。
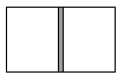
(6)某密闭容器,中间有一可自由滑动的隔板(厚度忽略不计)将容器分成两部分,装置如图所示(左、右两侧温度相同)。左侧充入1mol氦气;右侧充入CO和NO的混合气体,原子总数为1.6mol。则左右两室体积比为___________ 。
(1)在标准状况下,3.4g氨气与同条件下
 含有相同的质子数。
含有相同的质子数。(2)在标准状况下,由CO和
 组成的混合气体体积为6.72L,质量为12g,此混合物中CO和
组成的混合气体体积为6.72L,质量为12g,此混合物中CO和 物质的量之比是
物质的量之比是(3)在溶质仅含
 、
、 和
和 的混合溶液中,
的混合溶液中, ,
,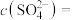
 ,
,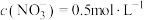 ,则此溶液中
,则此溶液中 为
为 。
。(4)0.2g
 、8.8g
、8.8g 组成的混合气体,其密度是同样条件下
组成的混合气体,其密度是同样条件下 的密度的
的密度的(5)某元素X的一种含氧酸化学式为
 ,属于二元酸,则
,属于二元酸,则 与过量氢氧化钠溶液反应生成的产物为
与过量氢氧化钠溶液反应生成的产物为 和
和(6)某密闭容器,中间有一可自由滑动的隔板(厚度忽略不计)将容器分成两部分,装置如图所示(左、右两侧温度相同)。左侧充入1mol氦气;右侧充入CO和NO的混合气体,原子总数为1.6mol。则左右两室体积比为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】利用相关知识填空。
(1)标准状况下 中含
中含___________ 个氨分子,___________ 个氢原子。
(2)标准状况下,等质量的 和
和 物质的量之比是
物质的量之比是___________ ,分子数之比为___________ ,所含的氧原子个·数之比是___________ ,相同条件下(同温同压)的体积之比为___________ 。
(3)在标准状况下①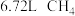 ②
② 个
个 分子③
分子③ ④
④ ,物质的量最大的是
,物质的量最大的是___________ ,氢原子个数最多的是___________ 。(填写序号)
(4)同温同压条件下, 和
和 混合气体相对氢气的密度为11,则两者的体积比是
混合气体相对氢气的密度为11,则两者的体积比是___________ 。
(5)已知反应 ,产物B、C、D均为气体,混合气体相对氢气密度为15,则A的相对分子质量为
,产物B、C、D均为气体,混合气体相对氢气密度为15,则A的相对分子质量为___________ 。
(6)一个 原子质量为
原子质量为 ,一个B原子质量为
,一个B原子质量为 ,一个
,一个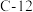 原子质量为C,阿伏加德罗常数为
原子质量为C,阿伏加德罗常数为 ,则
,则 分子的相对分子质量为
分子的相对分子质量为___________ 或___________ 。
(1)标准状况下
 中含
中含(2)标准状况下,等质量的
 和
和 物质的量之比是
物质的量之比是(3)在标准状况下①
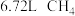 ②
② 个
个 分子③
分子③ ④
④ ,物质的量最大的是
,物质的量最大的是(4)同温同压条件下,
 和
和 混合气体相对氢气的密度为11,则两者的体积比是
混合气体相对氢气的密度为11,则两者的体积比是(5)已知反应
 ,产物B、C、D均为气体,混合气体相对氢气密度为15,则A的相对分子质量为
,产物B、C、D均为气体,混合气体相对氢气密度为15,则A的相对分子质量为(6)一个
 原子质量为
原子质量为 ,一个B原子质量为
,一个B原子质量为 ,一个
,一个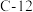 原子质量为C,阿伏加德罗常数为
原子质量为C,阿伏加德罗常数为 ,则
,则 分子的相对分子质量为
分子的相对分子质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】物质的量是沟通宏观和微观的桥梁,请回答下列问题:
(1)标准状况下,同体积的氨气(NH3)和硫化氢(H2S)气体的物质的量之比为___________ ,质量之比为___________ ;同温同压下,同质量的氮气(N2)和氧气(O2)的物质的量之比为___________ 。
(2)实验室欲配置460 mL 0.1mol·L-1碳酸钠溶液,实验时应选用的仪器有托盘天平(精确度0.1g)、玻璃棒、烧杯、___________ 。
(3)实验中应用托盘天平称取碳酸钠质量为___________ g。
(4)在容量瓶的使用方法中,下列操作不正确的是___________ (填序号)。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,瓶中残余少量水,对实验无影响
C.配制溶液时,把称好的碳酸钠倒入容量瓶中,加蒸馏水到刻度线
D.配制溶液结束后,可将溶液储存在容量瓶中
E.盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转和摇动多次
(1)标准状况下,同体积的氨气(NH3)和硫化氢(H2S)气体的物质的量之比为
(2)实验室欲配置460 mL 0.1mol·L-1碳酸钠溶液,实验时应选用的仪器有托盘天平(精确度0.1g)、玻璃棒、烧杯、
(3)实验中应用托盘天平称取碳酸钠质量为
(4)在容量瓶的使用方法中,下列操作不正确的是
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,瓶中残余少量水,对实验无影响
C.配制溶液时,把称好的碳酸钠倒入容量瓶中,加蒸馏水到刻度线
D.配制溶液结束后,可将溶液储存在容量瓶中
E.盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转和摇动多次
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】(1)下列物质能导电的是___ ,属于电解质的是___ 。
①NaCl晶体 ②液态SO2 ③液态醋酸 ④铜 ⑤BaSO4固体 ⑥纯蔗糖(C12H22O11) ⑦氨水 ⑧熔化的KNO3
(2)0.5molCH4的质量是___ g,在标准状况下的体积为___ L;
(3)8.4g氮气和9.6g某单质Rx所含原子个数相同,且分子个数之比为3:2,则x的值是___ ,R的摩尔质量是___ 。
①NaCl晶体 ②液态SO2 ③液态醋酸 ④铜 ⑤BaSO4固体 ⑥纯蔗糖(C12H22O11) ⑦氨水 ⑧熔化的KNO3
(2)0.5molCH4的质量是
(3)8.4g氮气和9.6g某单质Rx所含原子个数相同,且分子个数之比为3:2,则x的值是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)与16gO2所含原子总数相同的NH3标准状况下体积是________ L;
(2)已知2L Al2(SO4)3溶液中c(Al3+)=3mol/L,它与3L__________ mol/LNa2SO4中SO42-的物质的量浓度相等。
(3)同温同压下:同体积的NH3和H2S气体的质量比为_____________ ;同质量的NH3和H2S气体的体积比为___________ ,其中含有的氢的原子个数比为________ ;若NH3和H2S中的氢原子数相等,它们的体积比为____________ 。
(4)在标准状况下,8.96L的CH4和CO的混合气体,混合气体对氢气相对密度是9.5,则混合气体中CH4的体积为____________ ,CH4和CO原子个数比为_______________ 。
(2)已知2L Al2(SO4)3溶液中c(Al3+)=3mol/L,它与3L
(3)同温同压下:同体积的NH3和H2S气体的质量比为
(4)在标准状况下,8.96L的CH4和CO的混合气体,混合气体对氢气相对密度是9.5,则混合气体中CH4的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某双原子分子构成的气体,其摩尔质量为M g·mol-1,该气体的质量为m g,阿伏加 德罗常数为NA,则:
(1)该气体在标准状况下的体积为____ L;
(2)该气体在标准状况下的密度为____ g·L-1;
(3)该气体所含的原子总数为____ ;
(4)该气体的一个分子的质量为____ g。
(1)该气体在标准状况下的体积为
(2)该气体在标准状况下的密度为
(3)该气体所含的原子总数为
(4)该气体的一个分子的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】ⅰ.现有mg某气体,它由双原子分子构成,它的摩尔质量为Mg·mol-1.若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为___________ mol。
(2)该气体所含原子总数为___________ 个。
(3)该气体在标准状况下的体积为___________ L。
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为___________ 。
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为___________ mol/L。
2.已知某饱和NaCl溶液的体积为V mL。密度为ρ g/cm3,质量分数为 %。物质的量浓度为c mol/L,溶液中含NaCl的质量为m g。
%。物质的量浓度为c mol/L,溶液中含NaCl的质量为m g。
(6)用m、V表示溶液物质的量浓度___________ 。
(7)用 、ρ表示溶液物质的量浓度
、ρ表示溶液物质的量浓度___________ 。
(8)用c、ρ表示溶液的质量分数___________ 。
(9)用 表示该温度下NaCl的溶解度
表示该温度下NaCl的溶解度___________ 。
(1)该气体的物质的量为
(2)该气体所含原子总数为
(3)该气体在标准状况下的体积为
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为
(5)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为
2.已知某饱和NaCl溶液的体积为V mL。密度为ρ g/cm3,质量分数为
 %。物质的量浓度为c mol/L,溶液中含NaCl的质量为m g。
%。物质的量浓度为c mol/L,溶液中含NaCl的质量为m g。(6)用m、V表示溶液物质的量浓度
(7)用
 、ρ表示溶液物质的量浓度
、ρ表示溶液物质的量浓度(8)用c、ρ表示溶液的质量分数
(9)用
 表示该温度下NaCl的溶解度
表示该温度下NaCl的溶解度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】填写下列空白:
(1)含有6.02×1023个H的H2O,其物质的量是_____ mol;某硫酸钠溶液中含有3.01×1023个Na+,则溶液中SO 的物质的量是
的物质的量是 _______ mol,该溶液中Na2SO4的质量为 ____ g。
(2)______ mol H2O中含有的氧原子数与1.5 mol CO2中含有的氧原子数相等。
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为_____ 。
(4)已知16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为____ 。
(5)写出与下列化学方程式相对应的离子方程式:
①2HCl+Ba(OH)2=BaCl2+2H2O_____
②BaCl2+K2SO4=BaSO4↓+2KCl______
(1)含有6.02×1023个H的H2O,其物质的量是
 的物质的量是
的物质的量是 (2)
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为
(4)已知16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为
(5)写出与下列化学方程式相对应的离子方程式:
①2HCl+Ba(OH)2=BaCl2+2H2O
②BaCl2+K2SO4=BaSO4↓+2KCl
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】向蔗糖(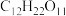 )中滴入98%的浓硫酸,蔗糖会变成疏松的“炭块”,同时产生
)中滴入98%的浓硫酸,蔗糖会变成疏松的“炭块”,同时产生 ,
, ;
; 可用酸性高锰酸钾溶液吸收。请回答下列问题:
可用酸性高锰酸钾溶液吸收。请回答下列问题:
(1)蔗糖的摩尔质量为______ 。17.1 g 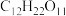 的物质的量为
的物质的量为______ 。
(2)500℃时,34.2 g蔗糖完全燃烧,产生两种气体的体积之比为______ ,其中产生 的体积(折算成标准状况下)为
的体积(折算成标准状况下)为______ L。
(3)质量分数为98%、密度为1.84 g⋅cm 的浓硫酸的物质的量浓度为
的浓硫酸的物质的量浓度为______ mol·L ;酸性高锰酸钾溶液需要用浓度为3 mol⋅L
;酸性高锰酸钾溶液需要用浓度为3 mol⋅L 的硫酸酸化,则实验室配制50 mL该浓度的硫酸需质量分数为98%的浓硫酸
的硫酸酸化,则实验室配制50 mL该浓度的硫酸需质量分数为98%的浓硫酸______ mL,需要用到的定量仪器有______ 。
(4) 被酸性高锰酸钾溶液吸收发生反应的离子方程式为
被酸性高锰酸钾溶液吸收发生反应的离子方程式为______ 。
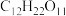 )中滴入98%的浓硫酸,蔗糖会变成疏松的“炭块”,同时产生
)中滴入98%的浓硫酸,蔗糖会变成疏松的“炭块”,同时产生 ,
, ;
; 可用酸性高锰酸钾溶液吸收。请回答下列问题:
可用酸性高锰酸钾溶液吸收。请回答下列问题:(1)蔗糖的摩尔质量为
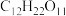 的物质的量为
的物质的量为(2)500℃时,34.2 g蔗糖完全燃烧,产生两种气体的体积之比为
 的体积(折算成标准状况下)为
的体积(折算成标准状况下)为(3)质量分数为98%、密度为1.84 g⋅cm
 的浓硫酸的物质的量浓度为
的浓硫酸的物质的量浓度为 ;酸性高锰酸钾溶液需要用浓度为3 mol⋅L
;酸性高锰酸钾溶液需要用浓度为3 mol⋅L 的硫酸酸化,则实验室配制50 mL该浓度的硫酸需质量分数为98%的浓硫酸
的硫酸酸化,则实验室配制50 mL该浓度的硫酸需质量分数为98%的浓硫酸(4)
 被酸性高锰酸钾溶液吸收发生反应的离子方程式为
被酸性高锰酸钾溶液吸收发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】物质的量在计算中有广泛的应用,请完成下列各小题:
(1)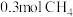 的质量是
的质量是_______ g,在标准状况下的体积为_______ L;含_______ 个氢原子(用 表示)。
表示)。
(2)将标准状况下 的
的 溶于水配成
溶于水配成 的溶液,所得溶液的物质的量浓度为
的溶液,所得溶液的物质的量浓度为_______ ,该溶液可与足量锌反应,产生的 在标准状况下体积为
在标准状况下体积为_______ 。
(3)当 和
和 所含分子数之比为
所含分子数之比为 时,其所含原子数之比为
时,其所含原子数之比为_______ ,质量之比为_______ 。
(4)在同温同压下, 某气体A的分子数与
某气体A的分子数与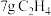 的分子数相等,则气体A的摩尔质量是
的分子数相等,则气体A的摩尔质量是_______  。
。
(5)硫酸镁和硫酸铝溶液等体积混合后,铝离子浓度为 ,硫酸根离子的浓度为
,硫酸根离子的浓度为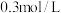 ,则混合溶液中镁离子浓度为
,则混合溶液中镁离子浓度为_______ 。
(6)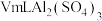 溶液中含
溶液中含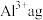 ,取
,取 溶液稀释到
溶液稀释到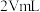 ,则稀释后溶液中
,则稀释后溶液中 的物质的量浓度是
的物质的量浓度是_______  。
。
(7)将 由铝、锌两种金属组成的混合物加入到
由铝、锌两种金属组成的混合物加入到 稀硫酸中,恰好完全反应,将反应后的溶液低温小心蒸干,得到无水固体
稀硫酸中,恰好完全反应,将反应后的溶液低温小心蒸干,得到无水固体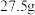 ,则原稀硫酸中溶液的质量分数为
,则原稀硫酸中溶液的质量分数为_______ 。
(8)在硫酸、硫酸铜、硫酸铁的混合溶液 中,各阳离子物质的量浓度相等,硫酸根离子的浓度为
中,各阳离子物质的量浓度相等,硫酸根离子的浓度为 。此溶液中铜离子的物质的量为
。此溶液中铜离子的物质的量为_______ ,此溶液理论上最多可溶解铁粉_______ g。[已知:铁能与硫酸铁溶液发生反应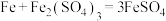 ]
]
(1)
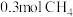 的质量是
的质量是 表示)。
表示)。(2)将标准状况下
 的
的 溶于水配成
溶于水配成 的溶液,所得溶液的物质的量浓度为
的溶液,所得溶液的物质的量浓度为 在标准状况下体积为
在标准状况下体积为(3)当
 和
和 所含分子数之比为
所含分子数之比为 时,其所含原子数之比为
时,其所含原子数之比为(4)在同温同压下,
 某气体A的分子数与
某气体A的分子数与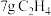 的分子数相等,则气体A的摩尔质量是
的分子数相等,则气体A的摩尔质量是 。
。(5)硫酸镁和硫酸铝溶液等体积混合后,铝离子浓度为
 ,硫酸根离子的浓度为
,硫酸根离子的浓度为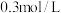 ,则混合溶液中镁离子浓度为
,则混合溶液中镁离子浓度为(6)
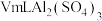 溶液中含
溶液中含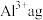 ,取
,取 溶液稀释到
溶液稀释到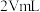 ,则稀释后溶液中
,则稀释后溶液中 的物质的量浓度是
的物质的量浓度是 。
。(7)将
 由铝、锌两种金属组成的混合物加入到
由铝、锌两种金属组成的混合物加入到 稀硫酸中,恰好完全反应,将反应后的溶液低温小心蒸干,得到无水固体
稀硫酸中,恰好完全反应,将反应后的溶液低温小心蒸干,得到无水固体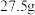 ,则原稀硫酸中溶液的质量分数为
,则原稀硫酸中溶液的质量分数为(8)在硫酸、硫酸铜、硫酸铁的混合溶液
 中,各阳离子物质的量浓度相等,硫酸根离子的浓度为
中,各阳离子物质的量浓度相等,硫酸根离子的浓度为 。此溶液中铜离子的物质的量为
。此溶液中铜离子的物质的量为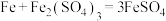 ]
]
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)0.25 mol某固体A的质量是15 g,A的相对分子质量为______________ 。
(2)在同温同压同体积的条件下,H2与气体A的质量之比是1∶8,则A的摩尔质量为_________ 。
(3)当SO2和SO3中分子个数比为1:1 时,原子总数之比为______ ,质量之比为______ .
(4)将5mol/L的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3﹣的物质的量浓度是______ mol•L﹣1。
(5)中和含0.2mol HCl的稀盐酸,需NaOH的质量为____________ g.
(6)在同温同压下,气体A与空气的密度之比为2,则A的摩尔质量为____________ 。
(2)在同温同压同体积的条件下,H2与气体A的质量之比是1∶8,则A的摩尔质量为
(3)当SO2和SO3中分子个数比为1:1 时,原子总数之比为
(4)将5mol/L的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3﹣的物质的量浓度是
(5)中和含0.2mol HCl的稀盐酸,需NaOH的质量为
(6)在同温同压下,气体A与空气的密度之比为2,则A的摩尔质量为
您最近一年使用:0次



