关于自发反应的叙述正确的是 ( )
| A.常温下的自发反应一定是不需要条件就能自发的反应,因此氮气和氢气合成氨气的反应在常温下不能自动发生 |
| B.常温下自然界发生的任何反应都是自发反应,光合作用是自发反应 |
| C.电解水在通常状况下是非自发反应,因此水在任何条件下生成氢气和氧气均为非自发反应 |
| D.某个反应是放热、熵增大的反应,该反应一定能自发进行 |
更新时间:2017-11-05 09:03:25
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】下列反应中,属于吸热反应的是
| A.铝热反应 |
| B.钠与水反应 |
| C.盐酸和氢氧化钠溶液反应 |
D.将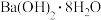 晶体和 晶体和 晶体研细后混合并搅拌 晶体研细后混合并搅拌 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列化学反应过程中的能量变化符合如图所示的是


A.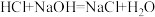 |
B.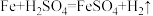 |
C. |
D. |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列有关化学反应方向及其判据的说法中错误的是
A.  能否自发进行与温度有关 能否自发进行与温度有关 |
B.常温下,反应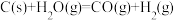 不能自发进行,则该反应的 不能自发进行,则该反应的 |
C. 溶于水放热,说明其溶于水的反应是放热反应,是自发过程 溶于水放热,说明其溶于水的反应是放热反应,是自发过程 |
D.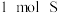 在不同状态时的熵值: 在不同状态时的熵值: |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列反应既是氧化还原反应又是吸热反应的是( )
| A.电解水 | B.碳酸钙的分解 |
| C.铝与盐酸反应 | D.氢氧化钡与氯化铵反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】化学反应中的能量变化,通常主要表现为热量的变化。下列相关表述正确的是
| A.已知C(石墨,s)= C(金刚石,s) ∆H>0,则金刚石比石墨稳定 |
B.一定条件下,将0.5mol H2和0.5mol I2(g)置于密闭容器中充分反应生成HI放热akJ,其热化学方程式为:H2(g)+I2(g) 2HI(g) ∆H=-2akJ/mol 2HI(g) ∆H=-2akJ/mol |
| C.C(s)+O2(g)=CO2(g) ΔH1;C(s)+ O2(g)=CO2(l) ΔH2,则ΔH1>ΔH2 |
| D.H+和OH-反应的中和热∆H=-57.3kJ/mol,则H2SO4和Ba(OH)2反应焓变∆H=-114.6kJ/mol |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】在298K时,NaCl在水中的溶解度为26g。如将1mol NaCl溶解在1L水中,此溶解过程中体系的ΔH-TΔS和熵如何变化
| A.ΔH-TΔS>0,ΔS>0 | B.ΔH-TΔS<0,ΔS>0 |
| C.ΔH-TΔS>0,ΔS<0 | D.ΔH-TΔS<0,ΔS<0 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】CO2转化为燃料甲醇是实现碳中和的途径之一,在恒温恒容密闭容器中进行反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH<0,下列有关说法正确的是
CH3OH(g)+H2O(g) ΔH<0,下列有关说法正确的是
 CH3OH(g)+H2O(g) ΔH<0,下列有关说法正确的是
CH3OH(g)+H2O(g) ΔH<0,下列有关说法正确的是| A.该反应的正反应为熵增过程,ΔS>0 |
| B.该反应在高温下可自发进行 |
| C.CH3OH分子中每个原子均满足8电子稳定结构 |
| D.降低温度有利于提高甲醇的产率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】反应mA(g)+nB(g)=qC(g)在高温时能自发进行,反应后体系中物质的总能量升高,则该反应的△H、△S应为
| A.△H>0,△S>0 | B.△H>0,△S<0 |
| C.△H<0,△S>0 | D.△H<0,△S<0 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列判断反应自发性的描述正确的是
| A.焓减少的反应一定可以自发进行 | B.焓增加的反应可能自发进行 |
| C.熵增加的反应一定可以自发进行 | D.熵减少的反应一定不能自发进行 |
您最近一年使用:0次

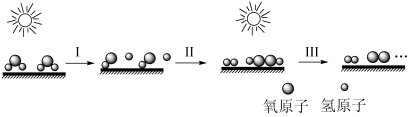

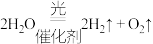
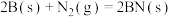

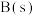 、
、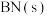 、
、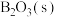 熔点分别约为
熔点分别约为 、
、 、
、 ,下列说法正确的是
,下列说法正确的是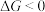 ,因此速率快
,因此速率快 ,
,


