(1)有镁和铁的混合物共4.0克,与200毫升盐酸恰好完全反应,在标准状况下共收集到2.24L气体。假设反应后溶液体积不变,则铁的质量为_____ g;反应后溶液中Mg2+的物质的量浓度为_______ 。
(2)一定量氢气在氯气中燃烧,所得混合气体用 100 mL、2.00 moL·L-1NaOH 溶液恰好完全吸收,测得溶液中含有 NaClO 的物质的量为 0.05mol。试计算下列问题: 所得溶液中 Cl-的物质的量为_______ ;所用氯气和参加反应的氢气的物质的量之比n(C12):n(H2)为 _______ 。
(2)一定量氢气在氯气中燃烧,所得混合气体用 100 mL、2.00 moL·L-1NaOH 溶液恰好完全吸收,测得溶液中含有 NaClO 的物质的量为 0.05mol。试计算下列问题: 所得溶液中 Cl-的物质的量为
更新时间:2017-11-13 14:28:05
|
相似题推荐
计算题
|
较难
(0.4)
名校
【推荐1】H2和Cl2组成的混合气体,经光照充分反应后气体中存在的物质可能有的情况为:
a_____ ;b______________ ;c_____________ 。
将反应后的气体通入100mL1.0mol/L NaOH溶液中,图中表示溶液中某种离子的物质的量随通入气体体积的变化曲线

(1)图中表示溶液中__________ 离子的变化的曲线。
(2)如图,当n=0.02mol时,光照前的混合气体中H2和Cl2的体积之比为__________
a
将反应后的气体通入100mL1.0mol/L NaOH溶液中,图中表示溶液中某种离子的物质的量随通入气体体积的变化曲线

(1)图中表示溶液中
(2)如图,当n=0.02mol时,光照前的混合气体中H2和Cl2的体积之比为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】一定量的氢气在氯气中充分燃烧,所得混合物用200mL 2.00mo/L的NaOH溶液(密度为1.12g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.05mol。
(1)求所得溶液中Cl-的物质的量_____ 。
(2)求原混合气体中氯气和氢气的物质的量之比_____ 。
(1)求所得溶液中Cl-的物质的量
(2)求原混合气体中氯气和氢气的物质的量之比
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】有一镁铝混合物重a g,取其一半和足量的盐酸反应,放出V1L的氢气。取其另一半和足量的NaOH溶液反应,放出V2L的氢气(均为标况下)。求混合物中镁和铝的质量比。_____________
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】将一定质量的Al、Mg混合物加入到足量的盐酸中,充分反应后得到标准状况下的氢气8.96L;如果将等质量的该混合物加入到足量的NaOH溶液中,充分反应后得到标准状况下的氢气6.72L.
(1)当混合物与盐酸反应时,转移电子总物质的质量为______ mol;
(2)求混合物中Al质量为__________ gMg的质量为_________ g
(1)当混合物与盐酸反应时,转移电子总物质的质量为
(2)求混合物中Al质量为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】甲、乙、丙三组实验中均取30 mL同浓度的盐酸,加入同一种镁铝合金粉末,加入合金的质量与生成气体的体积(已换算成标准状况下)的有关数据如表所示:
(1)甲、乙两组实验中,哪一组盐酸是已完全反应的?___ (填“甲”或“乙”),理由是_______ 。
(2)盐酸的物质的量浓度为________ 。
(3)合金中Mg、Al的物质的量之比为_____________ 。
| 实验序号 | 甲 | 乙 | 丙 |
| 合金的质量/mg | 255 | 385 | 459 |
| 生成气体的体积/mL | 280 | 336 | 336 |
(2)盐酸的物质的量浓度为
(3)合金中Mg、Al的物质的量之比为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】(1)将铁和氧化铁的混合物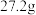 投入到
投入到 某浓度的硫酸溶液中,恰好完全反应,并产生
某浓度的硫酸溶液中,恰好完全反应,并产生 (标准状况),向反应后的溶液中滴入
(标准状况),向反应后的溶液中滴入 溶液,溶液不显红色。试计算所用硫酸溶液的物质的量浓度
溶液,溶液不显红色。试计算所用硫酸溶液的物质的量浓度______________ 。
(2)将一定质量的铁、氧化铁、氧化铜的固体混合物加入 盐酸中,充分反应后产生
盐酸中,充分反应后产生 (标准状况),残留固体
(标准状况),残留固体 。过滤,滤液中无
。过滤,滤液中无 。将滤液加水稀释到
。将滤液加水稀释到 ,测得其中
,测得其中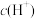 为
为 。试计算原混合物中单质铁的质量
。试计算原混合物中单质铁的质量______________ 。
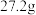 投入到
投入到 某浓度的硫酸溶液中,恰好完全反应,并产生
某浓度的硫酸溶液中,恰好完全反应,并产生 (标准状况),向反应后的溶液中滴入
(标准状况),向反应后的溶液中滴入 溶液,溶液不显红色。试计算所用硫酸溶液的物质的量浓度
溶液,溶液不显红色。试计算所用硫酸溶液的物质的量浓度(2)将一定质量的铁、氧化铁、氧化铜的固体混合物加入
 盐酸中,充分反应后产生
盐酸中,充分反应后产生 (标准状况),残留固体
(标准状况),残留固体 。过滤,滤液中无
。过滤,滤液中无 。将滤液加水稀释到
。将滤液加水稀释到 ,测得其中
,测得其中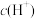 为
为 。试计算原混合物中单质铁的质量
。试计算原混合物中单质铁的质量
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】为确定Fe2O3和Cu混合物的组成(假设混合均匀),某兴趣小组称取五份不同质量的样品,分别投入15.0mL某浓度的稀硫酸中。充分反应后,每组样品剩余固体的质量与原样品质量的关系如图所示。
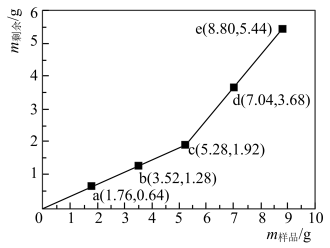
(1)该混合物中n(Fe2O3)︰n(Cu)=_______ 。
(2)稀硫酸的浓度为_______ mol/L。

(1)该混合物中n(Fe2O3)︰n(Cu)=
(2)稀硫酸的浓度为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】将一定量混合均匀的铁粉与硫粉在隔绝空气的条件下共热,充分反应后冷却至室温,得到固体A。将质量为m的固体A加入到300 mL 2 mol/L盐酸中使之完全溶解。测得室温下加入固体A的质量与收集到气体体积(已换算成标准状况)的关系如右图所示(假设所得氢硫酸溶液饱和前无硫化氢气体逸出)。已知:
①加入固体A的质量m≤3.2 g时,收集到的气体为H2;
②当m>3.2 g时,收集到的气体为H2和H2S的混合气体。

⑴3.2 g固体A中所含的物质有______________ 。
⑵3.2 g固体A中各物质的物质的量分别为______________ ,溶于上述盐酸充分反应后,所得溶液中氢硫酸的物质的量浓度为______________ (忽略溶液体积的变化)。
⑶当固体A全部溶于上述盐酸,且A的质量m>3.2 g时,收集到的气体体积(标准状况下)V=______________ mL(用含m的代数式表示)。
①加入固体A的质量m≤3.2 g时,收集到的气体为H2;
②当m>3.2 g时,收集到的气体为H2和H2S的混合气体。

⑴3.2 g固体A中所含的物质有
⑵3.2 g固体A中各物质的物质的量分别为
⑶当固体A全部溶于上述盐酸,且A的质量m>3.2 g时,收集到的气体体积(标准状况下)V=
您最近一年使用:0次

 溶液恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500 mol。
溶液恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500 mol。


