已知FeS溶于盐酸中,生成FeCl2和H2S气体。现将8.8g FeS固体置于200mL、2.0mol•L﹣1的盐酸中,以制备H2S气体。反应完全后,若溶液中H2S的浓度为0.10mol•L﹣1,假定溶液体积不变,试计算:
(1)收集到标准状况下H2S气体的体积_______
(2)溶液中Fe2+物质的量浓度_______
(1)收集到标准状况下H2S气体的体积
(2)溶液中Fe2+物质的量浓度
更新时间:2017-11-09 19:17:10
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】电解26.8%的食盐水1500g,若食盐的利用率为87.3%,求:
(1)在标准状况下可制得Cl2多少升?___ (不考虑氯气溶解)
(2)电解液中氢氧化钠的质量百分比浓度为多少?___
(3)取一定量的氢气和氯气混合,点燃充分反应,所得混合物用100mL15.67%的NaOH溶液(密度为1.12g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol。求溶液中NaCl的物质的量浓度___ ,以及所取氢气和氯气的混合气体相对于同温同压下空气的相对密度,假设反应前后溶液体积不变,结果保留两位小数。___
(1)在标准状况下可制得Cl2多少升?
(2)电解液中氢氧化钠的质量百分比浓度为多少?
(3)取一定量的氢气和氯气混合,点燃充分反应,所得混合物用100mL15.67%的NaOH溶液(密度为1.12g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol。求溶液中NaCl的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】利用“化学计量在实验中的应用”的相关知识填空。
(1)含有6.02×1023个氧原子的H2SO4的物质的量是___________ 。
(2)与标准状况下V LCO2所含氧原子数目相同的水的质量是___________ g(用分式表示)
(3)设NA为阿伏加 德罗常数的数值,如果a g氧气中含有的分子数为b,则c g氧气在标准状况下的体积约是________ (用含NA的式子表示)。
(4)将4 g NaOH溶解在水中配成10 mL溶液,再稀释成1 L,从中取出10 mL,这10 mL溶液的物质的量浓度为_______ 。
(5)体积比为1∶2∶3的氯化钠、氯化镁和氯化铝溶液,分别加入等体积、等浓度的硝酸银溶液,均恰好完全反应生成氯化银沉淀,则这三种溶液的物质的量浓度之比为_________ 。
(1)含有6.02×1023个氧原子的H2SO4的物质的量是
(2)与标准状况下V LCO2所含氧原子数目相同的水的质量是
(3)设NA为阿伏加 德罗常数的数值,如果a g氧气中含有的分子数为b,则c g氧气在标准状况下的体积约是
(4)将4 g NaOH溶解在水中配成10 mL溶液,再稀释成1 L,从中取出10 mL,这10 mL溶液的物质的量浓度为
(5)体积比为1∶2∶3的氯化钠、氯化镁和氯化铝溶液,分别加入等体积、等浓度的硝酸银溶液,均恰好完全反应生成氯化银沉淀,则这三种溶液的物质的量浓度之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】中国古代科学家在化学取得了非常多的成就。
素材I.“熬胆矾铁釜,久之亦化为铜”涉及到化学反应为: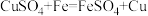 。
。
素材Ⅱ.宋代《洗冤集录》中记载有“银针探毒”,其原理是: 。
。
素材Ⅲ.我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为: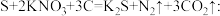 。回答下列问题:
。回答下列问题:
(1)该反应中 的摩尔质量是
的摩尔质量是___________ 。
(2) 铁粉中含有的
铁粉中含有的 原子数目为
原子数目为___________ 。
(3)若 铁粉完全反应,析出
铁粉完全反应,析出 单质的质量为
单质的质量为___________ 。
(4)在相同条件下体积相同的 和
和 两种气体分子数之比为
两种气体分子数之比为___________ 。
(5)“银针探毒”反应中, 完全反应时,消耗的
完全反应时,消耗的 的体积为
的体积为___________ L。
(6)黑火药反应中,化合价升高的元素是___________ (填元素符号)。
(7)黑火药反应中,作为氧化剂的物质是___________ (填化学式)。
(8)向空气中排放 会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
该雨水中氢离子的浓度a=___________ 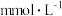 。
。
素材I.“熬胆矾铁釜,久之亦化为铜”涉及到化学反应为:
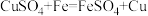 。
。素材Ⅱ.宋代《洗冤集录》中记载有“银针探毒”,其原理是:
 。
。素材Ⅲ.我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为:
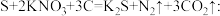 。回答下列问题:
。回答下列问题:(1)该反应中
 的摩尔质量是
的摩尔质量是(2)
 铁粉中含有的
铁粉中含有的 原子数目为
原子数目为(3)若
 铁粉完全反应,析出
铁粉完全反应,析出 单质的质量为
单质的质量为(4)在相同条件下体积相同的
 和
和 两种气体分子数之比为
两种气体分子数之比为(5)“银针探毒”反应中,
 完全反应时,消耗的
完全反应时,消耗的 的体积为
的体积为(6)黑火药反应中,化合价升高的元素是
(7)黑火药反应中,作为氧化剂的物质是
(8)向空气中排放
 会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:| 离子 |  |  |  |  |  |
浓度(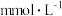 ) ) | 0.06 | 0.08 | 0.02 | 0.04 | a |
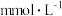 。
。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】用Cu与浓硫酸反应,得到的体积为2..24L(标准状况)。试计算:
(1)被还原的H2SO4的物质的量_______
(2)把所得到的CuSO4配制成500mlLCuSO4溶液,所得溶液中溶质的物质的量浓度为___ 。
(1)被还原的H2SO4的物质的量
(2)把所得到的CuSO4配制成500mlLCuSO4溶液,所得溶液中溶质的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】将 4.6g 金属钠投入一定量的水中,待反应完毕后,得到 100mL 溶液.求:
(1)标准状况下产生氢气多少 mL_______________ ?
(2)所得溶液的物质的浓度是多少_____________ ?
(1)标准状况下产生氢气多少 mL
(2)所得溶液的物质的浓度是多少
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】阿伏加 德罗常数的近似值为6.02×1023.按要求完成下列填空:
(1)1mol Cl2中约含有______ 个氯气分子,约含有______ 个氯原子,含有6.02×1023个氢原子的H2SO4的物质的量是______ ;
(2)标准状况下11.2L N2O4和______ mol NO所含有的原子数相等。
(3)某硫酸钠溶液中含有3.01×1023个Na+,则该溶液中SO42-的物质的量是______ 。
(4)2L 1mol/L MgCl2中镁离子的物质的量为______ ,Cl-的物质的量浓度为______ 。
(1)1mol Cl2中约含有
(2)标准状况下11.2L N2O4和
(3)某硫酸钠溶液中含有3.01×1023个Na+,则该溶液中SO42-的物质的量是
(4)2L 1mol/L MgCl2中镁离子的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】通过下列方法测定产品纯度:准确称取0.5000gCuSO4·5H2O样品,加适量水溶解,转移至碘量瓶中,加过量KI溶液并用稀H2SO4酸化,以淀粉溶液为指示剂,用0.1000mol∙L−1Na2S2O3标准溶液滴定至终点,消耗Na2S2O3的溶液19.80mL。测定过程中发生下列反应:2Cu2++4I-=2CuI↓+I2、2 +I2=
+I2=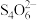 +2I-。计算CuSO4·5H2O样品的纯度(写出计算过程):
+2I-。计算CuSO4·5H2O样品的纯度(写出计算过程):_____ 。
 +I2=
+I2=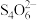 +2I-。计算CuSO4·5H2O样品的纯度(写出计算过程):
+2I-。计算CuSO4·5H2O样品的纯度(写出计算过程):
您最近一年使用:0次
【推荐2】饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,请配平化学方程式:10Al+6NaNO3+4NaOH+18H2O=10______ +3N2↑+2H2O若反应过程中转移5 mol电子,则生成标况下的N2体积为______ L.
您最近一年使用:0次



