X、Y、Z、W为原子序数递增的短周期主族元素,Y的简单气态氢化物水溶液呈弱碱性, Z元素无正价,且基态原子有2个未成对电子,基态W原子价层电子排布式为nsn-1npn-1 ,X与W为同主族元素。基态R原子M能层全充满且核外有且仅有1个未成对电子。请回答下列问题:
(1)基态R原子的核外电子排布式为____________________ 。R单质晶体晶胞的堆积方式_______________ ,晶胞的空间利用率为___________________ 。
(2) X、Y、Z三种元素的第一电离能由小到大的顺序为__________ (填“元素符号”,下同)
(3)YF3分子中Y的杂化类型为______________ 。该分子的空间构型为_________________ 。
(4)Y的气态氢化物在水中可形成氢键,其氢键最可能的形式为____________ 。

(5)X的某气态氧化物的相对分子质量为44,分子中的大π键可用符号Π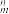 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则其气态氧化物中的大π键应表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则其气态氧化物中的大π键应表示为_______________ ,其中σ键与π数目之比为______________ 。
(6)R元素与Y元素形成某种化合物的晶胞结构如图所示(黑球代表R原子),若该晶体的密度为ρg·cm-3,则该晶胞的边长是_________ cm (NA表示阿伏伽德罗常数的值)。

(1)基态R原子的核外电子排布式为
(2) X、Y、Z三种元素的第一电离能由小到大的顺序为
(3)YF3分子中Y的杂化类型为
(4)Y的气态氢化物在水中可形成氢键,其氢键最可能的形式为

(5)X的某气态氧化物的相对分子质量为44,分子中的大π键可用符号Π
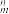 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则其气态氧化物中的大π键应表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则其气态氧化物中的大π键应表示为(6)R元素与Y元素形成某种化合物的晶胞结构如图所示(黑球代表R原子),若该晶体的密度为ρg·cm-3,则该晶胞的边长是

更新时间:2017-11-24 23:34:38
|
【知识点】 物质结构与性质综合考查解读
相似题推荐
解答题-结构与性质
|
适中
(0.65)
【推荐1】磷酸亚铁锂( )是锂离子电池电极材料,主要用于动力锂离子电池,作为正极活性物质使用,人们习惯也称其为磷酸铁锂。回答下列问题:
)是锂离子电池电极材料,主要用于动力锂离子电池,作为正极活性物质使用,人们习惯也称其为磷酸铁锂。回答下列问题:
(1)基态锂原子核外能量最高的电子电子云轮廓图形状为___________ ;基态磷原子第一电离能比基态硫的___________ (填“大”或“小”),原因是___________ 。
(2)实验室中可用KSCN或 来检验
来检验 。
。 与KSCN溶液混合,可得到配位数为5的配合物的化学式是
与KSCN溶液混合,可得到配位数为5的配合物的化学式是___________ ,其中硫、碳的杂化类型分别是___________ 、___________ 。
(3)磷酸和亚磷酸( )是磷元素的两种含氧酸。
)是磷元素的两种含氧酸。 的空间构型为
的空间构型为___________ ;亚磷酸与NaOH反应只生成 和
和 两种盐,则
两种盐,则 的结构简式为
的结构简式为___________ 。
(4) 和
和 都是三角锥形分子,但键角
都是三角锥形分子,但键角 ,可能的原因是
,可能的原因是___________ 。
(5)氧化亚铁晶体的晶胞如图。已知:氧化亚铁晶体的密度为ρ g⋅cm ,
, 代表阿伏加德罗常数的值。在该晶胞中,与
代表阿伏加德罗常数的值。在该晶胞中,与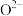 紧邻且等距离的
紧邻且等距离的 数目为
数目为___________ , 与
与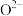 最短核间距为
最短核间距为___________ pm。
 )是锂离子电池电极材料,主要用于动力锂离子电池,作为正极活性物质使用,人们习惯也称其为磷酸铁锂。回答下列问题:
)是锂离子电池电极材料,主要用于动力锂离子电池,作为正极活性物质使用,人们习惯也称其为磷酸铁锂。回答下列问题:(1)基态锂原子核外能量最高的电子电子云轮廓图形状为
(2)实验室中可用KSCN或
 来检验
来检验 。
。 与KSCN溶液混合,可得到配位数为5的配合物的化学式是
与KSCN溶液混合,可得到配位数为5的配合物的化学式是(3)磷酸和亚磷酸(
 )是磷元素的两种含氧酸。
)是磷元素的两种含氧酸。 的空间构型为
的空间构型为 和
和 两种盐,则
两种盐,则 的结构简式为
的结构简式为(4)
 和
和 都是三角锥形分子,但键角
都是三角锥形分子,但键角 ,可能的原因是
,可能的原因是(5)氧化亚铁晶体的晶胞如图。已知:氧化亚铁晶体的密度为ρ g⋅cm
 ,
, 代表阿伏加德罗常数的值。在该晶胞中,与
代表阿伏加德罗常数的值。在该晶胞中,与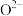 紧邻且等距离的
紧邻且等距离的 数目为
数目为 与
与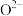 最短核间距为
最短核间距为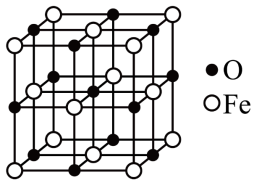
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】祖母绿的主要成分为Be3Al2Si6Ol8,含有O、Si、Al、Be等元素。请回答下列问题:
(1)基态A1原子中,电子占据的最高能级的符号是_______________________ ,该能级具有的原子轨道数为_______ 。
(2)在1000℃时,氯化铍以BeCl2形式存在,其中Be原子的杂化方式为_________ ;在500〜600℃气相中,氯化铍则以二聚体Be2Cl4的形式存在,画出Be2Cl4的结构____________ ,1molBe2Cl4中含有____ mol配位键。
(3)氢化铝锂(LiAlH4)是有机合成中一种重要的还原剂,LiAlH4的阴离子的空间构型为____________ ,该阴离子的等电子体为____________ (写一种分子、一种离子)。一种无限长单链结构的多硅酸根的一部分如图所示,则该硅酸根的化学式为____________________ 。
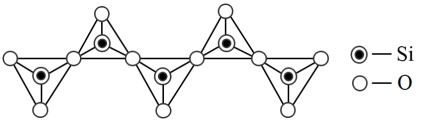
(4)用氧化物的形式表示出祖母绿的组成:___________ 。如图是Be与O形成的氧化物的立方晶胞结构,已知氧化铍的密度为ρg/cm3,则晶胞边长为__________ cm。(设NA为阿伏加 德罗常数的值,用含ρ、NA的代数式表示),O2-的配位数为_____________ 。

(1)基态A1原子中,电子占据的最高能级的符号是
(2)在1000℃时,氯化铍以BeCl2形式存在,其中Be原子的杂化方式为
(3)氢化铝锂(LiAlH4)是有机合成中一种重要的还原剂,LiAlH4的阴离子的空间构型为

(4)用氧化物的形式表示出祖母绿的组成:

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下表是元素周期表的一部分,表中所列的字母分别代表一种元素。
试回答下列问题(注意:每问中的字母代号为上表中的字母代号,并非为元素符号)
(1)N的单质和水蒸气反应能生成固体X,则I的单质与X高温下反应的化学方程式______ 。
(2)D的简单气态氢化物的VSEPR模型的名称为______ 。
(3)由A、C、D形成的ACD分子中,σ键和π键个数=______ 。
(4)元素M的化合物(ME2L2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。回答问题:
①ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是______ (填“极性”或“非极性”)分子。
②将N和O的单质用导线连接后插入D的最高价氧化物对应的水化物浓溶液中,可制成原电池,则组成负极材料的元素的外围电子轨道表示式为______ 。
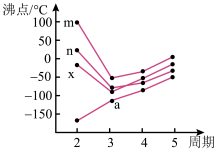
(5)如图四条折线分别表示ⅣA族、ⅤA族、ⅥA族、ⅦA族元素气态氢化物沸点变化,则E的氢化物所在的折线是______ (填m、n、x或y)。
| A | R | |||||||||||||||||
| B | C | D | E | F | T | |||||||||||||
| G | H | I | J | K | L | |||||||||||||
| M | N | O | ||||||||||||||||
试回答下列问题(注意:每问中的字母代号为上表中的字母代号,并非为元素符号)
(1)N的单质和水蒸气反应能生成固体X,则I的单质与X高温下反应的化学方程式
(2)D的简单气态氢化物的VSEPR模型的名称为
(3)由A、C、D形成的ACD分子中,σ键和π键个数=
(4)元素M的化合物(ME2L2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。回答问题:
①ME2L2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断ME2L2是
②将N和O的单质用导线连接后插入D的最高价氧化物对应的水化物浓溶液中,可制成原电池,则组成负极材料的元素的外围电子轨道表示式为
(5)如图四条折线分别表示ⅣA族、ⅤA族、ⅥA族、ⅦA族元素气态氢化物沸点变化,则E的氢化物所在的折线是

您最近一年使用:0次



