下图中甲为甲烷和O2构成的燃料电池示意图,电解质为KOH溶液,乙为电解饱和MgCl2溶液的装置,其中乙装置中X为阳离子交换膜。用该装置进行实验,反应开始后观察到Fe电极附近出现白色沉淀。下列说法正确 的是
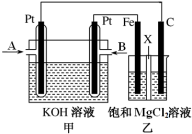

A.甲中A处通入CH4,电极反应式为CH4 + 10OH- - 8e- CO32-+ 7H2O CO32-+ 7H2O |
B.乙中电解MgCl2溶液的总反应为2Cl- + 2H2O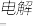 Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
| C.理论上甲中每消耗22.4 L CH4(标准状况下),乙中产生4 mol Cl2 |
| D.甲、乙中电解质溶液的pH都增大 |
更新时间:2017-09-13 15:20:50
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】通过传感器可以监测空气中甲醛的含量。一种燃料电池型甲醛气体传感器的原理如图所示,下列说法错误的是
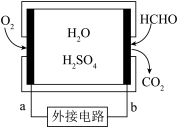

| A.b为电池的负极,甲醛被氧化 |
| B.a极的电极反应为O2+4e-+4H+==2H2O |
| C.传感器工作过程中,电解质溶液中硫酸的浓度不变 |
| D.当电路中转移1×10-4 mol电子时,传感器内参加反应的HCHO为0.75 mg |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】锂/氟化碳(Li/CFx)电池的工作原理如图所示。
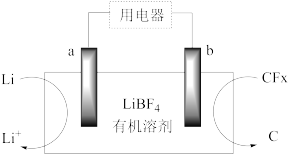
下列说法错误的是

下列说法错误的是
| A.电子由a极经用电器流向b极 |
| B.有机溶剂可能是羟基乙酸(HOCH2COOH) |
| C.正极上的电极反应式:CFx+xe-=C+xF- |
| D.14.0gLi参与反应理论上转移2mol电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
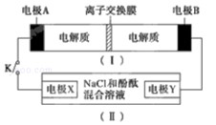
【推荐1】装置(Ⅰ)为铁镍(Fe﹣Ni)可充电电池:Fe+NiO2 Fe(OH)2+Ni(OH)2;装置(Ⅱ)为电解示意图,当闭合开关 K 时,Y 附近溶液先变红.下 列说法正确的是
Fe(OH)2+Ni(OH)2;装置(Ⅱ)为电解示意图,当闭合开关 K 时,Y 附近溶液先变红.下 列说法正确的是
 Fe(OH)2+Ni(OH)2;装置(Ⅱ)为电解示意图,当闭合开关 K 时,Y 附近溶液先变红.下 列说法正确的是
Fe(OH)2+Ni(OH)2;装置(Ⅱ)为电解示意图,当闭合开关 K 时,Y 附近溶液先变红.下 列说法正确的是
| A.闭合 K 时,X 的电极反应式为:2H++2e−═H2↑ |
| B.给装置(Ⅰ)充电时,OH−通过阴离子交换膜,移向 A 电 极 |
| C.给装置(Ⅰ)充电时,B 极参与反应的物质被氧化 |
| D.闭合 K 时,A 电极反应式为:NiO2 + 2e− +2H+═Ni(OH)2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】化学与社会、生活密切相关。下列说法正确的是
| A.明矾净水与自来水的杀菌清毒原理不同 |
| B.医学上常采用碳酸钡作为钡餐 |
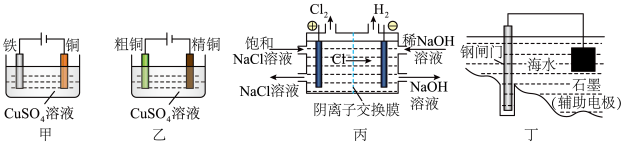
| C.粗铜精炼时,与电源正极相连的是纯铜,电极反应为:Cu-2e-=Cu2+ |
| D.泡沫灭火剂利用了硫酸铝溶液与碳酸钠溶液混合后能发生双水解反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
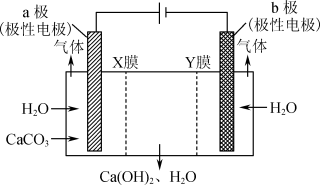
【推荐1】最近研究人员开发出一种生产水泥的绿色工艺,其中的电化学装置如图所示。装置工作时,下列说法正确的是

| A.化学能转变为电能 |
| B.X膜为阴离子交换膜 |
| C.阴极区溶液的pH不断变小 |
| D.a极上的电极反应式为2H2O-4e-=4H++O2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】工业上可以通过电解NO2制备NH4NO3,其工作原理如图所示,下列说法正确的是


| A.电解过程中,阴极区NO2流入速率比阳极区NO2流入速率快些 |
| B.阴极区消耗1molNO2需补充6mol化合物X |
| C.阳极反应为:NO2+e-+H2O=NO3-+2H+ |
| D.电解过程中,阴极区的pH小于阳极区的pH |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】碘化亚铜(CuI)是一种不溶于水的白色固体,它可由反应:2Cu2++4I-=2CuI↓+I2而制得。选取铜片、石墨、KI溶液组成电化学装置制取CuI。为确认反应情况,通电前在溶液中又加入了少量酚酞试液和淀粉溶液。电解一段时间后得到白色沉淀,同时阴极区溶液变红,阳极区溶液变蓝。下列说法不正确 的是
| A.铜片做阳极,石墨做阴极 |
| B.白色沉淀在靠近阳极处产生 |
| C.阴极区溶液变红的原因:2H++2e-=H2↑,促进H2O电离,c(OH-)升高 |
| D.阳极区溶液变蓝的原因:4OH--4e-=2H2O+O2↑,O2将I-氧化为I2,I2遇淀粉变蓝 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】利用电化学原理可对海水(主要成分 和
和 ,还含有少量微生物)进行消毒,并能清除残留的含氯消毒物质(工作原理如图,其中电极均为惰性电极)。已知:工作时,先断开
,还含有少量微生物)进行消毒,并能清除残留的含氯消毒物质(工作原理如图,其中电极均为惰性电极)。已知:工作时,先断开 ,闭合
,闭合 ,一段时间后,断开
,一段时间后,断开 ,闭合
,闭合 。下列说法不正确的是( )
。下列说法不正确的是( )

 和
和 ,还含有少量微生物)进行消毒,并能清除残留的含氯消毒物质(工作原理如图,其中电极均为惰性电极)。已知:工作时,先断开
,还含有少量微生物)进行消毒,并能清除残留的含氯消毒物质(工作原理如图,其中电极均为惰性电极)。已知:工作时,先断开 ,闭合
,闭合 ,一段时间后,断开
,一段时间后,断开 ,闭合
,闭合 。下列说法不正确的是( )
。下列说法不正确的是( )
A.闭合 后的总反应为 后的总反应为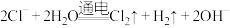 |
B.闭合 后, 后, 通过离子交换膜从Ⅱ室迁移至Ⅲ室 通过离子交换膜从Ⅱ室迁移至Ⅲ室 |
| C.工作完成后,Ⅱ室中有金属Na剩余 |
| D.残留的含氯消毒物质在Ⅲ室放电被脱除 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
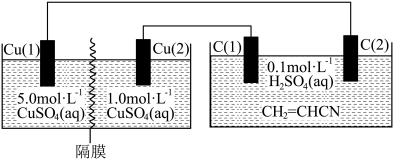
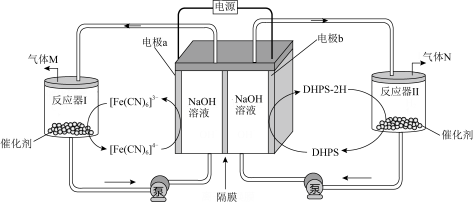
【推荐2】浓差电池指利用两极电解质溶液中浓度不同引起的电势差放电。实验室利用浓差电池实现电解丙烯腈( )合成己二腈[
)合成己二腈[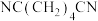 ],装置如图所示(实验前,隔膜两侧溶液均为200 mL,铜电极质量均为100 g)。
],装置如图所示(实验前,隔膜两侧溶液均为200 mL,铜电极质量均为100 g)。
下列说法正确的是
 )合成己二腈[
)合成己二腈[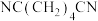 ],装置如图所示(实验前,隔膜两侧溶液均为200 mL,铜电极质量均为100 g)。
],装置如图所示(实验前,隔膜两侧溶液均为200 mL,铜电极质量均为100 g)。
下列说法正确的是
A.Cu(1)极为负极,其电极反应为 |
| B.隔膜为阴离子交换膜,C(2)极为阴极 |
| C.上述装置理论上可制备0.6 mol己二腈 |
| D.当电解停止时,Cu(1)极与Cu(2)极质量相差51.2 g |
您最近一年使用:0次

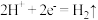
 4[Fa(CN)6]4-+O2↑+2H2O
4[Fa(CN)6]4-+O2↑+2H2O

