次氯酸钠稳定性远高于次氯酸钠,也可用于杀菌消毒。制备次氯酸钠方法较多,常用的一种合成路线如下:
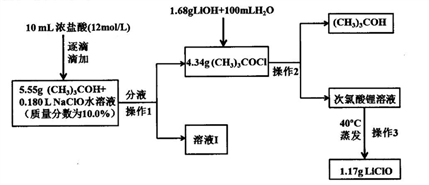
已知:1.次氯酸叔丁酯((CH3)3COCl),相对分子质量为108.5,是具有挥发性的黄色油状液体,密度为0.802g/mL,且有强烈刺激性臭味;2.(CH3)3COCl+LiOH=LiClO+(CH3)3COH
请回答:
(1)实验第一步的反应装置如图所示(夹持装置省略),B装置中支管的作用是___________ ;浓盐酸逐滴滴加而不是一次性加入的原因是_______________ 。
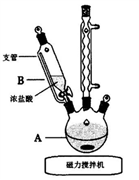
(2)请写出在装置A中发生反应的化学方程式___________________ 。
(3)对于操作1,下列说法不正确的是__________ 。
A.可以选用250mL规格的分液漏斗
B.操作1须在通风橱内进行
C.进行分液时,可提早关闭旋塞,以防止次氯酸叔丁酯从下口流出
D.装置B不合适进行操作1
(4)进行操作3时,并不是直接加热蒸发溶液,而是选择在40°C下缓慢蒸发溶液,试解释其原因__________ 。
(5)该实验中次氯酸锂的产率为_____________ 。

已知:1.次氯酸叔丁酯((CH3)3COCl),相对分子质量为108.5,是具有挥发性的黄色油状液体,密度为0.802g/mL,且有强烈刺激性臭味;2.(CH3)3COCl+LiOH=LiClO+(CH3)3COH
请回答:
(1)实验第一步的反应装置如图所示(夹持装置省略),B装置中支管的作用是

(2)请写出在装置A中发生反应的化学方程式
(3)对于操作1,下列说法不正确的是
A.可以选用250mL规格的分液漏斗
B.操作1须在通风橱内进行
C.进行分液时,可提早关闭旋塞,以防止次氯酸叔丁酯从下口流出
D.装置B不合适进行操作1
(4)进行操作3时,并不是直接加热蒸发溶液,而是选择在40°C下缓慢蒸发溶液,试解释其原因
(5)该实验中次氯酸锂的产率为
更新时间:2017-09-27 14:51:14
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下反应制得:
C6H12O6(葡萄糖)+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑
相关物质的溶解性见下表:
实验流程如下:
C6H12O6(aq)


 悬浊液
悬浊液
 (C6H11O7)2Ca
(C6H11O7)2Ca
请回答下列问题:
(1)第①步中溴水氧化葡萄糖时,下列装置最适合的是__ 。
A.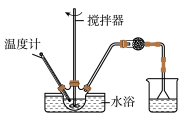
B.
C.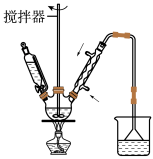
(2)制备葡萄糖酸钙的过程中,葡萄糖氧化也可用其它试剂,下列物质中最适合的是__ 。
A.新制氢氧化铜悬浊液
B.酸性高锰酸钾溶液
C.氧气/葡萄糖氧化酶
D.银氨溶液
(3)第②步充分反应后碳酸钙固体需有剩余,其目的是__ 。
(4)第②步实验中不用氯化钙替代碳酸钙的理由是__ 。
(5)第③步需趁热过滤的原因是__ 。
(6)第④步加入乙醇的作用是__ 。
(7)第⑥步中,下列洗涤剂最合适的是__ 。
A.冷水 B.热水
C.乙醇 D.乙醇-水混合溶液
C6H12O6(葡萄糖)+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑
相关物质的溶解性见下表:
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
C6H12O6(aq)



 悬浊液
悬浊液
 (C6H11O7)2Ca
(C6H11O7)2Ca请回答下列问题:
(1)第①步中溴水氧化葡萄糖时,下列装置最适合的是
A.

B.

C.

(2)制备葡萄糖酸钙的过程中,葡萄糖氧化也可用其它试剂,下列物质中最适合的是
A.新制氢氧化铜悬浊液
B.酸性高锰酸钾溶液
C.氧气/葡萄糖氧化酶
D.银氨溶液
(3)第②步充分反应后碳酸钙固体需有剩余,其目的是
(4)第②步实验中不用氯化钙替代碳酸钙的理由是
(5)第③步需趁热过滤的原因是
(6)第④步加入乙醇的作用是
(7)第⑥步中,下列洗涤剂最合适的是
A.冷水 B.热水
C.乙醇 D.乙醇-水混合溶液
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】硫酰氯(SO2Cl2)可用作有机化学的氯化剂,在药物和染料的制取中也有重要作用。某化学学习小组拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯。反应的化学方程式为:SO2(g)+ Cl2(g) =SO2Cl2(l) ΔH =−97.3 kJ·mol−1,实验装置如图所示(部分夹持装置未画出)。
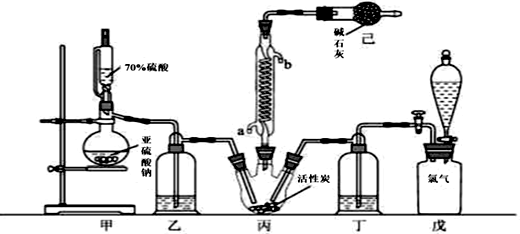
已知:硫酰氯通常条件下为无色液体,熔点−54.1℃,沸点69.1℃。在潮湿空气中“发烟”;100°C以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。
回答下列问题:
(1)装置甲中作为反应容器的仪器的名称为________ ,装置己的作用是________ ;如何控制两种反应物体积相等:________ 。
(2)装置戊上方分液漏斗中最好选用下列试剂:( ) (选填字母)。
A.蒸馏水 B.饱和食盐水 C.浓氢氧化钠溶液 D.6.0 mol·L−1盐酸
(3)若缺少装置乙和丁(均盛放浓硫酸),潮湿氯气和二氧化硫发生反应的化学方程式是________________________________________ 。
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯:2ClSO3H =SO2Cl2 + H2SO4,分离两种产物的方法是( ) (选填字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
(5)长期储存的硫酰氯会发黄,可能的原因是________ (用化学方程式和必要的文字加以解释)。
(6)若反应中消耗的氯气体积为896 mL(标准状况下),最后经过分离提纯得到4.05 g纯净的硫酰氯,则硫酰氯的产率为________ 。为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有________________ ________________________________________ (写两条即可)。

已知:硫酰氯通常条件下为无色液体,熔点−54.1℃,沸点69.1℃。在潮湿空气中“发烟”;100°C以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。
回答下列问题:
(1)装置甲中作为反应容器的仪器的名称为
(2)装置戊上方分液漏斗中最好选用下列试剂:
A.蒸馏水 B.饱和食盐水 C.浓氢氧化钠溶液 D.6.0 mol·L−1盐酸
(3)若缺少装置乙和丁(均盛放浓硫酸),潮湿氯气和二氧化硫发生反应的化学方程式是
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯:2ClSO3H =SO2Cl2 + H2SO4,分离两种产物的方法是
A.重结晶 B.过滤 C.蒸馏 D.萃取
(5)长期储存的硫酰氯会发黄,可能的原因是
(6)若反应中消耗的氯气体积为896 mL(标准状况下),最后经过分离提纯得到4.05 g纯净的硫酰氯,则硫酰氯的产率为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】我国科学家屠呦呦因青蒿素研究获得诺贝尔奖,青蒿素是从传统药材中发现的能治疗疟疾的有机化合物。现某实验小组拟提取青蒿素。
青蒿素为无色针状晶体,熔点为156~157°C,易溶于丙酮、氯仿和乙醚,在水中几乎不溶。
I.实验室流程如图所示:

(1)在操作I前要对青蒿进行粉碎,其目的是_______ ,操作II的名称是_______ 。
(2)操作III进行的是重结晶,其操作步骤为加热溶解→_______ →_______ →过滤、洗涤、干燥。
II.已知青蒿素是一种仅含有C、H、O三种元素的化合物,为进一步确定其化学式,进行了如图实验:

实验步骤:
①连接装置,检查装置气密性;
②称量E、F中仪器及药品的质量;
③取14. 10g青蒿素放入C的硬质玻璃管中,点燃C、D中的酒精灯加热,充分反应;
④实验结束后冷却至室温,称量反应后E、F中仪器及药品的质量。
(3)装置E、F应分别装入的药品为_______ 、_______ 。
(4)实验测得:
通过质谱法测得青蒿素的相对分子质量为282,结合上述数据,得出青蒿素的分子式为_______ 。
(5)若使用上述方法会产生较大实验误差,你的改进方法是_______ 。
青蒿素为无色针状晶体,熔点为156~157°C,易溶于丙酮、氯仿和乙醚,在水中几乎不溶。
I.实验室流程如图所示:

(1)在操作I前要对青蒿进行粉碎,其目的是
(2)操作III进行的是重结晶,其操作步骤为加热溶解→
II.已知青蒿素是一种仅含有C、H、O三种元素的化合物,为进一步确定其化学式,进行了如图实验:

实验步骤:
①连接装置,检查装置气密性;
②称量E、F中仪器及药品的质量;
③取14. 10g青蒿素放入C的硬质玻璃管中,点燃C、D中的酒精灯加热,充分反应;
④实验结束后冷却至室温,称量反应后E、F中仪器及药品的质量。
(3)装置E、F应分别装入的药品为
(4)实验测得:
| 装置 | 实验前 | 实验后 |
| E | 54.00g | 63.90g |
| F | 80.00g | 113.00g |
(5)若使用上述方法会产生较大实验误差,你的改进方法是
您最近半年使用:0次



