硫酰氯(SO2Cl2)可用作有机化学的氯化剂,在药物和染料的制取中也有重要作用。某化学学习小组拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯。反应的化学方程式为:SO2(g)+ Cl2(g) =SO2Cl2(l) ΔH =−97.3 kJ·mol−1,实验装置如图所示(部分夹持装置未画出)。
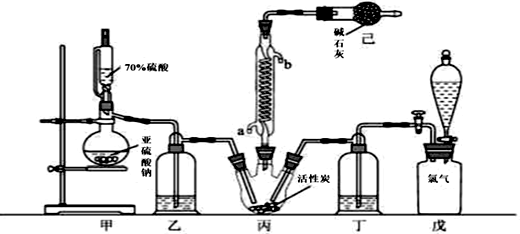
已知:硫酰氯通常条件下为无色液体,熔点−54.1℃,沸点69.1℃。在潮湿空气中“发烟”;100°C以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。
回答下列问题:
(1)装置甲中作为反应容器的仪器的名称为________ ,装置己的作用是________ ;如何控制两种反应物体积相等:________ 。
(2)装置戊上方分液漏斗中最好选用下列试剂:( ) (选填字母)。
A.蒸馏水 B.饱和食盐水 C.浓氢氧化钠溶液 D.6.0 mol·L−1盐酸
(3)若缺少装置乙和丁(均盛放浓硫酸),潮湿氯气和二氧化硫发生反应的化学方程式是________________________________________ 。
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯:2ClSO3H =SO2Cl2 + H2SO4,分离两种产物的方法是( ) (选填字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
(5)长期储存的硫酰氯会发黄,可能的原因是________ (用化学方程式和必要的文字加以解释)。
(6)若反应中消耗的氯气体积为896 mL(标准状况下),最后经过分离提纯得到4.05 g纯净的硫酰氯,则硫酰氯的产率为________ 。为提高本实验中硫酰氯的产率,在实验操作中需要注意的事项有________________ ________________________________________ (写两条即可)。

已知:硫酰氯通常条件下为无色液体,熔点−54.1℃,沸点69.1℃。在潮湿空气中“发烟”;100°C以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。
回答下列问题:
(1)装置甲中作为反应容器的仪器的名称为
(2)装置戊上方分液漏斗中最好选用下列试剂:
A.蒸馏水 B.饱和食盐水 C.浓氢氧化钠溶液 D.6.0 mol·L−1盐酸
(3)若缺少装置乙和丁(均盛放浓硫酸),潮湿氯气和二氧化硫发生反应的化学方程式是
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯:2ClSO3H =SO2Cl2 + H2SO4,分离两种产物的方法是
A.重结晶 B.过滤 C.蒸馏 D.萃取
(5)长期储存的硫酰氯会发黄,可能的原因是
(6)若反应中消耗的氯气体积为896 mL(标准状况下),最后经过分离提纯得到4.05 g纯净的硫酰氯,则硫酰氯的产率为
更新时间:2018-02-26 09:36:27
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某研究性学习小组欲探究氯气的化学性质,设计如图所示的实验装置。
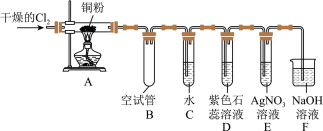
已知:该装置气密性良好,铜粉放在耐高温托盘内(托盘不与氯气反应,防止硬质玻璃管炸裂)。请回答下列问题:
(1)A中发生的化学反应方程式为___________ ;为防止铜与空气中的氧气反应,在加热之前应该进行的操作为___________ 。
(2)B装置中空试管的作用是___________ 。
(3)实验中,观察到D中颜色的变化为___________ 。
(4)当观察到E装置中 溶液中出现
溶液中出现___________ (填实验现象)时,点燃酒精灯加热;写出 溶液中发生反应的化学方程式:
溶液中发生反应的化学方程式:___________ 、___________ 。
(5)F中氢氧化钠溶液的作用是___________ ,发生反应的离子方程式为___________ 。

已知:该装置气密性良好,铜粉放在耐高温托盘内(托盘不与氯气反应,防止硬质玻璃管炸裂)。请回答下列问题:
(1)A中发生的化学反应方程式为
(2)B装置中空试管的作用是
(3)实验中,观察到D中颜色的变化为
(4)当观察到E装置中
 溶液中出现
溶液中出现 溶液中发生反应的化学方程式:
溶液中发生反应的化学方程式:(5)F中氢氧化钠溶液的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某同学用如图装置制备 并探究其性质。查阅资料知:
并探究其性质。查阅资料知:
i. 酸性条件下与
酸性条件下与 迅速反应生成S和
迅速反应生成S和
ii. 有较强的还原性
有较强的还原性
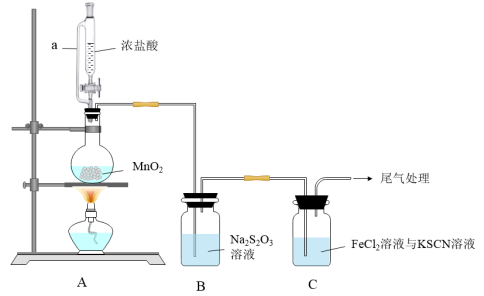
(1)装置A中a的作用是___________ ;装置A中制备 的离子方程式为
的离子方程式为___________ 。
(2)上述装置中存在一处缺陷,会干扰 和
和 性质的探究,改进的方法是
性质的探究,改进的方法是___________ 。
(3)改进实验装置后,B中 被氧化为
被氧化为 ,写出该反应的离子方程式
,写出该反应的离子方程式___________ 。
(4)装置C中溶液颜色先变为血红色,一段时间后褪色。
①生成使KSCN溶液变为血红色物质的离子方程式___________ ;
②某同学对褪色原因提出假设:
假设1: 被
被 氧化为更高价态;
氧化为更高价态;
假设2:___________ ;
为进一步探究,该同学取装置C褪色后的溶液少许于试管中,___________ (写出操作及现象)说明假设2成立。
 并探究其性质。查阅资料知:
并探究其性质。查阅资料知:i.
 酸性条件下与
酸性条件下与 迅速反应生成S和
迅速反应生成S和
ii.
 有较强的还原性
有较强的还原性
(1)装置A中a的作用是
 的离子方程式为
的离子方程式为(2)上述装置中存在一处缺陷,会干扰
 和
和 性质的探究,改进的方法是
性质的探究,改进的方法是(3)改进实验装置后,B中
 被氧化为
被氧化为 ,写出该反应的离子方程式
,写出该反应的离子方程式(4)装置C中溶液颜色先变为血红色,一段时间后褪色。
①生成使KSCN溶液变为血红色物质的离子方程式
②某同学对褪色原因提出假设:
假设1:
 被
被 氧化为更高价态;
氧化为更高价态;假设2:
为进一步探究,该同学取装置C褪色后的溶液少许于试管中,
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某校学生利用以下装置验证氯气与氨气之间的反应(部分装置已略去)。其中A、B分别为氯气和氨气的发生装置,C为纯净干燥的氯气与氨气反应的装置。



请回答下列问题:
(1)装置A中发生反应的离子方程式为_______________________ 。
(2)装置B中浓氨水与NaOH固体混合可制取氨气,其原因是__________________ 。
(3)装置C中氯气和氨气相遇,有浓厚的白烟并在容器内壁凝结,同时生成一种可参与生态循环的无毒气体,该反应的化学方程式为_____________________________________________
(4)将装置C中反应生成的固体溶于水,所得溶液中离子浓度由大到小的顺序为_________ 。



请回答下列问题:
(1)装置A中发生反应的离子方程式为
(2)装置B中浓氨水与NaOH固体混合可制取氨气,其原因是
(3)装置C中氯气和氨气相遇,有浓厚的白烟并在容器内壁凝结,同时生成一种可参与生态循环的无毒气体,该反应的化学方程式为
(4)将装置C中反应生成的固体溶于水,所得溶液中离子浓度由大到小的顺序为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某研究性学习小组的同学为在实验室再现二氧化硫催化氧化的过程,并制取少量三氧化硫晶体,设计了如图所示的装置。已知三氧化硫遇水生成硫酸并放出大量热,容易形成酸雾,工业上常用浓硫酸吸收三氧化硫。

试回答:
(1)已知6.4 g二氧化硫被氧气氧化成气态三氧化硫,放出9.83 kJ热量。反应的热化学方程式为____________________________________________________ ;
(2)A装置可用来观察二氧化硫和氧气的进气量。实验时使A中氧气导管冒出的气泡与二氧化硫导管冒出的气泡速率相近,其目的是___________________________ ;
(3)检查完装置的气密性且加入药品后,开始进行实验。此时首先应该进行的操作是________________________________ 。
(4)C装置用来收集三氧化硫,若用a g铜跟足量浓硫酸反应制二氧化硫,实验结束时得到b g三氧化硫,该实验中二氧化硫的转化率不小于_________________ ;
(5)为了减轻实验对环境的污染,请你设计尾气处理装置,绘出装置图:
___________________________________________________________________ 。

试回答:
(1)已知6.4 g二氧化硫被氧气氧化成气态三氧化硫,放出9.83 kJ热量。反应的热化学方程式为
(2)A装置可用来观察二氧化硫和氧气的进气量。实验时使A中氧气导管冒出的气泡与二氧化硫导管冒出的气泡速率相近,其目的是
(3)检查完装置的气密性且加入药品后,开始进行实验。此时首先应该进行的操作是
(4)C装置用来收集三氧化硫,若用a g铜跟足量浓硫酸反应制二氧化硫,实验结束时得到b g三氧化硫,该实验中二氧化硫的转化率不小于
(5)为了减轻实验对环境的污染,请你设计尾气处理装置,绘出装置图:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】硫酸在日常生产生活中应用非常广泛。请回答硫酸工业中的如下问题:
(1)早期生产硫酸以黄铁矿为原料,目前很多国家都已经限制以黄铁矿为原料而以硫黄为原料,以硫黄为原料的优点是______________ 。
(2)工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3,是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO27%;O211%;N282%);
利用表中数据分析。在实际生产中选择的适宜生产条件是:温度_______ ℃,压强 ___________ MPa。
(3)选择适宜的催化剂,是否可以提高SO2的转化率?_______ (填“是”或“否”),是否可以增大该反应所放出的热量?__________ (填“是” 或“否”)。
(4)为提高SO3吸收率,实际生产中用__________ 吸收SO3。
(5)在催化反应室中设有热交换装置,以下叙述与热交换装置的作用有关的是______ (填写序号)。
A.保护环境。防止空气污染 B.充分利用热量,降低生产成本
C.升高温度,提高SO2的转化率 D.防止催化剂中毒
(6)在硫酸工业尾气中,SO2是主要大气污染物,必须进行净化处理,处理方法可用________ (填名称)吸收,然后再用硫酸处理,重新生成SO2和一种生产水泥的辅料,写出这两步反应的化学方程式_______________________________________ 。
(1)早期生产硫酸以黄铁矿为原料,目前很多国家都已经限制以黄铁矿为原料而以硫黄为原料,以硫黄为原料的优点是
(2)工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3,是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO27%;O211%;N282%);
| 压强/Mpa 转化率/% 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
利用表中数据分析。在实际生产中选择的适宜生产条件是:温度
(3)选择适宜的催化剂,是否可以提高SO2的转化率?
(4)为提高SO3吸收率,实际生产中用
(5)在催化反应室中设有热交换装置,以下叙述与热交换装置的作用有关的是
A.保护环境。防止空气污染 B.充分利用热量,降低生产成本
C.升高温度,提高SO2的转化率 D.防止催化剂中毒
(6)在硫酸工业尾气中,SO2是主要大气污染物,必须进行净化处理,处理方法可用
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】为探究 、
、 、
、 氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验)。
氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验)。
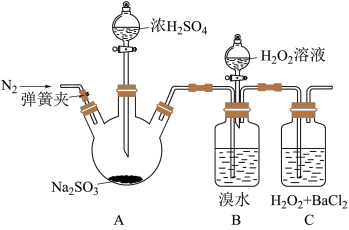
(1)A中发生反应的化学方程式是_______ 。B中红棕色褪色的化学方程式:_________ 。
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性: 。乙同学认为不能得出此结论,认为在滴加浓硫酸之前应增加一步操作,该操作是
。乙同学认为不能得出此结论,认为在滴加浓硫酸之前应增加一步操作,该操作是___________ 。
(3)iii中滴入少量 没有明显变化。提出假设:
没有明显变化。提出假设:
观点1: 的量少不能氧化
的量少不能氧化
观点2:B中有未反应的
为验证观点2,应进行的实验操作及现象是___________ 。
(4)通过上述全部实验,得出结论: 、
、 、
、 氧化性由强到弱的顺序是
氧化性由强到弱的顺序是___________ 。
 、
、 、
、 氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验)。
氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验)。
| 实验操作 | 实验现象 |
| i.打开A中分液漏斗活塞,滴加浓硫酸 | A中有气泡产生,B中红棕色溴水褪色,C中有白色沉淀 |
| ii.取C中沉淀加入盐酸 | C中白色沉淀不溶解 |
iii.打开B中分液漏斗活塞,逐滴滴加 | 开始时颜色无明显变化;继续滴加 溶液,一段时间后,混合液逐渐变成红棕色 溶液,一段时间后,混合液逐渐变成红棕色 |
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性:
 。乙同学认为不能得出此结论,认为在滴加浓硫酸之前应增加一步操作,该操作是
。乙同学认为不能得出此结论,认为在滴加浓硫酸之前应增加一步操作,该操作是(3)iii中滴入少量
 没有明显变化。提出假设:
没有明显变化。提出假设:观点1:
 的量少不能氧化
的量少不能氧化
观点2:B中有未反应的

为验证观点2,应进行的实验操作及现象是
(4)通过上述全部实验,得出结论:
 、
、 、
、 氧化性由强到弱的顺序是
氧化性由强到弱的顺序是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】从海产品中提取碘是我国工业上获取碘的重要途径,实验室证明海带中存在碘元素的方法如下:
Ⅰ.取3g左右的干海带,把干海带表面的附着物用刷子刷净,用剪刀剪碎后,用酒精润湿,灼烧至完全变成灰烬。
Ⅱ.将海带灰转移到小烧杯中,向其中加10mL蒸馏水,搅拌、煮沸2~3min,过滤。
Ⅲ.向滤液中加氧化剂氧化,最后检验碘单质的存在。
回答下列问题:
(1)“步骤1”中,灼烧时会用到下列仪器中的_______ (填标号)。
a. b.
b. c.
c. d.
d.
(2)某兴趣小组在实验室完成“步骤Ⅲ”中氧化剂氧化过程,装置如图所示。
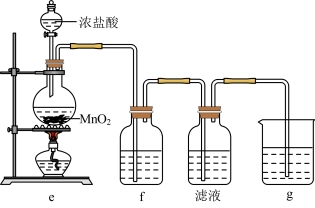
①装置e中发生反应的化学方程式是_______ 。
②装置f、g中所装的试剂分别是_______ 、_______ 。
③检验“滤液”中有碘单质生成的方法是_______ 。若通入 过量,检验发现“滤液”中无碘单质,其原因是
过量,检验发现“滤液”中无碘单质,其原因是_______ 。
(3)“步骤Ⅲ”氧化剂氧化时,用 在pH<2的酸性介质中反应效果最佳。已知还原产物是NO,则反应的离子方程式是
在pH<2的酸性介质中反应效果最佳。已知还原产物是NO,则反应的离子方程式是_______ 。
(4)若“步骤Ⅲ”所得溶液经过分离提纯获得 ,其物质的量是
,其物质的量是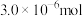 。则干海带中碘元素的含量是
。则干海带中碘元素的含量是_______ mg/kg。
Ⅰ.取3g左右的干海带,把干海带表面的附着物用刷子刷净,用剪刀剪碎后,用酒精润湿,灼烧至完全变成灰烬。
Ⅱ.将海带灰转移到小烧杯中,向其中加10mL蒸馏水,搅拌、煮沸2~3min,过滤。
Ⅲ.向滤液中加氧化剂氧化,最后检验碘单质的存在。
回答下列问题:
(1)“步骤1”中,灼烧时会用到下列仪器中的
a.
 b.
b. c.
c. d.
d.
(2)某兴趣小组在实验室完成“步骤Ⅲ”中氧化剂氧化过程,装置如图所示。

①装置e中发生反应的化学方程式是
②装置f、g中所装的试剂分别是
③检验“滤液”中有碘单质生成的方法是
 过量,检验发现“滤液”中无碘单质,其原因是
过量,检验发现“滤液”中无碘单质,其原因是(3)“步骤Ⅲ”氧化剂氧化时,用
 在pH<2的酸性介质中反应效果最佳。已知还原产物是NO,则反应的离子方程式是
在pH<2的酸性介质中反应效果最佳。已知还原产物是NO,则反应的离子方程式是(4)若“步骤Ⅲ”所得溶液经过分离提纯获得
 ,其物质的量是
,其物质的量是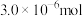 。则干海带中碘元素的含量是
。则干海带中碘元素的含量是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】ClO2与Cl2的氧化性相近。在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。


(1)仪器D的名称是_______ 。安装F中导管时,应选用图2中的_______ 。
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜_______ (填“快”或“慢”)。
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是_______ 。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为_______ ,在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是_______ 。
(5)已吸收ClO2气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如图3所示,若将其用于水果保鲜,你认为效果较好的稳定剂是_______ ,原因略



(1)仪器D的名称是
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为
(5)已吸收ClO2气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如图3所示,若将其用于水果保鲜,你认为效果较好的稳定剂是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学兴趣小组为了探究NH3的某些性质设计了如下实验:

(1)A装置试管中发生反应的化学方程式是___________ 。
(2)B装置的作用是___________ ,其中所装固体X应选用___________ 。
(3)实验过程中观察到装置C中黑色粉末逐渐变为红色,D中白色固体变蓝,说明C中反应的生成物有___________ ;E中集气瓶内收集到的气体无色无味,能使燃着的木条熄灭。综合分析,氨气与氧化铜反应的化学方程式为___________ 。

(1)A装置试管中发生反应的化学方程式是
(2)B装置的作用是
(3)实验过程中观察到装置C中黑色粉末逐渐变为红色,D中白色固体变蓝,说明C中反应的生成物有
您最近一年使用:0次



