常温下,发生下列几种反应:
①16H++10Z-+2XO4-===2X2++5Z2+8H2O
②2A2++B2===2A3++2B-
③2B-+Z2===B2+2Z-
根据上述反应,判断下列结论错误的是
①16H++10Z-+2XO4-===2X2++5Z2+8H2O
②2A2++B2===2A3++2B-
③2B-+Z2===B2+2Z-
根据上述反应,判断下列结论错误的是
| A.溶液中可发生:Z2+2A2+===2A3++2Z- | B.氧化性强弱的顺序为XO4->Z2>B2>A3+ |
| C.Z2在①③反应中为氧化剂 | D.反应③中B2是2B-的氧化产物 |
更新时间:2017-12-07 15:24:06
|
【知识点】 氧化性、还原性强弱的比较解读
相似题推荐
【推荐1】根据表中信息判断,下列选项不正确 的是
序号 | 反应物 | 产物 |
① | KMnO4 、H2O2 、H2SO4 | K2SO4 、MnSO4 ...... |
② | Cl2 、FeBr2 | FeCl3 、FeBr3 |
③ | MnO4- Cl- ...... | Cl2 、Mn2+ ...... |
| A.氧化性由强到弱顺序为MnO4- > Cl2 > Fe3+ > Br2 |
| B.第②组反应从产物结果可以得出还原性顺序:Fe2+ > Br- |
| C.第③组反应中生成1mol Cl2,转移电子数为2NA |
| D.第①组反应的其余产物为H2O和 O2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】已知,还原性 >Cl﹣,氧化性
>Cl﹣,氧化性 >Cl2。
>Cl2。
实验Ⅰ:在一定量NaHSO3的溶液中逐滴加入KClO3溶液至过量;
实验Ⅱ:在一定量的KClO3溶液中逐滴加入NaHSO3溶液至过量;
下列说法不正确的是
 >Cl﹣,氧化性
>Cl﹣,氧化性 >Cl2。
>Cl2。实验Ⅰ:在一定量NaHSO3的溶液中逐滴加入KClO3溶液至过量;
实验Ⅱ:在一定量的KClO3溶液中逐滴加入NaHSO3溶液至过量;
下列说法不正确的是
| A.两实验中溶液的pH变化趋势不相同 |
| B.试验Ⅱ反应结束后,加入淀粉碘化钾溶液,溶液不会变蓝 |
| C.两实验中生成等物质的量Cl2时,消耗的NaHSO3物质的量一定相等 |
| D.在实验Ⅱ的过程中,若KClO3初始量为4mol,当溶液中Cl2与Cl﹣的物质的量之比为5:6时,氧化产物为10.75mol |
您最近一年使用:0次

 、
、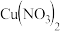 、
、 ,向其中逐渐加入铁粉,溶液中
,向其中逐渐加入铁粉,溶液中 的浓度
的浓度 纵坐标
纵坐标 和加入铁粉的物质的量
和加入铁粉的物质的量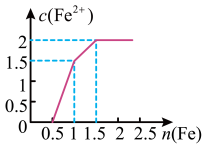
 无色气体
无色气体

