以下事实不能用元素周期律解释的是
| A.F2在暗处遇H2即爆炸,I2在暗处遇H2几乎不反应 |
| B.“NO2球”在冷水中颜色变浅,在热水中颜色加深 |
| C.氯原子与钠原子形成离子键,与硅原子形成共价键 |
| D.H2O在4000℃以上开始明显分解,H2S用酒精灯加热即可完全分解 |
2017·四川德阳·一模 查看更多[4]
陕西省西安市蓝田县2022-2023学年高二下学期6月期末考试化学试题(已下线)第14讲 元素周期律和元素周期表(练)-2023年高考化学一轮复习讲练测(新教材新高考)北京市昌平区2018届高三化学12月月考试题四川省德阳市三校2018届高三联合测试化学试题
更新时间:2017-12-06 17:55:23
|
【知识点】 金属与非金属在周期表中位置及其性质递变的规律
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】比较C、S元素的非金属性强弱方法错误的是
| A.酸性:H2SO4>H2CO3 |
| B.在高温下,碳能将BaSO4还原成BaS |
| C.化合物CS2中S元素显负二价 |
| D.S和H2加热条件下可以化合生成H2S,而C和H2高温条件下很难化合成CH4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】元素周期表和元素周期律可指导人们进行规律性推测和判断。下列说法中不合理的是
| A.若aX2+ 和bY- 的核外电子层结构相同,则原子序数:a=b+3 |
| B.盐酸(HCl)酸性比H2SiO3强,则元素的非金属性:Cl>Si |
| C.硅、锗都位于金属与非金属的交界处,都可用作半导体材料 |
D.Be与Al在周期表中处于对角线位置,可推出:Be(OH)2+2OH-=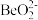 +2H2O +2H2O |
您最近一年使用:0次



