废水脱氮工艺中有一种方法是在废水中加入过量NaClO使NH4+完全转化为N2,该反应可表示为2NH4++3ClO-=N2↑+3Cl-+2H++3H2O。下列说法中,不正确的是
| A.反应中氮元素被氧化,氯元素被还原 |
| B.还原性NH4+< Cl- |
| C.反应中每生成1 mol N2,转移6 mol电子 |
| D.经此法处理过的废水不可以直接排放 |
17-18高一上·北京·期中 查看更多[3]
更新时间:2017-12-27 15:15:50
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列反应属于氧化还原反应,且水既不作氧化剂又不作还原剂的是
| A.2F2+2H2O=4HF+O2 |
| B.2Na2O2+2H2O=4NaOH+O2↑ |
| C.2H2O+2Na=2NaOH+H2↑ |
D.2H2O O2↑+2H2↑ O2↑+2H2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某废水中含有一定量的Na+、 ,可能含有
,可能含有 ,某研究小组欲测定其中
,某研究小组欲测定其中 的浓度,设计如图所示的实验方案:
的浓度,设计如图所示的实验方案:

则试剂X可以是( )
 ,可能含有
,可能含有 ,某研究小组欲测定其中
,某研究小组欲测定其中 的浓度,设计如图所示的实验方案:
的浓度,设计如图所示的实验方案:
则试剂X可以是( )
| A.0.1mol·L-1KMnO4(H2SO4酸化)溶液 |
| B.0.5mol·L-1NaOH溶液 |
| C.新制氯水 |
| D.KI溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列离子方程式书写正确的是
| A.乙酸溶液滴到大理石上产生气泡:2H++CaCO3=CO2↑+Ca2++H2O |
B.在偏铝酸钠溶液中通入少量二氧化碳:AlO +CO2+2H2O=Al(OH)3↓+HCO +CO2+2H2O=Al(OH)3↓+HCO |
| C.向含有FeBr2溶液中通入等物质的量的Cl2:2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl- |
D.用石墨作阴极、铁作阳极电解食盐水:2Cl-+2H2O 2OH-+Cl2↑+H2↑ 2OH-+Cl2↑+H2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验操作、现象和结论或解释均正确的是
| 选项 | 实验操作 | 现象 | 结论或解释 |
| A | 把 通入 通入 溶液中,然后滴加氯水 溶液中,然后滴加氯水 | 先有白色沉淀产生,滴加氯水后沉淀不溶解 | 先生成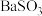 沉淀后被氧化为 沉淀后被氧化为 |
| B | 向 溶液和盐酸反应后的溶液中加入紫色石蕊试液 溶液和盐酸反应后的溶液中加入紫色石蕊试液 | 溶液变红 | 说明盐酸已经过量 |
| C | 向 溶液中通入足量的 溶液中通入足量的 | 生成两种沉淀 |  的氧化性强于S 的氧化性强于S |
| D | 向浓度均为 的 的 和 和 混合溶液中滴加少量 混合溶液中滴加少量 溶液 溶液 | 出现黄色沉淀 | 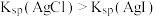 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】硝酸铵受热分解的化学方程式为5NH4NO3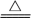 2HNO3+4N2↑+9H2O,则下列关于硝酸铵受热分解的说法不正确的是 ( )
2HNO3+4N2↑+9H2O,则下列关于硝酸铵受热分解的说法不正确的是 ( )
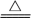 2HNO3+4N2↑+9H2O,则下列关于硝酸铵受热分解的说法不正确的是 ( )
2HNO3+4N2↑+9H2O,则下列关于硝酸铵受热分解的说法不正确的是 ( )| A.该反应属于氧化还原反应 |
| B.该反应中只有一种元素的化合价发生变化 |
| C.硝酸铵既是氧化剂又是还原剂 |
| D.氧化产物和还原产物的物质的量之比为3:5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】测定0.1 mol/LNa2SO3溶液先升温再降温过程中的pH数据如下
实验过程中,取①④时刻的溶液,加入盐酸酸化的BaCl2溶液做对比实验,④产生白色沉淀多。下列说法不正确的是
| 时刻 | ① | ② | ③ | ④ |
| 温度/℃ | 25 | 30 | 40 | 25 |
| pH | 9.66 | 9.52 | 9.37 | 9.25 |
A.Na2SO3溶液中存在水解平衡: +H2O⇌ +H2O⇌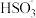 +OH- +OH- |
B.④的pH与①不同,其 浓度也小于① 浓度也小于① |
| C.①→③的过程中,温度和浓度对水解平衡移动方向的影响一致 |
| D.①与④的K值相等 |
您最近一年使用:0次




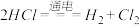
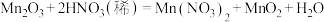
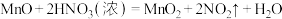
 相比,
相比, 与浓盐酸反应制取氯气的条件更容易
与浓盐酸反应制取氯气的条件更容易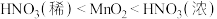

 看作
看作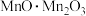 ,可发生反应:
,可发生反应: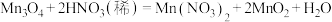
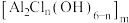 具有吸附性,可用作净水剂
具有吸附性,可用作净水剂

