(1)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水.当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出256.8kJ的热量(相当于25℃、101kPa下测得的热量).
①反应的热化学方程式为________________________________ .
②又已知H2O(l)=H2O(g)△H=+44kJ/mol.则16g液态肼与液态双氧水反应生成液态水时放出的热量是________________ kJ.
③此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是_________________________________________________ .
(2)已知热化学方程式:①Fe2O3(s)+3CO(g)==2Fe(s)+3CO2(g)ΔH=-25 kJ·mol-1
②3Fe2O3(s)+CO(g)==2Fe3O4(s)+CO2(g) ΔH=-47 kJ·mol-1
③Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) ΔH=19 kJ·mol-1
写出FeO(s)被CO还原生成Fe和CO2的热化学方程式:__________________________________________________________ 。
(3)已知反应2HI(g)=H2(g) + I2(g)的△H=+11kJ·mol-1,1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436KJ、151KJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为______________ kJ。
①反应的热化学方程式为
②又已知H2O(l)=H2O(g)△H=+44kJ/mol.则16g液态肼与液态双氧水反应生成液态水时放出的热量是
③此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
(2)已知热化学方程式:①Fe2O3(s)+3CO(g)==2Fe(s)+3CO2(g)ΔH=-25 kJ·mol-1
②3Fe2O3(s)+CO(g)==2Fe3O4(s)+CO2(g) ΔH=-47 kJ·mol-1
③Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) ΔH=19 kJ·mol-1
写出FeO(s)被CO还原生成Fe和CO2的热化学方程式:
(3)已知反应2HI(g)=H2(g) + I2(g)的△H=+11kJ·mol-1,1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436KJ、151KJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为
更新时间:2018-01-06 10:40:48
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】能源的合理利用和开发是当今社会人类面临的严峻课题。回答问题:
(1)我国是世界上少数以煤为主要燃料的国家,下列关于煤作燃料的论点不正确的是_____________ (填字母)。
A.煤是重要的化工原料,把煤作燃料简单燃烧掉太可惜,应该综合利用
B.煤是发热很高的固体燃料,我国煤炭资源相对集中,开采成本低,用煤作燃料实惠
C.煤燃烧时产生大量二氧化硫和烟尘,对环境污染严重
(2)把煤作为燃料可以通过下列两种途径:
途径Ⅰ: (放热
(放热 J)
J)
途径Ⅱ:先制水煤气: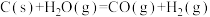 (吸热
(吸热 J)
J)
再燃烧水煤气: 共放热(
共放热(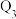 J)
J)
①途径Ⅰ放出的热量________ (填“大于”、“等于”或“小于”)途径Ⅱ放出的热量。
② 、
、 、
、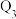 的数学关系式是
的数学关系式是________ 。
(3)科学家将铜和铁混合熔化制成多孔金属,用于制作太空火箭上使用的煤油燃料雾化器,该雾化器的作用是________ 。
(4)乙醇是未来内燃机的首选环保型液体燃料。2.0g乙醇完全燃烧生成液态水放出59.43kJ热量,表示乙醇燃烧热的热化学方程式为________ 。
(1)我国是世界上少数以煤为主要燃料的国家,下列关于煤作燃料的论点不正确的是
A.煤是重要的化工原料,把煤作燃料简单燃烧掉太可惜,应该综合利用
B.煤是发热很高的固体燃料,我国煤炭资源相对集中,开采成本低,用煤作燃料实惠
C.煤燃烧时产生大量二氧化硫和烟尘,对环境污染严重
(2)把煤作为燃料可以通过下列两种途径:
途径Ⅰ:
 (放热
(放热 J)
J)途径Ⅱ:先制水煤气:
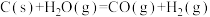 (吸热
(吸热 J)
J)再燃烧水煤气:
 共放热(
共放热( J)
J)①途径Ⅰ放出的热量
②
 、
、 、
、 的数学关系式是
的数学关系式是(3)科学家将铜和铁混合熔化制成多孔金属,用于制作太空火箭上使用的煤油燃料雾化器,该雾化器的作用是
(4)乙醇是未来内燃机的首选环保型液体燃料。2.0g乙醇完全燃烧生成液态水放出59.43kJ热量,表示乙醇燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】烟气(主要污染物SO2、NO、NO2)的大量排放造成严重的大气污染,国内较新研究成果是采用以尿素为还原剂的脱硫脱硝一体化技术。
(1)脱硫总反应:SO2(g)+CO(NH2)2(aq)+2H2O(l)+1/2O2(g)=(NH2)SO4(aq)+CO2(g),已知该反应能自发进行,则条件是____ (填“高温”、“低温”或“任何温度”)。
(2)电解稀硫酸制备O3(原理如图),则产生O3的电极反应式为______ 。
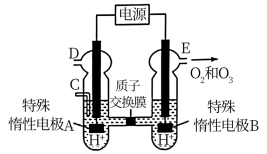

(3)室温下,往恒容的反应器中加入固定物质的量的SO2和NO,通入O3充分混合。反应相同时间后,各组分的物质的量随n(O3)∶n(NO)的变化见上图。
① n(NO2)随n(O3)∶n(NO)的变化先增加后减少,原因是____ 。
② 臭氧量对反应SO2(g)+O3(g)=SO3(g)+O2(g)的影响不大,试用过渡态理论解释可能原因__ 。
(4)通过控制变量法研究脱除效率的影响因素得到数据如下图所示,下列说法正确的是____ 。
A. 烟气在尿素溶液中的反应:v(脱硫)<v(脱硝)
B. 尿素溶液pH的变化对脱硝效率的影响大于对脱硫效率的影响
C. 强酸性条件下不利于尿素对氮氧化物的脱除
D. pH=7的尿素溶液脱硫效果最佳

(5)尿素的制备:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) ΔH<0。一定条件下,往10 L恒容密闭容器中充入2 mol NH3和1 mol CO2。
CO(NH2)2(s)+H2O(g) ΔH<0。一定条件下,往10 L恒容密闭容器中充入2 mol NH3和1 mol CO2。
① 该反应10 min 后达到平衡,测得容器中气体密度为4.8 g·L-1,平衡常数K=__ 。
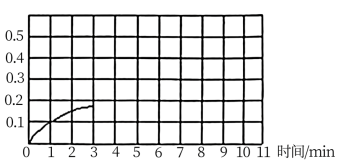
② 上图是该条件下,系统中尿素的物质的量随反应时间的变化趋势,当反应时间达到3min 时,迅速将体系升温,请在图中画出3~10 min 内容器中尿素的物质的量的变化趋势曲线__________ 。
(1)脱硫总反应:SO2(g)+CO(NH2)2(aq)+2H2O(l)+1/2O2(g)=(NH2)SO4(aq)+CO2(g),已知该反应能自发进行,则条件是
(2)电解稀硫酸制备O3(原理如图),则产生O3的电极反应式为


(3)室温下,往恒容的反应器中加入固定物质的量的SO2和NO,通入O3充分混合。反应相同时间后,各组分的物质的量随n(O3)∶n(NO)的变化见上图。
① n(NO2)随n(O3)∶n(NO)的变化先增加后减少,原因是
② 臭氧量对反应SO2(g)+O3(g)=SO3(g)+O2(g)的影响不大,试用过渡态理论解释可能原因
(4)通过控制变量法研究脱除效率的影响因素得到数据如下图所示,下列说法正确的是
A. 烟气在尿素溶液中的反应:v(脱硫)<v(脱硝)
B. 尿素溶液pH的变化对脱硝效率的影响大于对脱硫效率的影响
C. 强酸性条件下不利于尿素对氮氧化物的脱除
D. pH=7的尿素溶液脱硫效果最佳

(5)尿素的制备:2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g) ΔH<0。一定条件下,往10 L恒容密闭容器中充入2 mol NH3和1 mol CO2。
CO(NH2)2(s)+H2O(g) ΔH<0。一定条件下,往10 L恒容密闭容器中充入2 mol NH3和1 mol CO2。① 该反应10 min 后达到平衡,测得容器中气体密度为4.8 g·L-1,平衡常数K=

② 上图是该条件下,系统中尿素的物质的量随反应时间的变化趋势,当反应时间达到3min 时,迅速将体系升温,请在图中画出3~10 min 内容器中尿素的物质的量的变化趋势曲线
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下列各图均能表示甲烷的分子结构,按要求回答下列问题。

(1)甲烷的比例模型是______ (填序号)。
(2)相对分子质量为100的烷烃的分子式是_____ 。
(3)立方烷 的一氯代物有
的一氯代物有_________ 种,它的六氯代物有_________ 种。
(4)下列物质的沸点按由高到低的顺序排列正确的是___________ 。
①CH3(CH2)2CH3 ②CH3(CH2)3CH3 ③(CH3)3CH ④(CH3)2CHCH2CH3
A.②④①③ B.④②①③ C.④③②① D.②④③①
(5)已知拆开1mol H-H键,1molO-H(g)键,1molO=O键分别需要的能量是436kJ、463kJ、496kJ,则O2与H2反应生成2molH2O(g)所释放的热量为___________ kJ 。

(1)甲烷的比例模型是
(2)相对分子质量为100的烷烃的分子式是
(3)立方烷
 的一氯代物有
的一氯代物有(4)下列物质的沸点按由高到低的顺序排列正确的是
①CH3(CH2)2CH3 ②CH3(CH2)3CH3 ③(CH3)3CH ④(CH3)2CHCH2CH3
A.②④①③ B.④②①③ C.④③②① D.②④③①
(5)已知拆开1mol H-H键,1molO-H(g)键,1molO=O键分别需要的能量是436kJ、463kJ、496kJ,则O2与H2反应生成2molH2O(g)所释放的热量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】化学反应过程中发生物质变化的同时,常常伴有能量的变化.这种能量的变化常以热量的形式表现出来,叫做反应热.由于反应的情况不同,反应热可以分为许多种,如燃烧热和中和热等。
(1)下列△H表示物质燃烧热的是_______ ;表示物质中和热的是_______ (填“△H1”、“△H2”、“△H3”等).
A.2H2(g)+O2(g)═2H2O(l)△H1
B.C(s)+1/2O2(g)═CO(g)△H2
C.CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H3
D.C(s)+O2(g)═CO2(g)△H4
E.C6H12O6(s)+6O2(g)═6CO2(g)+6H2O(l)△H5
F. NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H6
G.2NaOH(aq)+H2SO4(aq)═Na2SO4(aq)+2H2O(l)△H7
H.CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H8
(2)依据事实,写出下列反应的热化学方程式.
Ⅰ、在25℃、101kPa下,1gCH3OH燃烧生成CO2和液态水时放热22.68kJ.则表示甲醇燃烧热的热化学方程式为_______________________ ;
Ⅱ、1.00L 1.00mol/L H2SO4溶液与2.00L 1.00mol/L NaOH溶液完全反应,放出114.6kJ的热量,表示其中和热的热化学方程式为________________________ ;
Ⅲ、已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、 946kJ,则N2与H2反应生成NH3的热化学方程式为_______________________ 。
(1)下列△H表示物质燃烧热的是
A.2H2(g)+O2(g)═2H2O(l)△H1
B.C(s)+1/2O2(g)═CO(g)△H2
C.CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H3
D.C(s)+O2(g)═CO2(g)△H4
E.C6H12O6(s)+6O2(g)═6CO2(g)+6H2O(l)△H5
F. NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H6
G.2NaOH(aq)+H2SO4(aq)═Na2SO4(aq)+2H2O(l)△H7
H.CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H8
(2)依据事实,写出下列反应的热化学方程式.
Ⅰ、在25℃、101kPa下,1gCH3OH燃烧生成CO2和液态水时放热22.68kJ.则表示甲醇燃烧热的热化学方程式为
Ⅱ、1.00L 1.00mol/L H2SO4溶液与2.00L 1.00mol/L NaOH溶液完全反应,放出114.6kJ的热量,表示其中和热的热化学方程式为
Ⅲ、已知拆开1molH-H键,1molN-H键,1molN≡N键分别需要的能量是436kJ、391kJ、 946kJ,则N2与H2反应生成NH3的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】按要求完成下列各空。
(1)已知数据如图,写出工业合成氨的热化学方程式:___________ 。

(2)0.5 mol甲烷与一定量水蒸气在一定条件下,完全反应生成一氧化碳和氢气,吸热a kJ,则反应物总能量___________ (填“ ”、“
”、“ ”或“=”)生成物总能量。
”或“=”)生成物总能量。
(3)使Cl2和H2O(g)通过灼热炭层,生成气态HCl和CO2,当反应中转移1mol电子时释放145kJ热量。当有1molCO2生成时,ΔH =___________ kJ/mol。
(4)反应mA(g)+nB(g) = pC(g) +qD(g)过程中的能量变化如图所示:

①该反应ΔH =___________ kJ/mol(用含E1、E2式子表示)。
②在反应体系中加入催化剂,ΔH___________ (填“增大”、“减小”、“不变”)。
(1)已知数据如图,写出工业合成氨的热化学方程式:

(2)0.5 mol甲烷与一定量水蒸气在一定条件下,完全反应生成一氧化碳和氢气,吸热a kJ,则反应物总能量
 ”、“
”、“ ”或“=”)生成物总能量。
”或“=”)生成物总能量。(3)使Cl2和H2O(g)通过灼热炭层,生成气态HCl和CO2,当反应中转移1mol电子时释放145kJ热量。当有1molCO2生成时,ΔH =
(4)反应mA(g)+nB(g) = pC(g) +qD(g)过程中的能量变化如图所示:

①该反应ΔH =
②在反应体系中加入催化剂,ΔH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氢是宇宙中含量最高的元素,占宇宙总质量的75%,应用前景十分广阔。
(1)H可与N形成多种分子,其中某分子含18个e-、6个原子,则该分子的结构式为___________ 。
(2)工业上用C和H2O制取H2。已知:
①C(s) + H2O(g) = H2(g) + CO(g) ΔH1
②C(s) + 2H2O(g) = 2H2(g) + CO2(g) ΔH2
则CO(s) + H2O(g) = H2(g) + CO2(g) ΔH =___________ (用ΔH1、ΔH2表示)。
(3)NaBH4是一种重要的储氢载体。
①B在元素周期表中的位置为___________ 。
②NaBH4(s)与H2O (l)反应生成NaBO2(s)和一种气体,在25℃,101kPa下,已知每消耗3.8g NaBH4放热21.6kJ,则该反应的热化学方程式为___________ ;反应前后B的化合价不变,则反应消耗1molNaBH4时转移的电子数目为___________ 。
(1)H可与N形成多种分子,其中某分子含18个e-、6个原子,则该分子的结构式为
(2)工业上用C和H2O制取H2。已知:
①C(s) + H2O(g) = H2(g) + CO(g) ΔH1
②C(s) + 2H2O(g) = 2H2(g) + CO2(g) ΔH2
则CO(s) + H2O(g) = H2(g) + CO2(g) ΔH =
(3)NaBH4是一种重要的储氢载体。
①B在元素周期表中的位置为
②NaBH4(s)与H2O (l)反应生成NaBO2(s)和一种气体,在25℃,101kPa下,已知每消耗3.8g NaBH4放热21.6kJ,则该反应的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烧, 电解质是熔融碳酸盐,电池总反应方程式为:C3H8+5O2 = 3CO2+4H2O。
(1)已知:2C3H8(g) + 7O2(g) = 6CO(g) + 8H2O(l) △H1
C(s) + O2(g) = CO2(g) △H2
2C(s) + O2(g) = 2CO(g) △H3
则 C3H8(g)+5O2((g) = 3CO2(g) + 4H2O(l) △H=________ (用△H1、△H2、△H3表示)
(2)写出该电池正极的电极反应式:_________ ,电池工作时CO32-移向_________ (填“正极”或“负极”);用该电池电解1000 mL lmol/L的AgNO3溶液(惰性电极),此电解池的反应方程式为_____________________________________ 。
(1)已知:2C3H8(g) + 7O2(g) = 6CO(g) + 8H2O(l) △H1
C(s) + O2(g) = CO2(g) △H2
2C(s) + O2(g) = 2CO(g) △H3
则 C3H8(g)+5O2((g) = 3CO2(g) + 4H2O(l) △H=
(2)写出该电池正极的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】对含氮物质的研究和利用有着极为重要的意义。
(1)N2、O2和H2相互之间可以发生化合反应,已知反应的热化学方程式如下:
N2(g)+O2(g)=2NO(g) H= +180 kJ·mol-1;
H= +180 kJ·mol-1;
2H2(g)+O2(g)=2H2O(g) H =-483 kJ·mol-1;
H =-483 kJ·mol-1;
N2(g)+3H2(g)=2NH3(g) H = -93 kJ·mol-1。
H = -93 kJ·mol-1。
则氨的催化氧化反应的热化学方程式为___________________________________ 。
(2)汽车尾气净化的一个反应原理为:2NO(g)+2CO(g) N2(g)+2CO2(g) △H<0。一定温度下,将2.8mol NO、2.4mol CO通入固定容积为2L的密闭容器中,反应过程中部分物质的物质的量变化如右图所示。
N2(g)+2CO2(g) △H<0。一定温度下,将2.8mol NO、2.4mol CO通入固定容积为2L的密闭容器中,反应过程中部分物质的物质的量变化如右图所示。

①NO的平衡转化率为_________ ,0~20min平均反应速率v(NO)为_____________ mol/(L min);该温度下的化学平衡常数数值是
min);该温度下的化学平衡常数数值是_____________ 。25min时,若保持反应温度不变,再向容器中充入CO、N2各0.8 mol,则化学平衡将_________ 移动(填“向左”、“向右”或“不”)。
②下列可说明该反应已经达到平衡的是__________ 。
a. v生成(CO2)= v消耗(CO)
b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变
d.单位时间内消耗2n mol CO2的同时生成n mol N≡N
e.NO、CO、N2、CO2的浓度相等
③反应达到平衡后,改变某一个条件,下列示意图曲线①〜⑧中正确的是________

(1)N2、O2和H2相互之间可以发生化合反应,已知反应的热化学方程式如下:
N2(g)+O2(g)=2NO(g)
 H= +180 kJ·mol-1;
H= +180 kJ·mol-1;2H2(g)+O2(g)=2H2O(g)
 H =-483 kJ·mol-1;
H =-483 kJ·mol-1;N2(g)+3H2(g)=2NH3(g)
 H = -93 kJ·mol-1。
H = -93 kJ·mol-1。则氨的催化氧化反应的热化学方程式为
(2)汽车尾气净化的一个反应原理为:2NO(g)+2CO(g)
 N2(g)+2CO2(g) △H<0。一定温度下,将2.8mol NO、2.4mol CO通入固定容积为2L的密闭容器中,反应过程中部分物质的物质的量变化如右图所示。
N2(g)+2CO2(g) △H<0。一定温度下,将2.8mol NO、2.4mol CO通入固定容积为2L的密闭容器中,反应过程中部分物质的物质的量变化如右图所示。
①NO的平衡转化率为
 min);该温度下的化学平衡常数数值是
min);该温度下的化学平衡常数数值是②下列可说明该反应已经达到平衡的是
a. v生成(CO2)= v消耗(CO)
b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变
d.单位时间内消耗2n mol CO2的同时生成n mol N≡N
e.NO、CO、N2、CO2的浓度相等
③反应达到平衡后,改变某一个条件,下列示意图曲线①〜⑧中正确的是

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.写出下列反应的热化学方程式。
(1)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是___________ 。
(2)在1.01×105 Pa时,16 g S固体在足量的氧气中充分燃烧生成二氧化硫,放出148.5 kJ的热量,则S固体燃烧热的热化学方程式为_____________ 。 (S相对原子质量为32)
II.研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(3)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S固体。已知:
①CO(g)+ O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
②S(s)+O2(g)=SO2(g) ΔH=-296.0 kJ·mol-1
此反应的热化学方程式是___________ 。
(1)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是
(2)在1.01×105 Pa时,16 g S固体在足量的氧气中充分燃烧生成二氧化硫,放出148.5 kJ的热量,则S固体燃烧热的热化学方程式为
II.研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(3)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S固体。已知:
①CO(g)+
 O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1②S(s)+O2(g)=SO2(g) ΔH=-296.0 kJ·mol-1
此反应的热化学方程式是
您最近一年使用:0次



