掌握仪器的名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。
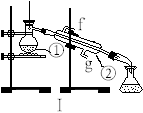
(1)写出下列仪器的名称:①__________ ;②_________ 。
(2)若利用装置I制取蒸馏水,将仪器补充完整后进行实验,冷却水从____________ 口进。(填g或f)
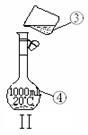
(3)现需配制250 mL 0.2 mol·L—1 NaCl溶液,其中装置II是某同学配制此溶液时转移操作的示意图,图中有两处错误,一处是未用玻璃棒引流,另一处是_________________ 。
(4)在配制过程中,其他操作都是正确的,下列情况对所配制的NaCl溶液的浓度偏低有______ 。
A.没有洗涤烧杯和玻璃棒 B.容量瓶不干燥,含有少量蒸馏水 C.定容时俯视刻度线 D.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线。


(1)写出下列仪器的名称:①
(2)若利用装置I制取蒸馏水,将仪器补充完整后进行实验,冷却水从
(3)现需配制250 mL 0.2 mol·L—1 NaCl溶液,其中装置II是某同学配制此溶液时转移操作的示意图,图中有两处错误,一处是未用玻璃棒引流,另一处是
(4)在配制过程中,其他操作都是正确的,下列情况对所配制的NaCl溶液的浓度偏低有
A.没有洗涤烧杯和玻璃棒 B.容量瓶不干燥,含有少量蒸馏水 C.定容时俯视刻度线 D.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线。
更新时间:2018-01-08 19:19:50
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室配制500mL0.5mol·L-1的NaCl溶液,有如下操作步骤:
①把称量的NaCl晶体放入小烧杯中,加适量蒸馏水溶解。
②把①所得溶液小心转入500mL容量瓶中。
③继续向容量瓶中加蒸馏水至液面距刻度1~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部与刻度线相切。
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀。⑤将容量瓶塞塞紧,充分摇匀。
请填写下列空白:
(1)操作步骤的正确顺序为_______ (填序号)。
(2)本实验用到的玻璃仪器有_______ 。
(3)某同学观察液面的情况如图所示,对所配溶液浓度将有何影响?_______ (填“偏高”、“偏低”或“无影响”)。

(4)若出现如下情况,对所配溶液浓度将有何影响:没有进行操作步骤④_______ ;加蒸馏水时不慎超过了刻度_______ 。(填“偏高”、“偏低”或“无影响”)
(5)若实验过程中出现如下情况应如何处理?向容量瓶中转移溶液时(操作步骤②)溶液流到容量瓶外面_______ 。
①把称量的NaCl晶体放入小烧杯中,加适量蒸馏水溶解。
②把①所得溶液小心转入500mL容量瓶中。
③继续向容量瓶中加蒸馏水至液面距刻度1~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部与刻度线相切。
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀。⑤将容量瓶塞塞紧,充分摇匀。
请填写下列空白:
(1)操作步骤的正确顺序为
(2)本实验用到的玻璃仪器有
(3)某同学观察液面的情况如图所示,对所配溶液浓度将有何影响?

(4)若出现如下情况,对所配溶液浓度将有何影响:没有进行操作步骤④
(5)若实验过程中出现如下情况应如何处理?向容量瓶中转移溶液时(操作步骤②)溶液流到容量瓶外面
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】无土栽培试验需要用到 营养液,现配制
营养液,现配制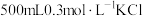 溶液。
溶液。
(1)根据计算,需用托盘天平称量 固体的质量为
固体的质量为___________ g。
(2)如图所示的仪器中,配制溶液肯定不需要的是___________ (填标号),容量瓶除刻度线外还标有以下四项中的___________ (填序号)。
①温度②浓度③容积④压强

(3)配制溶液时,进行如下操作,正确的顺序是___________ (填标号)
C→_______⟶_______→_______⟶________⟶E

(4)在上述操作中未进行D操作,会导致所配制溶液的物质的量浓度_______ (填“偏大”“偏小”或“无影响”)。
(5)现需要配制两份成分完全 相同的某营养液各 ,配方如下表。
,配方如下表。
所配制的溶液中, 的物质的量浓度为
的物质的量浓度为___________  。实验员在配完第一份溶液时发现
。实验员在配完第一份溶液时发现 已经用完了,锌盐中备选试剂有
已经用完了,锌盐中备选试剂有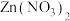 、
、 。实验员仍需配得第二份营养液,锌盐应选用
。实验员仍需配得第二份营养液,锌盐应选用___________ (写化学式)。为完成配制应取用 固体的物质的量为
固体的物质的量为___________ mol。
 营养液,现配制
营养液,现配制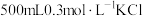 溶液。
溶液。(1)根据计算,需用托盘天平称量
 固体的质量为
固体的质量为(2)如图所示的仪器中,配制溶液肯定不需要的是
①温度②浓度③容积④压强

(3)配制溶液时,进行如下操作,正确的顺序是
C→_______⟶_______→_______⟶________⟶E

(4)在上述操作中未进行D操作,会导致所配制溶液的物质的量浓度
(5)现需要配制两份
 ,配方如下表。
,配方如下表。| 溶质 |  |  |  |
物质的量浓度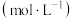 | 0.3 | 0.2 | 0.1 |
 的物质的量浓度为
的物质的量浓度为 。实验员在配完第一份溶液时发现
。实验员在配完第一份溶液时发现 已经用完了,锌盐中备选试剂有
已经用完了,锌盐中备选试剂有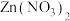 、
、 。实验员仍需配得第二份营养液,锌盐应选用
。实验员仍需配得第二份营养液,锌盐应选用 固体的物质的量为
固体的物质的量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某同学配制240mL 1.00mol·L-1 Na2CO3溶液,请回答有关问题。
(1)配制时,下列4个操作的顺序是(用序号表示,每个操作只能用一次)____ 。
①将已冷却的Na2CO3溶液沿玻璃棒注入____ 中;
②用天平准确称取____ g Na2CO3固体,加入少量蒸馏水(约30mL),用玻璃棒慢慢搅拌,使其充分溶解;
③塞上瓶塞,颠倒摇匀;
④继续往容量瓶内小心加水,直到液面接近刻度____ 处,改用____ 加水至溶液凹液面与刻度线相切。
(2)按上述步骤配制的Na2CO3溶液的浓度____ (选填“是”或“不是”)1.00mol·L-1,理由是____ 。
(1)配制时,下列4个操作的顺序是(用序号表示,每个操作只能用一次)
①将已冷却的Na2CO3溶液沿玻璃棒注入
②用天平准确称取
③塞上瓶塞,颠倒摇匀;
④继续往容量瓶内小心加水,直到液面接近刻度
(2)按上述步骤配制的Na2CO3溶液的浓度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室由安息香制备二苯乙二酮的反应式如下:
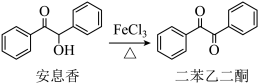
相关信息列表如下:
装置示意图所示,实验步骤为:
①在圆底烧瓶中加入10mL冰乙酸、5mL水及9.0gFeCl3∙6H2O,边搅拌边加热,至固体全部溶解。
②停止加热,待沸腾平息后加入2.0g安息香,加热回流45~60min。
③加入50mL水,煮沸后冷却,有黄色固体析出。
④过滤,并用冷水洗涤固体3次,得到粗品。
⑤粗品用75%的乙醇重结晶,干燥后得淡黄色结晶1.6g。
回答下列问题:
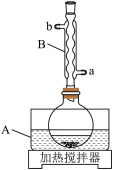
(1)仪器B的名称是___________ ;其作用是___________ ,冷却水应从___________ (填“a”或“b”)口通入。
(2)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是___________ 。
(3)冷水洗涤固体的目的是为了洗去___________ 。
(4)在本实验中,FeCl3为氧化剂且过量,其还原产物为___________ ;某同学尝试采用少量的FeCl3并通入空气也可制得二苯乙二酮。简述该方案可行的理由___________ 。
(5)若粗品中混有少量未氧化的安息香,可用少量___________ 洗涤的方法除去(填标号)。若要得到更高纯度的产品,可用重结晶的方法进一步提纯。
a.热水 b.乙酸 c.冷水 d.乙醇
(6)本实验的产率最接近于___________ (填标号)。
a.85% b.80% c.75% d.70%

相关信息列表如下:
| 物质 | 性状 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 安息香 | 白色固体 | 133 | 344 | 难溶于冷水 溶于热水、乙醇、乙酸 |
| 二苯乙二酮 | 淡黄色固体 | 95 | 347 | 不溶于水 溶于乙醇、苯、乙酸 |
| 冰乙酸 | 无色液体 | 17 | 118 | 与水、乙醇互溶 |
①在圆底烧瓶中加入10mL冰乙酸、5mL水及9.0gFeCl3∙6H2O,边搅拌边加热,至固体全部溶解。
②停止加热,待沸腾平息后加入2.0g安息香,加热回流45~60min。
③加入50mL水,煮沸后冷却,有黄色固体析出。
④过滤,并用冷水洗涤固体3次,得到粗品。
⑤粗品用75%的乙醇重结晶,干燥后得淡黄色结晶1.6g。
回答下列问题:

(1)仪器B的名称是
(2)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是
(3)冷水洗涤固体的目的是为了洗去
(4)在本实验中,FeCl3为氧化剂且过量,其还原产物为
(5)若粗品中混有少量未氧化的安息香,可用少量
a.热水 b.乙酸 c.冷水 d.乙醇
(6)本实验的产率最接近于
a.85% b.80% c.75% d.70%
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】I.如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:

(1)装置图1中A的名称是________________ ,B的名称是________________ 。A中一般要加入碎瓷片,其作用是________ 。下列关于上图实验操作说法一定正确的是______ (填字母)。
A 图1实验中,加热一段时间后发现未加入碎瓷片,应马上添加,以防发生危险
B 图2实验中,应打开活塞,将有机溶剂从下端导管中放出
C 图3实验中,可以用玻璃棒在漏斗中搅拌,以加快过滤速度
D 图4实验中,当加热至有较多固体析出时,即停止加热
(2)在图2所示实验中,静置分层后,如果不知道哪一层液体是“水层”,试设计一种简便的判断方法:________ 。
II.现用质量分数为98%、密度为1.84 g·cm-3的浓硫酸来配制480 mL 0.2 mol·L-1的稀硫酸。可供选择的仪器有:①玻璃棒 ②烧杯 ③胶头滴管 ④量筒,
请回答下列问题:
(1)上述仪器中,在配制稀硫酸时还需要用到的仪器有_____ (填名称)。
(2)经计算,浓硫酸物质的量的浓度________________ ;需用量筒量取浓硫酸的体积为 _________ ;现有①10 mL、②50mL、③100 mL三种规格的量筒,应选用的量筒是_______ (填代号)。
(3)在配制过程中,下列操作中会引起稀硫酸物质的量浓度偏低的有_______ (填代号)。
①洗涤量取浓硫酸后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的硫酸溶液冷却至室温就转移到容量瓶中
③定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
④转移前,容量瓶中含有少量蒸馏水
⑤量取浓硫酸时,俯视刻度线

(1)装置图1中A的名称是
A 图1实验中,加热一段时间后发现未加入碎瓷片,应马上添加,以防发生危险
B 图2实验中,应打开活塞,将有机溶剂从下端导管中放出
C 图3实验中,可以用玻璃棒在漏斗中搅拌,以加快过滤速度
D 图4实验中,当加热至有较多固体析出时,即停止加热
(2)在图2所示实验中,静置分层后,如果不知道哪一层液体是“水层”,试设计一种简便的判断方法:
II.现用质量分数为98%、密度为1.84 g·cm-3的浓硫酸来配制480 mL 0.2 mol·L-1的稀硫酸。可供选择的仪器有:①玻璃棒 ②烧杯 ③胶头滴管 ④量筒,
请回答下列问题:
(1)上述仪器中,在配制稀硫酸时还需要用到的仪器有
(2)经计算,浓硫酸物质的量的浓度
(3)在配制过程中,下列操作中会引起稀硫酸物质的量浓度偏低的有
①洗涤量取浓硫酸后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的硫酸溶液冷却至室温就转移到容量瓶中
③定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
④转移前,容量瓶中含有少量蒸馏水
⑤量取浓硫酸时,俯视刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】Ⅰ.下图为实验室蒸馏自来水得到少量蒸馏水的装置示意图,请根据图示回答下列问题:
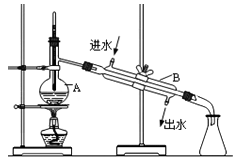
(1)装置中仪器A的名称是___________ ,仪器B 的名称是_____________ 。
(2)请指出上图中的三处明显错误中的两处:__________ 、__________ 。
Ⅱ.选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.蒸馏 B.过滤 C.结晶 D.分液
(1)分离水和煤油的混合物__________ 。
(2)从硝酸钾和氯化钠的混合液中获得硝酸钾__________ 。
(3)从加热氯酸钾制氧气后的剩余固体中获得MnO2。溶解、__________ 。
(4)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物____________ 。

(1)装置中仪器A的名称是
(2)请指出上图中的三处明显错误中的两处:
Ⅱ.选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.蒸馏 B.过滤 C.结晶 D.分液
(1)分离水和煤油的混合物
(2)从硝酸钾和氯化钠的混合液中获得硝酸钾
(3)从加热氯酸钾制氧气后的剩余固体中获得MnO2。溶解、
(4)分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物
您最近一年使用:0次



