现有混有氯化钠杂质碳酸钠固体,为测定其中碳酸钠的质量分数,设计如下方案:
(1)称取20.0g上述固体,溶于水配成溶液,加入过量的CaCl2溶液,溶液变浑浊,过滤洗涤干燥,得到固体10g,求碳酸钠的质量分数。______________
(2)现取等质量的上述固体,加入过量的盐酸,求生成的气体在标准状况下的体积。__________
(1)称取20.0g上述固体,溶于水配成溶液,加入过量的CaCl2溶液,溶液变浑浊,过滤洗涤干燥,得到固体10g,求碳酸钠的质量分数。
(2)现取等质量的上述固体,加入过量的盐酸,求生成的气体在标准状况下的体积。
更新时间:2018-01-10 23:11:52
|
相似题推荐
计算题
|
适中
(0.65)
真题
名校
【推荐1】生态溶液涉及农家肥料的综合利用,某种肥料经发酵得到一种含有甲烷、二氧化碳、氮气的混合气体。2.016L(标准状况)该气体通过盛有红色CuO粉末的硬质玻璃管,发生的反应为:CH4+4CuO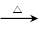 CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8g。将反应后产生的气体通过过量的澄清石灰水,充分吸收,生成沉淀8.5g。
CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8g。将反应后产生的气体通过过量的澄清石灰水,充分吸收,生成沉淀8.5g。
(1)原混合气体中甲烷的物质的量是____________ 。
(2)原混合气体中氮气的体积分数为多少?(写出计算过程)
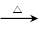 CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8g。将反应后产生的气体通过过量的澄清石灰水,充分吸收,生成沉淀8.5g。
CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8g。将反应后产生的气体通过过量的澄清石灰水,充分吸收,生成沉淀8.5g。(1)原混合气体中甲烷的物质的量是
(2)原混合气体中氮气的体积分数为多少?(写出计算过程)
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】市售铁强化盐中铁含量测定。
已知:①铁强化盐中含有NaCl、KIO3、NaFeY,其中n(KIO3):n(NaFeY)=1:50,
②I2+2S2O =2I-+S4O
=2I-+S4O
称取m g样品,加稀硫酸溶解后配成100 mL溶液。取出10 mL,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用c mol/L Na2S2O3标准溶液滴定,重复操作2~3次,消耗Na2S2O3标准溶液平均值为V mL。
(1)I-除了与Fe3+反应外,还可发生的反应的离子方程式为___________ 。
(2)样品中铁元素的质量分数为___________ (列出式子即可)。
已知:①铁强化盐中含有NaCl、KIO3、NaFeY,其中n(KIO3):n(NaFeY)=1:50,
②I2+2S2O
 =2I-+S4O
=2I-+S4O
称取m g样品,加稀硫酸溶解后配成100 mL溶液。取出10 mL,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用c mol/L Na2S2O3标准溶液滴定,重复操作2~3次,消耗Na2S2O3标准溶液平均值为V mL。
(1)I-除了与Fe3+反应外,还可发生的反应的离子方程式为
(2)样品中铁元素的质量分数为
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】固体化合物 X 由 3 种元素组成。某学习小组进行了如下实验:
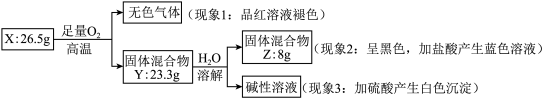
请回答:
(1)由现象 1 得出化合物 X 含有_____________ 元素(填元素符号),X 的化学式_____________ 。
(2)固体混合物 Y 的成分_____________ (填化学式)。
(3)实验室常将氨气(NH3)通过红热的黑色固体化合物 Z 制备氮气,该反应的化学方程式是_____________ 。

请回答:
(1)由现象 1 得出化合物 X 含有
(2)固体混合物 Y 的成分
(3)实验室常将氨气(NH3)通过红热的黑色固体化合物 Z 制备氮气,该反应的化学方程式是
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐2】取m克铁粉与1 L 1.2 mol/L的稀HNO3恰好完全反应,反应后的溶液中只含Fe2+且硝酸的还原产物只有NO。则:
(1)m=______________ g。
(2)若将反应后的溶液低温蒸干,析出晶体135 g,则析出晶体的组成可能是_________ 。
a.Fe(NO3)2∙7H2O和Fe(NO3)2∙4H2O
b.Fe(NO3)2∙7H2O和Fe(NO3)2∙H2O
c.Fe(NO3)2∙4H2O和Fe(NO3)2∙H2O
(3)若向反应后的溶液中加入100 mL 1.5 mol/L的稀H2SO4,则标准状态下还能产生NO的体积为______ L。
(1)m=
(2)若将反应后的溶液低温蒸干,析出晶体135 g,则析出晶体的组成可能是
a.Fe(NO3)2∙7H2O和Fe(NO3)2∙4H2O
b.Fe(NO3)2∙7H2O和Fe(NO3)2∙H2O
c.Fe(NO3)2∙4H2O和Fe(NO3)2∙H2O
(3)若向反应后的溶液中加入100 mL 1.5 mol/L的稀H2SO4,则标准状态下还能产生NO的体积为
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】I.将200mLH2SO4 和Fe2(SO4)3的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少4.48g;向另一份中加入足量BaCl2溶液,经过滤、洗涤、干 燥、称量,得到46.6g 白色沉淀。则:
(1)原溶液中c( )=
)=_______ ;
(2)原溶液中H2SO4和Fe2(SO4)3的物质的量浓度之比为_______ 。
(3)实验室中的FeSO4溶液常因氧化而变质。除杂的方法是______________________ ,检验是否变质的方法是_______
II.准确称取某种铁的氧化物2.88 g,用足量的CO进行还原,将生成的CO2全部用足量的澄清石灰水吸收,得到沉淀4 g,则这种铁的氧化物为_______
(1)原溶液中c(
 )=
)=(2)原溶液中H2SO4和Fe2(SO4)3的物质的量浓度之比为
(3)实验室中的FeSO4溶液常因氧化而变质。除杂的方法是
II.准确称取某种铁的氧化物2.88 g,用足量的CO进行还原,将生成的CO2全部用足量的澄清石灰水吸收,得到沉淀4 g,则这种铁的氧化物为
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐1】现有Na2CO3和NaHCO3的混合物共13.7g,现把混合物充分加热到不再有气体放出为止,发现混合物质量变为10.6g,试计算原混合物中Na2CO3的物质的量。
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】将镁、铝、铁各0.3 mol分别放入100 mL 1mol/L的盐酸中,求同温同压下产生的气体体积之比是多少?(请写出计算过程)____________
您最近半年使用:0次



