根据金属及其化合物的所学知识回答下列问题:
(1)常温下,在没有氧气存在时,铁与水几乎不反应,但在高温下,铁能与水蒸气反应。写出化学反应方程式________________________ 。
(2)待(1)中的反应完全,所得固体中Fe元素化合价为_________ ,该物质与盐酸反应的离子方程式为_________________________ 。
(3)将铁粉投入到盛有Cu2+、Fe3+的溶液中,反应完毕时,若烧杯底部有固体剩余,溶液中一定不含的金属离子是____________ ,若烧杯中没有铁粉剩余,则溶液中一定含有的金属离子是________ ,写出证明溶液中是否有Fe3+的实验操作方法____________ 。
(4)向盛有Ca(HCO3)2溶液的水槽中,加入一小块金属钠。下列现象描述正确的是_________ (填字母)。
A.钠浮在液面上,并四处游动,最后消失 B.钠熔化成一个光亮的小球
C.反应开始后,溶液由无色变红色 D.恢复到室温时,烧杯底部有固体物质析出
(1)常温下,在没有氧气存在时,铁与水几乎不反应,但在高温下,铁能与水蒸气反应。写出化学反应方程式
(2)待(1)中的反应完全,所得固体中Fe元素化合价为
(3)将铁粉投入到盛有Cu2+、Fe3+的溶液中,反应完毕时,若烧杯底部有固体剩余,溶液中一定不含的金属离子是
(4)向盛有Ca(HCO3)2溶液的水槽中,加入一小块金属钠。下列现象描述正确的是
A.钠浮在液面上,并四处游动,最后消失 B.钠熔化成一个光亮的小球
C.反应开始后,溶液由无色变红色 D.恢复到室温时,烧杯底部有固体物质析出
更新时间:2018-01-12 20:07:25
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】金属钠及其化合物在材料和工业生产方面有着重要作用。
Ⅰ.Na的生产和性质。
(1) 的熔点为
的熔点为 ,但加入
,但加入 形成混合盐后
形成混合盐后 的熔点降低到580℃,故工业上,采用电解熔融的混合盐来制备金属
的熔点降低到580℃,故工业上,采用电解熔融的混合盐来制备金属 ,电解的化学方程式为:
,电解的化学方程式为: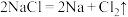 ,加入
,加入 的目的是
的目的是___________ 。
(2)将金属钠放入盛有下列溶液的小烧杯中,既有气体产生,又有沉淀产生的是___________ (填序号)。
① 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④饱和的澄清石灰水 ⑤
溶液 ④饱和的澄清石灰水 ⑤ 溶液 ⑥
溶液 ⑥ 溶液 ⑦
溶液 ⑦ 溶液
溶液
Ⅱ. 是
是 的重要氧化物。
的重要氧化物。
(3) 的电子式是
的电子式是___________ 。
(4)向酸性 溶液中加入
溶液中加入 粉末,观察到溶液褪色,配平下述反应方程式
粉末,观察到溶液褪色,配平下述反应方程式____________
 →
→
(5)200℃时,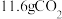 和
和 的混合气体与足量的
的混合气体与足量的 反应,反应后固体增加了
反应,反应后固体增加了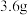 ,则原混合气体的平均摩尔质量为
,则原混合气体的平均摩尔质量为___________  。
。
Ⅲ.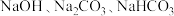 之间在一定条件下能相互转化。
之间在一定条件下能相互转化。
(6)向 中通入一定量的
中通入一定量的 气体,充分反应得到溶液X后,再向所得溶液X中逐滴加入稀盐酸。产生
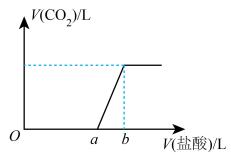
气体,充分反应得到溶液X后,再向所得溶液X中逐滴加入稀盐酸。产生 的体积与所加盐酸体积之间的关系如图所示,完成下列表格:
的体积与所加盐酸体积之间的关系如图所示,完成下列表格:
Ⅰ.Na的生产和性质。
(1)
 的熔点为
的熔点为 ,但加入
,但加入 形成混合盐后
形成混合盐后 的熔点降低到580℃,故工业上,采用电解熔融的混合盐来制备金属
的熔点降低到580℃,故工业上,采用电解熔融的混合盐来制备金属 ,电解的化学方程式为:
,电解的化学方程式为: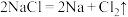 ,加入
,加入 的目的是
的目的是(2)将金属钠放入盛有下列溶液的小烧杯中,既有气体产生,又有沉淀产生的是
①
 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④饱和的澄清石灰水 ⑤
溶液 ④饱和的澄清石灰水 ⑤ 溶液 ⑥
溶液 ⑥ 溶液 ⑦
溶液 ⑦ 溶液
溶液Ⅱ.
 是
是 的重要氧化物。
的重要氧化物。(3)
 的电子式是
的电子式是(4)向酸性
 溶液中加入
溶液中加入 粉末,观察到溶液褪色,配平下述反应方程式
粉末,观察到溶液褪色,配平下述反应方程式 →
→
(5)200℃时,
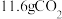 和
和 的混合气体与足量的
的混合气体与足量的 反应,反应后固体增加了
反应,反应后固体增加了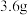 ,则原混合气体的平均摩尔质量为
,则原混合气体的平均摩尔质量为 。
。Ⅲ.
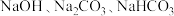 之间在一定条件下能相互转化。
之间在一定条件下能相互转化。(6)向
 中通入一定量的
中通入一定量的 气体,充分反应得到溶液X后,再向所得溶液X中逐滴加入稀盐酸。产生
气体,充分反应得到溶液X后,再向所得溶液X中逐滴加入稀盐酸。产生 的体积与所加盐酸体积之间的关系如图所示,完成下列表格:
的体积与所加盐酸体积之间的关系如图所示,完成下列表格:
| V(盐酸)/L | 溶液X溶质 | 通入 得到溶液X的离子方程式 得到溶液X的离子方程式 |
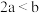 | ① | |
 | ② | |
 | ③ | ④ |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题。
(1)将金属钠投入FeCl3溶液中的离子方程式___________ 。
(2)请写出将 通入水中发生的离子反应方程式
通入水中发生的离子反应方程式___________ 。
(3)写出硫酸氢钠在熔融状态下的电离方程式___________ 。
(4)过氧化钠与水的反应中,其中水的作用是___________ (填“氧化剂”或“还原剂”或“既不是氧化剂也不是还原剂”)。
(5)84消毒液不能与洁厕灵大量混合使用的原因是___________ (书写离子方程式)。
(6)漂白粉的主要成分___________ 。(填化学式)
(1)将金属钠投入FeCl3溶液中的离子方程式
(2)请写出将
 通入水中发生的离子反应方程式
通入水中发生的离子反应方程式(3)写出硫酸氢钠在熔融状态下的电离方程式
(4)过氧化钠与水的反应中,其中水的作用是
(5)84消毒液不能与洁厕灵大量混合使用的原因是
(6)漂白粉的主要成分
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】钠、氯及其化合物在生产和生活中有广泛的应用。金属钠是在1807年通过电解氢氧化钠制得的,这个原理应用于工业生产,约在1891年才获得成功。1921年实现了电解氯化钠制得工业方法,其反应原理: 。根据所学知识完成下列各题。
。根据所学知识完成下列各题。
(1)下列各项中保存金属钠的正确方法是_______。
(2)将金属钠放入 溶液中会产生蓝色沉淀,请用化学方程式解释这一现象
溶液中会产生蓝色沉淀,请用化学方程式解释这一现象_______ 。
(3)将一小块金属钠放在干燥的坩埚中,用酒精灯加热充分反应,其现象为_______ 。请写出发生反应的化学方程式:_______ 。
(4)钠的一种氧化物常用于呼吸面具和潜水艇氧气的来源,用化学反应方程式表示其原理:_______ 。
(5)已知金属钠在二氧化碳中燃烧生成碳酸钠和一种黑色固体,请写出该反应的化学方程式,并用双线桥表示电子的转移_______ 。
 。根据所学知识完成下列各题。
。根据所学知识完成下列各题。(1)下列各项中保存金属钠的正确方法是_______。
| A.石蜡封存 | B.放在细沙中 | C.放在水中 | D.放在煤油中 |
 溶液中会产生蓝色沉淀,请用化学方程式解释这一现象
溶液中会产生蓝色沉淀,请用化学方程式解释这一现象(3)将一小块金属钠放在干燥的坩埚中,用酒精灯加热充分反应,其现象为
(4)钠的一种氧化物常用于呼吸面具和潜水艇氧气的来源,用化学反应方程式表示其原理:
(5)已知金属钠在二氧化碳中燃烧生成碳酸钠和一种黑色固体,请写出该反应的化学方程式,并用双线桥表示电子的转移
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】铁是目前产量最大、使用最广泛的金属。
(1)铁元素26号元素,位于周期表第四周期第_______ 族,其原子最外电子层上只有2个电子,次外层上有_______ 个电子。
(2)写出下列反应的化学方程式或离子方程式。
①高温下,铁跟水蒸气反应的化学方程式是:_______ 。
②已知锰元素的常见化合价有+7、+6、+4、+2等,则加热条件下,铁、锰合金粉未跟 反应的化学方程为:
反应的化学方程为:_______ 、_______ 。
③已知 溶液跟
溶液跟 反应有红褐色
反应有红褐色 沉淀生成,且溶液呈棕黄色,则反应的离子方程式为:
沉淀生成,且溶液呈棕黄色,则反应的离子方程式为:_______ 。
(3) 与
与 混合后在缺氧条件下焙烧生成
混合后在缺氧条件下焙烧生成 和
和 ,理论上完全反应消耗的
,理论上完全反应消耗的
_______ ,
(4)石墨稀负载的纳米铁活性强,能迅速有效地吸附和还原污水中的 ,纳米铁还原废水中
,纳米铁还原废水中 的可能反应机理如图表示。纳米铁还原
的可能反应机理如图表示。纳米铁还原 生成
生成 或
或 的过程可描述为:
的过程可描述为:
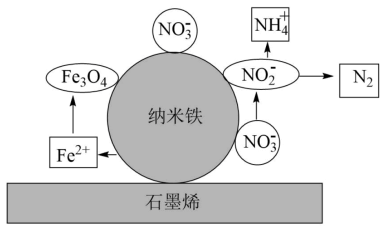
①_______ ,
②吸附在纳米铁表面的 得到的电子还原生成
得到的电子还原生成 ,
,
③_______ 。
(1)铁元素26号元素,位于周期表第四周期第
(2)写出下列反应的化学方程式或离子方程式。
①高温下,铁跟水蒸气反应的化学方程式是:
②已知锰元素的常见化合价有+7、+6、+4、+2等,则加热条件下,铁、锰合金粉未跟
 反应的化学方程为:
反应的化学方程为:③已知
 溶液跟
溶液跟 反应有红褐色
反应有红褐色 沉淀生成,且溶液呈棕黄色,则反应的离子方程式为:
沉淀生成,且溶液呈棕黄色,则反应的离子方程式为:(3)
 与
与 混合后在缺氧条件下焙烧生成
混合后在缺氧条件下焙烧生成 和
和 ,理论上完全反应消耗的
,理论上完全反应消耗的
(4)石墨稀负载的纳米铁活性强,能迅速有效地吸附和还原污水中的
 ,纳米铁还原废水中
,纳米铁还原废水中 的可能反应机理如图表示。纳米铁还原
的可能反应机理如图表示。纳米铁还原 生成
生成 或
或 的过程可描述为:
的过程可描述为:
①
②吸附在纳米铁表面的
 得到的电子还原生成
得到的电子还原生成 ,
,③
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某探究小组采用下图所示装置进行Fe粉与水蒸气的反应。

(1)实验前检查装置气密性的方法为______________ 。
(2)检验实验中生成气体的实验操作是_____________ 。
(3)写出试管中发生的化学反应方程式________________

(1)实验前检查装置气密性的方法为
(2)检验实验中生成气体的实验操作是
(3)写出试管中发生的化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(NH4)2Fe(SO4)2·6H2O(硫酸亚铁铵)是一种重要的化工原料,用途广泛。完成下列填空:
(1)铁在元素周期表的第ⅦB和第ⅠB之间。铁位于第___ 周期___ 族。
(2)写出Fe与水反应的化学方程式:___ 。
(3)将(NH4)2Fe(SO4)2中非金属元素的简单阴离子按半径由小到大的顺序排列:___ 。
(4)同温度同浓度的FeSO4和(NH4)2Fe(SO4)2溶液中,c(Fe2+)是否相等___ ?为什么?___ 。
(5)设计实验,证明(NH4)2Fe(SO4)2·6H2O晶体中含有Fe2+___ 。
(6)已知:(NH4)2Fe(SO4)2·6H2O在200℃失去全部结晶水。将一定质量的粉末状该晶体置于坩埚中,保持200℃受热,经冷却、恒重等正确操作,计算得到的1mol晶体中结晶水含量总是偏低,偏低的可能原因是___ (写一条即可)。
(1)铁在元素周期表的第ⅦB和第ⅠB之间。铁位于第
(2)写出Fe与水反应的化学方程式:
(3)将(NH4)2Fe(SO4)2中非金属元素的简单阴离子按半径由小到大的顺序排列:
(4)同温度同浓度的FeSO4和(NH4)2Fe(SO4)2溶液中,c(Fe2+)是否相等
(5)设计实验,证明(NH4)2Fe(SO4)2·6H2O晶体中含有Fe2+
(6)已知:(NH4)2Fe(SO4)2·6H2O在200℃失去全部结晶水。将一定质量的粉末状该晶体置于坩埚中,保持200℃受热,经冷却、恒重等正确操作,计算得到的1mol晶体中结晶水含量总是偏低,偏低的可能原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】从元素化合价和物质类别两个角度研究物质的性质是一种行之有效的方法。如图是由铁元素组成的物质的部分信息。

(1)写出X的化学式:___________ 。
(2)①FeO与稀硫酸反应的离子方程式:___________ 。
②Y物质在空气中变化的化学方程式___________ 该变化的现象是___________ 。
(3)一定量的铁粉在氯气中充分燃烧后,将所得固体完全溶于稀盐酸,制得溶液A。
①推测溶液A中可能含有的金属阳离子:a.只有Fe3+; b.只有Fe2+;c.___________ 。
②甲同学为探究溶液的组成,实验如下:取少量溶液A置于试管中,加入KSCN溶液,溶液_______ ,说明假设b不成立,假设a或c成立;
(4)乙同学继续探究溶液A的组成。
查阅资料:16HCl+2KMnO4=2KCl+2MnCl2+5Cl2↑+8H2O
实验过程:另取少量溶液A置于试管中,逐滴加入酸性KMnO4溶液,充分振荡,KMnO4溶液紫色褪去。实验结论:___________ (填写字母序号)。
A.可能有Fe2+ B.可能无Fe2+ C.一定有Fe2+
根据你选择的实验结论,简述理由:___________ 。

(1)写出X的化学式:
(2)①FeO与稀硫酸反应的离子方程式:
②Y物质在空气中变化的化学方程式
(3)一定量的铁粉在氯气中充分燃烧后,将所得固体完全溶于稀盐酸,制得溶液A。
①推测溶液A中可能含有的金属阳离子:a.只有Fe3+; b.只有Fe2+;c.
②甲同学为探究溶液的组成,实验如下:取少量溶液A置于试管中,加入KSCN溶液,溶液
(4)乙同学继续探究溶液A的组成。
查阅资料:16HCl+2KMnO4=2KCl+2MnCl2+5Cl2↑+8H2O
实验过程:另取少量溶液A置于试管中,逐滴加入酸性KMnO4溶液,充分振荡,KMnO4溶液紫色褪去。实验结论:
A.可能有Fe2+ B.可能无Fe2+ C.一定有Fe2+
根据你选择的实验结论,简述理由:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】H2S是一种无色、有毒的可燃性气体,其水溶液叫氢硫酸(二元弱酸)。
(1)实验室可用硫化亚铁固体与稀硫酸反应来制备H2S气体。
①该反应的化学方程式为____________________________ 。
②多余的H2S气体可用_____________ 溶液来吸收,不能用燃烧的方法处理H2S气体的理由是___________ 。
(2)用30% FeCl3溶液作吸收液也能吸收H2S气体,反应方程式为:2FeCl3+H2S = S↓+2FeCl2+2HCl,废吸收液经电解可循环使用。
①该反应中H2S显__________ (填字母)。
a、不稳定性 b、弱酸性 c、氧化性 d、还原性
②检验废吸收液中是否含有Fe3+的适宜试剂是___________ 。
③强酸性的废吸收液电解可生成FeCl3和一种分子量最小的气体,则化学方程式为____________ 。
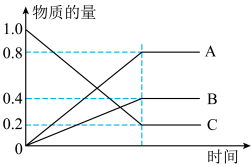
(3)已知:H2S在高温下分解生成硫蒸气和H2。现测得某温度下,H2S分解过程中各物质的物质的量随时间变化关系如图所示。
①表示H2的曲线是__________ (填“A”、“B”或“C”)。
②生成硫蒸气的分子式为__________ 。
(1)实验室可用硫化亚铁固体与稀硫酸反应来制备H2S气体。
①该反应的化学方程式为
②多余的H2S气体可用
(2)用30% FeCl3溶液作吸收液也能吸收H2S气体,反应方程式为:2FeCl3+H2S = S↓+2FeCl2+2HCl,废吸收液经电解可循环使用。
①该反应中H2S显
a、不稳定性 b、弱酸性 c、氧化性 d、还原性
②检验废吸收液中是否含有Fe3+的适宜试剂是
③强酸性的废吸收液电解可生成FeCl3和一种分子量最小的气体,则化学方程式为
(3)已知:H2S在高温下分解生成硫蒸气和H2。现测得某温度下,H2S分解过程中各物质的物质的量随时间变化关系如图所示。

①表示H2的曲线是
②生成硫蒸气的分子式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某Fe2(SO4)3样品含有少量FeSO4杂质,将其配成溶液。
①若要检验溶液中的Fe3+,可加入___ 试剂(填化学式),观察溶液呈血红色。反应的离子方程式:___ 。
②若要检验溶液中的Fe2+,下列方法可行的是:___ 。
A.取少量溶液于试管中,滴入几滴酸性高锰酸钾溶液,若紫红色褪去,则含有Fe2+
B.取少量溶液于试管中,加入新制氯水,再滴入硫氰化钾,若呈血红色,则含有Fe2+
C.取少量溶液于试管中,滴入NaOH溶液,看到白色沉淀迅速变为灰绿再变为红褐色,则含有Fe2+
(2)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,某学习小组设计如图方案制备高铁酸钾:

①高铁酸钾中铁元素的化合价为___ ,据此推测它具有的化学性质是____ 。
②其中第一步操作是:在NaClO溶液中加入烧碱固体形成强碱性环境,将研磨过的硝酸铁少量多次地加入上述溶液中,温度保持0℃反应1h,则采用的合适控温方式是___ 。发生的离子反应为:___ 。
③高铁酸钾和水发生反应,生成一种胶体能吸附杂质净水,同时还产生气体,写出反应的离子方程式:___ 。
①若要检验溶液中的Fe3+,可加入
②若要检验溶液中的Fe2+,下列方法可行的是:
A.取少量溶液于试管中,滴入几滴酸性高锰酸钾溶液,若紫红色褪去,则含有Fe2+
B.取少量溶液于试管中,加入新制氯水,再滴入硫氰化钾,若呈血红色,则含有Fe2+
C.取少量溶液于试管中,滴入NaOH溶液,看到白色沉淀迅速变为灰绿再变为红褐色,则含有Fe2+
(2)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,某学习小组设计如图方案制备高铁酸钾:

①高铁酸钾中铁元素的化合价为
②其中第一步操作是:在NaClO溶液中加入烧碱固体形成强碱性环境,将研磨过的硝酸铁少量多次地加入上述溶液中,温度保持0℃反应1h,则采用的合适控温方式是
③高铁酸钾和水发生反应,生成一种胶体能吸附杂质净水,同时还产生气体,写出反应的离子方程式:
您最近一年使用:0次



