目前已开发出用电解法制取ClO2的新工艺。
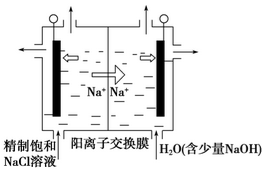
(1)图中用石墨做电极,在一定条件下电解饱和食盐水制取ClO2。则阳极产生ClO2的电极反应式为___________________________________________ 。
(2)电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为________ mol

(1)图中用石墨做电极,在一定条件下电解饱和食盐水制取ClO2。则阳极产生ClO2的电极反应式为
(2)电解一段时间,当阴极产生的气体体积为112 mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为
更新时间:2018-02-25 10:29:59
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】下图中反应①是制备SiH4的一种方法,其副产物MgCl2·6NH3是优质的镁资源。回答下列问题:
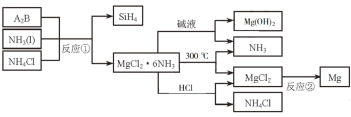
(1)MgCl2·6NH3所含元素的简单离子半径由小到大的顺序(H− 除外)___________ ,Mg在元素周期表中的位置:___________ ,Mg(OH)2的电子式:___________ 。
(2)A2B的化学式为___________ 。反应②的必备条件是___________ 。上图中可以循环使用的物质有___________ 。
(3)在一定条件下,由SiH4和CH4反应生成H2和一种固体耐磨材料___________ (写化学式)。
(4)为实现燃煤脱硫,向煤中加入浆状Mg(OH)2,使燃烧产生的SO2转化为稳定的Mg化合物,写出该反应的化学方程式:___________ 。

(1)MgCl2·6NH3所含元素的简单离子半径由小到大的顺序(H− 除外)
(2)A2B的化学式为
(3)在一定条件下,由SiH4和CH4反应生成H2和一种固体耐磨材料
(4)为实现燃煤脱硫,向煤中加入浆状Mg(OH)2,使燃烧产生的SO2转化为稳定的Mg化合物,写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ.电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应为 。
。
(1)铅蓄电池放电时,负极质量_______ (填“变大”“变小”或“不变”),正极反应式为_______ 。
(2)充电时,铅蓄电池的负极应连接外电源的_______ (填“正极”或“负极”)。
(3)用惰性电极电解足量饱和食盐水时,若用铅蓄电池作外电源,当两电极共收集到 (标准气体时,消耗铅蓄电池中
(标准气体时,消耗铅蓄电池中 的物质的量为
的物质的量为_______ 。
(4)若用铅蓄电池作外电源进行粗铜的精炼,则连接粗铜的电极为_______ (填“Pb”或“PbO2”)。
Ⅱ.一氧化碳催化加氢制甲醇的反应原理为
已知断开 下列化学键吸收的能量如下表所示:
下列化学键吸收的能量如下表所示:
(5)上表中的x为_______ 。
 。
。(1)铅蓄电池放电时,负极质量
(2)充电时,铅蓄电池的负极应连接外电源的
(3)用惰性电极电解足量饱和食盐水时,若用铅蓄电池作外电源,当两电极共收集到
 (标准气体时,消耗铅蓄电池中
(标准气体时,消耗铅蓄电池中 的物质的量为
的物质的量为(4)若用铅蓄电池作外电源进行粗铜的精炼,则连接粗铜的电极为
Ⅱ.一氧化碳催化加氢制甲醇的反应原理为

已知断开
 下列化学键吸收的能量如下表所示:
下列化学键吸收的能量如下表所示:| 化学键 |  |  | 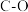 |  |  (CO的化学键) (CO的化学键) |
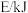 | x | 413 | 348 | 463 | 1076 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】电解原理在化学工业中有广泛应用。
(1)电解食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如图所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:
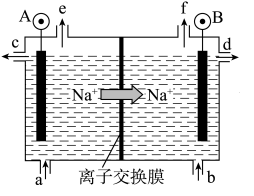
精制饱和食盐水在b口加入的物质为___________ (写化学式)
(2)全钒液流电池是一种新型的绿色环保储能系统,工作原理如图:
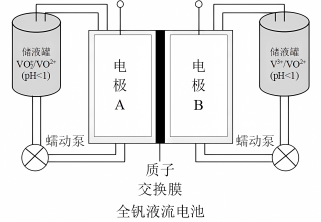
①全钒液流电池放电时V2+发生氧化反应,该电池放电时总反应式是___________ 。
②当完成储能时,阴极溶液的颜色是___________
(3)将PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示。
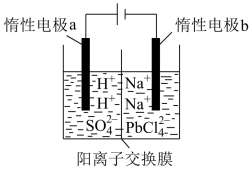
①写出电解时阴极的电极反应式___________
②电解过程中通过阳离子交换膜的离子主要为___________
③电解过程中,Na2PbCl4电解液浓度不断减小,为了恢复其浓度,应该向___________ 极室(填“阴”或者“阳”)加入___________ (填化学式)。
(1)电解食盐水是氯碱工业的基础。目前比较先进的方法是阳离子交换膜法,电解示意图如图所示,图中的阳离子交换膜只允许阳离子通过,请回答以下问题:

精制饱和食盐水在b口加入的物质为
(2)全钒液流电池是一种新型的绿色环保储能系统,工作原理如图:
| 离子种类 | VO | VO2+ | V3+ | V2+ |
| 颜色 | 黄色 | 蓝色 | 绿色 | 紫色 |

①全钒液流电池放电时V2+发生氧化反应,该电池放电时总反应式是
②当完成储能时,阴极溶液的颜色是
(3)将PbO溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液生成Pb的装置如图所示。

①写出电解时阴极的电极反应式
②电解过程中通过阳离子交换膜的离子主要为
③电解过程中,Na2PbCl4电解液浓度不断减小,为了恢复其浓度,应该向
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某实验小组同学对电化学原理进行了一系列探究活动。
(1)如图为某实验小组依据氧化还原反应设计的原电池装置,反应前,电极质量相等,一段时间后,两电极质量相差12 g,导线中通过________ mol电子。
(2)其他条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极会产生气泡,这是由于NH4Cl溶液显________ (填“酸性”“碱性”或“中性”),用离子方程式表示溶液显此性的原因__________________ ,用吸管吸出铁片附近溶液少许置于试管中,向其中滴加少量新制饱和氯水,然后滴加几滴硫氰化钾溶液,溶液变红,继续滴加过量新制饱和氯水,颜色褪去,同学们对此做了多种假设,某同学的假设是:“溶液中的+3价铁被氧化为更高的价态。”如果+3价铁被氧化为FeO42-,试写出该反应(红色褪去)的离子方程式:______________ 。
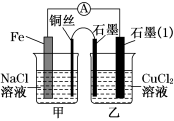
(3)如图其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图所示。一段时间后,在甲装置铜丝电极反应为___________________ ;乙装置中石墨(1)电极现象为__________________________ 。
(1)如图为某实验小组依据氧化还原反应设计的原电池装置,反应前,电极质量相等,一段时间后,两电极质量相差12 g,导线中通过
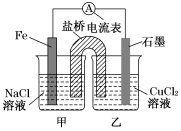
(2)其他条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极会产生气泡,这是由于NH4Cl溶液显
(3)如图其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,如图所示。一段时间后,在甲装置铜丝电极反应为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的开关时,观察到电流表的指针发生了偏转。
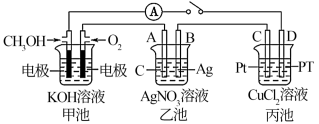
请回答下列问题:
(1)甲池为原电池,通入CH3OH电极的电极反应为__ 。
(2)乙池中A(石墨)电极的名称为___ (填“正极”“负极”或“阴极”“阳极”),总化学反应方程式为___ 。
(3)当乙池B极质量增加5.4g时,甲池中理论上消耗O2的体积为__ mL(标准状况),丙池D极析出___ g铜。
(4)若将丙池CuCl2溶液换成NaCl溶液,发生的总化学反应方程式为__ 。

请回答下列问题:
(1)甲池为原电池,通入CH3OH电极的电极反应为
(2)乙池中A(石墨)电极的名称为
(3)当乙池B极质量增加5.4g时,甲池中理论上消耗O2的体积为
(4)若将丙池CuCl2溶液换成NaCl溶液,发生的总化学反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】电解原理和原电池原理是电化的两个重要内容。某兴趣小组做如下探究实验:
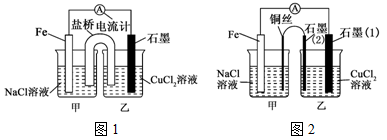
(1)如图1为某实验小组依据氧化还原反应设计的原电池装置,该反应的离子方程式为_______________________ 。反应前,电极质量相等,一段时间后,两电极质量相差12g,导线中通过_______ mol电子。
(2)其他条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极的反应式为________________ 。
(3)如图2,其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,则乙装置中石墨(1)为____ 极(填正、负、阴、阳),乙装置中石墨(2)电极上发生的反应式为_________________ 。
(4)在图2乙装置中改为加入400 mL CuSO4溶液,一段时间后,若电极质量增重1.28g,则此时溶液的pH为_______________ 。

(1)如图1为某实验小组依据氧化还原反应设计的原电池装置,该反应的离子方程式为
(2)其他条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极的反应式为
(3)如图2,其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,则乙装置中石墨(1)为
(4)在图2乙装置中改为加入400 mL CuSO4溶液,一段时间后,若电极质量增重1.28g,则此时溶液的pH为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】在如图中,甲烧杯中盛有100 mL 0.50 mol•L-1 AgNO3溶液,乙烧杯中盛有100 mL 0.25 mol•L-1 CuCl2溶液,A、B、C、D均为质量相同的石墨电极,如果电解一段时间后,发现A极比C极重1.9 g,则
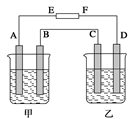
(1)电源E为________ 极。
(2)A极析出物质______ mol。
(3)B极的电极反应式为____________________ 。
(4)C极的电极反应式为_____________________ 。
(5)D极析出气体________ mL(标准状况)。

(1)电源E为
(2)A极析出物质
(3)B极的电极反应式为
(4)C极的电极反应式为
(5)D极析出气体
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.某兴趣小组的同学用下图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流计的指针发生了偏转。请回答下列问题:
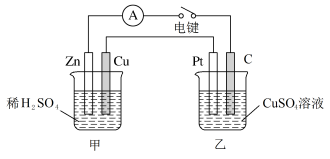
(1)甲装置的名称是_______ (填“原电池”或“电解池”)。
(2)写出电极反应式:Pt极_______ ;当甲中产生0.1 mol气体时,乙中析出铜的质量应为_______ 。
(3)若乙中溶液不变,将其电极都换成铜电极,电键闭合一段时间后,乙中溶液的颜色_______ (填“变深”、“变浅”或“无变化”)。
(4)若乙池溶液通电一段时间后,向所得的溶液中加入0.1mol的Cu(OH)2后恰好恢复到电解前的浓度。则电解过程中转移电子的数目为_______ 。(用NA表示)
II.由Cu2+、 、Na+、
、Na+、 四种离子中的两种离子组成的电解质溶液若干种,可选用铁电极、铜电极、铂电极进行电解实验。
四种离子中的两种离子组成的电解质溶液若干种,可选用铁电极、铜电极、铂电极进行电解实验。
(5)欲使铁制品表面镀铜,应以_______ 为阳极,电解质溶液为_______ 。
(6)以铂作阳极电解某溶液时,溶液的碱性有明显增强,且溶液保澄清,电解时总反应的化学方程式为_______ 。
Ⅲ.铅蓄电池放电时:
(7)电解质溶液的pH不断_______ (增大、减小、不变);电池充电时,电池正极和电源的_______ (正极、负极)连接,电极反应式为_______ 。

(1)甲装置的名称是
(2)写出电极反应式:Pt极
(3)若乙中溶液不变,将其电极都换成铜电极,电键闭合一段时间后,乙中溶液的颜色
(4)若乙池溶液通电一段时间后,向所得的溶液中加入0.1mol的Cu(OH)2后恰好恢复到电解前的浓度。则电解过程中转移电子的数目为
II.由Cu2+、
 、Na+、
、Na+、 四种离子中的两种离子组成的电解质溶液若干种,可选用铁电极、铜电极、铂电极进行电解实验。
四种离子中的两种离子组成的电解质溶液若干种,可选用铁电极、铜电极、铂电极进行电解实验。(5)欲使铁制品表面镀铜,应以
(6)以铂作阳极电解某溶液时,溶液的碱性有明显增强,且溶液保澄清,电解时总反应的化学方程式为
Ⅲ.铅蓄电池放电时:
(7)电解质溶液的pH不断
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】I.某化学兴趣小组利用如图所示的装置研究有关电化学的相关知识。当闭合该装置的开关时,观察到电流表的指针发生了偏转,已知丙为电解精炼铜装置。请回答下列问题:
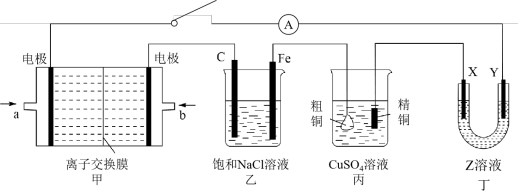
(1)若甲装置为甲醇(CH3OH)燃料电池,电解质溶液为KOH溶液,电极a上发生的电极反应式是___________ 。
(2)25℃,若乙装置中饱和NaCl溶液体积为500 mL,电路接通后一段时间,丙中精铜电极增重1.6 g,则此时乙装置中溶液pH为___________ (电解前后溶液体积变化忽略不计),阴极电极反应式为___________ ,欲使乙溶液复原需加入的物质是___________ (填名称)。
(3)若使用丁装置在铜牌上镀银,则铜牌应该与___________ (填“X”或“Y”)电极相连,Z溶液可选用___________ (填化学式)溶液。
II.纳米级Cu2O由于具有优良的催化性能而受到关注,采用甲醇燃料电池为电源,用离子交换膜控制电解液中的c(OH−)制备纳米Cu2O,其装置如图戊。
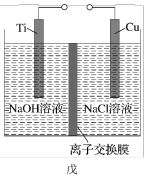
(4)装置戊中铜电极应连接甲醇燃料电池的___________ (填“正”或“负”)极,该电解池中离子交换膜为___________ (填“阴”或“阳”)离子交换膜。
(5)该电解池的阳极反应式为___________ 。

(1)若甲装置为甲醇(CH3OH)燃料电池,电解质溶液为KOH溶液,电极a上发生的电极反应式是
(2)25℃,若乙装置中饱和NaCl溶液体积为500 mL,电路接通后一段时间,丙中精铜电极增重1.6 g,则此时乙装置中溶液pH为
(3)若使用丁装置在铜牌上镀银,则铜牌应该与
II.纳米级Cu2O由于具有优良的催化性能而受到关注,采用甲醇燃料电池为电源,用离子交换膜控制电解液中的c(OH−)制备纳米Cu2O,其装置如图戊。

(4)装置戊中铜电极应连接甲醇燃料电池的
(5)该电解池的阳极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】电催化还原 是当今资源化利用二氧化碳的重点课题,常用的阴极材料有有机多孔电极材料、铜基复合电极材料等。
是当今资源化利用二氧化碳的重点课题,常用的阴极材料有有机多孔电极材料、铜基复合电极材料等。
(1)一种有机多孔电极材料(铜粉沉积在一种有机物的骨架上)电催化还原 的装置示意图如图-1所示。控制其他条件相同,将一定量的
的装置示意图如图-1所示。控制其他条件相同,将一定量的 通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如图-2所示。
通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如图-2所示。
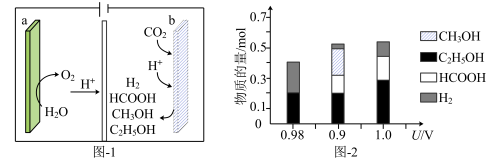
①电解前需向电解质溶液中持续通入过量 的原因是
的原因是___________ 。
②控制电压为0.8V,电解时转移电子的物质的量为___________ mol。
③科研小组利用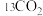 代替原有的
代替原有的 进行研究,其目的是
进行研究,其目的是___________ 。
(2)一种铜基复合电极材料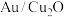 的制备方法:将一定量
的制备方法:将一定量 分散至水与乙醇的混合溶液中,向溶液中逐滴滴加
分散至水与乙醇的混合溶液中,向溶液中逐滴滴加 (一种强酸)溶液,搅拌一段时间后离心分离,得
(一种强酸)溶液,搅拌一段时间后离心分离,得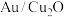 ,溶液呈蓝色。写出
,溶液呈蓝色。写出 还原
还原 的离子方程式:
的离子方程式:___________ 。
(3)金属Cu/La复合电极材料电催化还原CO₂制备甲醛和乙醇的可能机理如图-3所示。研究表明,在不同电极材料上形成中间体的部分反应活化能如图-4所示。
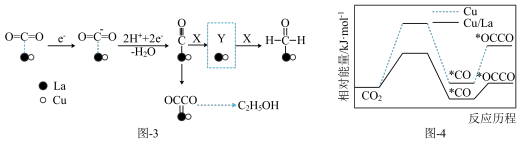
①X为___________ 。在答题卡上相应位置补充完整虚线框内Y的结构。_________
②与单纯的Cu电极相比,利用Cu/La复合电极材料电催化还原 的优点是
的优点是___________ 。
 是当今资源化利用二氧化碳的重点课题,常用的阴极材料有有机多孔电极材料、铜基复合电极材料等。
是当今资源化利用二氧化碳的重点课题,常用的阴极材料有有机多孔电极材料、铜基复合电极材料等。(1)一种有机多孔电极材料(铜粉沉积在一种有机物的骨架上)电催化还原
 的装置示意图如图-1所示。控制其他条件相同,将一定量的
的装置示意图如图-1所示。控制其他条件相同,将一定量的 通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如图-2所示。
通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如图-2所示。
①电解前需向电解质溶液中持续通入过量
 的原因是
的原因是②控制电压为0.8V,电解时转移电子的物质的量为
③科研小组利用
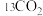 代替原有的
代替原有的 进行研究,其目的是
进行研究,其目的是(2)一种铜基复合电极材料
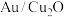 的制备方法:将一定量
的制备方法:将一定量 分散至水与乙醇的混合溶液中,向溶液中逐滴滴加
分散至水与乙醇的混合溶液中,向溶液中逐滴滴加 (一种强酸)溶液,搅拌一段时间后离心分离,得
(一种强酸)溶液,搅拌一段时间后离心分离,得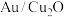 ,溶液呈蓝色。写出
,溶液呈蓝色。写出 还原
还原 的离子方程式:
的离子方程式:(3)金属Cu/La复合电极材料电催化还原CO₂制备甲醛和乙醇的可能机理如图-3所示。研究表明,在不同电极材料上形成中间体的部分反应活化能如图-4所示。

①X为
②与单纯的Cu电极相比,利用Cu/La复合电极材料电催化还原
 的优点是
的优点是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】如下图为相互串联的甲、乙两电解池。试回答:
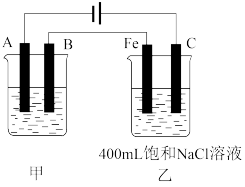
(1)若甲电解池利用电解原理在铁上镀银,则B是(填电极材料)___ ,电极反应为____________ , 甲中电解质溶液的溶质为__________ 。
(2)若甲电解池某极增重4.32g,则乙槽中Fe极上放出的气体在标准状况下的体积是__________ mL。
(3)若乙电解池中剩余溶液仍为400mL,则电解后所得溶液的pH等于__________ 。

(1)若甲电解池利用电解原理在铁上镀银,则B是(填电极材料)
(2)若甲电解池某极增重4.32g,则乙槽中Fe极上放出的气体在标准状况下的体积是
(3)若乙电解池中剩余溶液仍为400mL,则电解后所得溶液的pH等于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某研究性学习小组将下列装置如图连接,C、D、E、F、X、Y都是惰性电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:
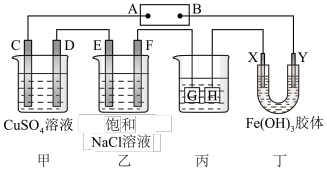
(1)电源A极的名称是________ 。
(2)甲装置中电解反应的总化学方程式为(电解质溶液是足量的):_______ 电解后若使电解质溶液复原需要加入适量的__________________
(3)如果收集乙装置中产生的气体,两种气体的体积比是(忽略气体的溶解)________ 。ClO2为一种黄绿色气体,是目前国际上公认的高效、广谱、快速安全的杀菌剂。制备ClO2的新工艺是电解法。若调控合适的电压可以利用乙装置制备ClO2,写出阳极产生ClO2的电极反应式__________ ClO2对污水中Fe2+、Mn2+、S2-、CN-等有明显去除效果,某工厂污水中含CN-,现用ClO2把CN-氧化成两种无毒气体,写出该反应的离子方程式:_____________ 。
(4)欲用丙装置给铜镀银,G应该是________ (填“铜”或“银”),电镀液的主要成分是________ (填化学式)。
(5)装置丁中的现象是_______ 。

(1)电源A极的名称是
(2)甲装置中电解反应的总化学方程式为(电解质溶液是足量的):
(3)如果收集乙装置中产生的气体,两种气体的体积比是(忽略气体的溶解)
(4)欲用丙装置给铜镀银,G应该是
(5)装置丁中的现象是
您最近一年使用:0次



