A~J 是中学化学常见的物质,它们之间的转化关系如下图所示 (部分反应条件、生成物已省略)。已知A是一种高熔点物质,D是一种红棕色固体。
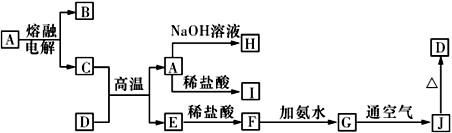
请回答下列问题:
(1)电解A物质的阴极电极反应式为________ ,C 与D在高温下反应,引发该反应需要加入的两种试剂是________________________ (填名称)。
(2)写出G→J 反应的实验现象与化学方程式:____________________________ ,________________________________ 。
(3)C 与NaOH溶液反应的离子方程式为________________________________ 。

请回答下列问题:
(1)电解A物质的阴极电极反应式为
(2)写出G→J 反应的实验现象与化学方程式:
(3)C 与NaOH溶液反应的离子方程式为
更新时间:2018-03-10 21:51:12
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】A~J分别表示中学化学中常见的一种物质,它们之间相互关系如图所示(部分反应物、生成物没有列出),且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。

请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素在周期表中的位置_________。
(2)写出反应①、⑤、⑥的化学方程式和反应④的离子方程式。
反应①:___________________________
反应⑤:___________________________
反应⑥:___________________________
反应④:__________________________。
(3)从能量变化的角度看,①、②、③反应中,ΔH<0的是_______(填序号)。

请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素在周期表中的位置_________。
(2)写出反应①、⑤、⑥的化学方程式和反应④的离子方程式。
反应①:___________________________
反应⑤:___________________________
反应⑥:___________________________
反应④:__________________________。
(3)从能量变化的角度看,①、②、③反应中,ΔH<0的是_______(填序号)。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】金属钒主要用于冶炼特种钢,被誉为“合金的维生素”。以富钒炉渣(其中的钒以 、
、 等形式存在,还有少量的
等形式存在,还有少量的 、
、 等)为原料提取金属钒的工艺流程如下图所示。
等)为原料提取金属钒的工艺流程如下图所示。
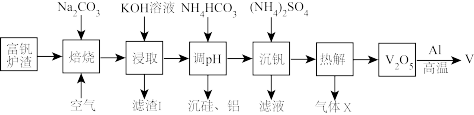
提示:钒有多种价态,其中 价最稳定。
价最稳定。
(1)“焙烧”是该流程中物质转化较为复杂的过程,其中二氧化硅发生的反应为_______ ,氧化铝转化为_______ (填产物名称),通入空气的主要作用是_______ 。
(2)气体X、滤渣1主要成分为_______ 、_______ (填写化学式)。
(3) 作为一种具有强氧化性的物质,在高温条件下可将
作为一种具有强氧化性的物质,在高温条件下可将 氧化为对应的高价氧化物,试写出
氧化为对应的高价氧化物,试写出 固体与
固体与 反应的化学方程式
反应的化学方程式_______ 。
(4) 在沉铝时发生反应的离子方程式为
在沉铝时发生反应的离子方程式为_______ 。
(5)金属铝与 高温下可得到金属钒,请写出反应的化学方程式
高温下可得到金属钒,请写出反应的化学方程式_______ 。
 、
、 等形式存在,还有少量的
等形式存在,还有少量的 、
、 等)为原料提取金属钒的工艺流程如下图所示。
等)为原料提取金属钒的工艺流程如下图所示。
提示:钒有多种价态,其中
 价最稳定。
价最稳定。(1)“焙烧”是该流程中物质转化较为复杂的过程,其中二氧化硅发生的反应为
(2)气体X、滤渣1主要成分为
(3)
 作为一种具有强氧化性的物质,在高温条件下可将
作为一种具有强氧化性的物质,在高温条件下可将 氧化为对应的高价氧化物,试写出
氧化为对应的高价氧化物,试写出 固体与
固体与 反应的化学方程式
反应的化学方程式(4)
 在沉铝时发生反应的离子方程式为
在沉铝时发生反应的离子方程式为(5)金属铝与
 高温下可得到金属钒,请写出反应的化学方程式
高温下可得到金属钒,请写出反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】请根据以下信息答题:
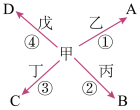
已知:I.图中,①②③④四个反应均为单质与单质在一定条件下的化合反应。
II.图中涉及的物质中除乙和A外均由短周期元素组成。
II. 丙与A在高温下反应能放出大量的热,生成B和乙,该反应能用于焊接钢轨。
IV.乙在甲中燃烧生成A,戊能在C中燃烧生成D和丁,C是一种常见的温室气体。且D中甲元素的质量分数为40%。
(1)请写出III对应的化学方程式:______ 。
(2)23.2gA溶于足量盐酸,得到的溶液与铜粉完全反应,至少需铜粉的质量为_____ 。
(3)丙与少量的NaOH溶液反应的离子方程式为______ 。
(4)C的电子式为___ ,它的空间结构是_____ 。

已知:I.图中,①②③④四个反应均为单质与单质在一定条件下的化合反应。
II.图中涉及的物质中除乙和A外均由短周期元素组成。
II. 丙与A在高温下反应能放出大量的热,生成B和乙,该反应能用于焊接钢轨。
IV.乙在甲中燃烧生成A,戊能在C中燃烧生成D和丁,C是一种常见的温室气体。且D中甲元素的质量分数为40%。
(1)请写出III对应的化学方程式:
(2)23.2gA溶于足量盐酸,得到的溶液与铜粉完全反应,至少需铜粉的质量为
(3)丙与少量的NaOH溶液反应的离子方程式为
(4)C的电子式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】硫酸铵焙烧浸出液水解制备偏钛酸 可回收钛。
可回收钛。
已知:i.一定条件下, 水解方程式:
水解方程式: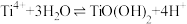
ⅱ.一定温度下: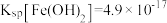 ;
;
I.水解制备偏钛酸:浸出液中含 、
、 等,先向其中加入还原铁粉,然后控制水解条件实现
等,先向其中加入还原铁粉,然后控制水解条件实现 水解制备偏钛酸。
水解制备偏钛酸。
(1)用化学用语表示 溶液呈酸性的原因
溶液呈酸性的原因_______ 。
(2)浸出液( )时:
)时:
① 转化为
转化为 沉淀需要的浓度为
沉淀需要的浓度为_______  ;
; 转化为
转化为 沉淀需要的浓度为
沉淀需要的浓度为_______  ;
;
②若杂质离子沉淀会降低钛水解率。从定量角度解释加入还原铁粉的目的_______ 。
(3)一定条件下,还原铁粉添加比对钛水解率的影响如图1所示。当还原铁粉添加比大于1时,钛水解率急剧下降,解释其原因_______ 。

已知:还原铁粉添加比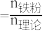 ;
;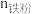 为还原铁粉添加量,
为还原铁粉添加量,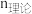 验为浸出液中
验为浸出液中 全部还原为
全部还原为 所需的还原铁粉理论量。
所需的还原铁粉理论量。
(4)一定条件下,温度对钛水解率的影响如图2所示。结合化学平衡移动原理解释钛水解率随温度升高而增大的原因_______ 。

Ⅱ.电解制备钛:偏钛酸煅烧得到二氧化钛( ),运用电化学原理在无水
),运用电化学原理在无水 熔盐电解质中电解
熔盐电解质中电解 得到海绵钛,装置如图3所示。
得到海绵钛,装置如图3所示。
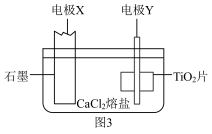
(5)电极X连接电源_______ (填“正”或“负”)极;写出电极Y上发生的电极反应式_______ 。
 可回收钛。
可回收钛。已知:i.一定条件下,
 水解方程式:
水解方程式: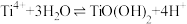
ⅱ.一定温度下:
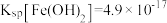 ;
;
I.水解制备偏钛酸:浸出液中含
 、
、 等,先向其中加入还原铁粉,然后控制水解条件实现
等,先向其中加入还原铁粉,然后控制水解条件实现 水解制备偏钛酸。
水解制备偏钛酸。(1)用化学用语表示
 溶液呈酸性的原因
溶液呈酸性的原因(2)浸出液(
 )时:
)时:①
 转化为
转化为 沉淀需要的浓度为
沉淀需要的浓度为 ;
; 转化为
转化为 沉淀需要的浓度为
沉淀需要的浓度为 ;
;②若杂质离子沉淀会降低钛水解率。从定量角度解释加入还原铁粉的目的
(3)一定条件下,还原铁粉添加比对钛水解率的影响如图1所示。当还原铁粉添加比大于1时,钛水解率急剧下降,解释其原因

已知:还原铁粉添加比
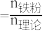 ;
;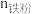 为还原铁粉添加量,
为还原铁粉添加量,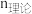 验为浸出液中
验为浸出液中 全部还原为
全部还原为 所需的还原铁粉理论量。
所需的还原铁粉理论量。(4)一定条件下,温度对钛水解率的影响如图2所示。结合化学平衡移动原理解释钛水解率随温度升高而增大的原因

Ⅱ.电解制备钛:偏钛酸煅烧得到二氧化钛(
 ),运用电化学原理在无水
),运用电化学原理在无水 熔盐电解质中电解
熔盐电解质中电解 得到海绵钛,装置如图3所示。
得到海绵钛,装置如图3所示。
(5)电极X连接电源
您最近一年使用:0次
【推荐2】金属铝有广泛的应用,有人对碳还原氧化铝制备铝进行了实验研究。在2.0 L真空密闭容器中稍过量石墨与1.0 mol Al2O3混合后加热,图1是体系压强随着加热时间变化的曲线图,图2是在不同的恒定温度下,反应达到平衡,冷却后容器内剩余固体中部分 含铝元素物质的物质的量随温度变化曲线图。

已知:1.01×105 Pa下Al熔点933 K,沸点2700 K;10 Pa下Al沸点低于1000 K,Al2O3和C沸点高于2000 K。
反应I:Al2O3(s)+3C(s) 2Al(s)+3CO(g) △H1=+1339.1 kJ·mol-1
2Al(s)+3CO(g) △H1=+1339.1 kJ·mol-1
反应II:2Al2O3(s)+9C(s) Al4C3(s)+6CO(g) △H2=+2249.5 kJ·mol-1
Al4C3(s)+6CO(g) △H2=+2249.5 kJ·mol-1
反应III:Al2O3(s)+Al4C3(s) 6Al(s)+3CO(g) △H3
6Al(s)+3CO(g) △H3
请回答下列问题:
(1)工业上电解法冶炼铝的化学方程式为___ 。
(2)△H3=___ 。
(3)图1中石墨与Al2O3混合物加热至150 min时容器内温度约为___ 。
(4)从反应自发性推测,实验室进行碳还原氧化铝制备铝的实验需要在真空容器中进行,可能的原因是___ 。
(5)由图2可得1650 K时,反应I的平衡常数K=___ 。
(6)下列说法不正确 的是___ 。
A.图1中约170 min后体系压强很快减小可能是反应I、II急剧发生,吸收了大量的热,容器内温度降低,导致反应I、II平衡向逆方向移动
B.图2显示约1650~1700 K之间是石墨与Al2O3反应制备Al的最佳温度
C.图2中T≥1700K时体系中一定还发生了其他副反应
D.综合分析可得,碳还原氧化铝制备铝比电解法成本更低,产率更高,适合大规模应用
(7)请在图3中画出温度在1450-1650 K之间2.0 L真空密闭容器中CO的浓度随温度变化曲线图___ 。


已知:1.01×105 Pa下Al熔点933 K,沸点2700 K;10 Pa下Al沸点低于1000 K,Al2O3和C沸点高于2000 K。
反应I:Al2O3(s)+3C(s)
 2Al(s)+3CO(g) △H1=+1339.1 kJ·mol-1
2Al(s)+3CO(g) △H1=+1339.1 kJ·mol-1反应II:2Al2O3(s)+9C(s)
 Al4C3(s)+6CO(g) △H2=+2249.5 kJ·mol-1
Al4C3(s)+6CO(g) △H2=+2249.5 kJ·mol-1反应III:Al2O3(s)+Al4C3(s)
 6Al(s)+3CO(g) △H3
6Al(s)+3CO(g) △H3请回答下列问题:
(1)工业上电解法冶炼铝的化学方程式为
(2)△H3=
(3)图1中石墨与Al2O3混合物加热至150 min时容器内温度约为
(4)从反应自发性推测,实验室进行碳还原氧化铝制备铝的实验需要在真空容器中进行,可能的原因是
(5)由图2可得1650 K时,反应I的平衡常数K=
(6)下列说法
A.图1中约170 min后体系压强很快减小可能是反应I、II急剧发生,吸收了大量的热,容器内温度降低,导致反应I、II平衡向逆方向移动
B.图2显示约1650~1700 K之间是石墨与Al2O3反应制备Al的最佳温度
C.图2中T≥1700K时体系中一定还发生了其他副反应
D.综合分析可得,碳还原氧化铝制备铝比电解法成本更低,产率更高,适合大规模应用
(7)请在图3中画出温度在1450-1650 K之间2.0 L真空密闭容器中CO的浓度随温度变化曲线图

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】金属单质及其化合物在工农业生产中应用广泛。
(1)用FeC13溶液腐蚀印刷电路板上的铜,向所得溶液中加入铁粉。对加入铁粉充分反应后的溶液分析合理的是_______ 。
a.若无固体剩余,则溶液中可能有Fe3+
b.若有固体存在,则溶液中一定有Cu2+和Fe2+
c.若溶液中有Cu2+,则可能有固体存在,且该固体中一定没有铁粉
d.若溶液中有Fe2+,则一定有固体存在
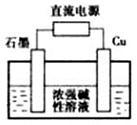
(2)Cu2O是一种半导体材料,制取Cu2O的电解池如图,则石墨电极接电源的_______ (填“正”或“负”)极,电解池工作时,Cu电极的电极反应式为______ ;电解后溶液pH______ (填“变大”、“变小”或“不变”)
(3)查阅资料可知:Cu2O为红色碱性氧化物,在酸性溶液中可发生反应:Cu2O+2H+=Cu+Cu2++H2O。请设计简单实验来验证某铜粉样品中是否有氧化亚铜:_____ 。
(1)用FeC13溶液腐蚀印刷电路板上的铜,向所得溶液中加入铁粉。对加入铁粉充分反应后的溶液分析合理的是
a.若无固体剩余,则溶液中可能有Fe3+
b.若有固体存在,则溶液中一定有Cu2+和Fe2+
c.若溶液中有Cu2+,则可能有固体存在,且该固体中一定没有铁粉
d.若溶液中有Fe2+,则一定有固体存在
(2)Cu2O是一种半导体材料,制取Cu2O的电解池如图,则石墨电极接电源的

(3)查阅资料可知:Cu2O为红色碱性氧化物,在酸性溶液中可发生反应:Cu2O+2H+=Cu+Cu2++H2O。请设计简单实验来验证某铜粉样品中是否有氧化亚铜:
您最近一年使用:0次



