下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。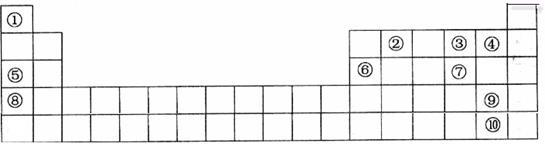
用化学符号回答下列问题:
(1)表中最活泼的金属与最活泼的非金属形成的物质是_____________ ;
(2)⑤、⑥、⑧的最高价水化物的碱性由强到弱的顺序是__________________________ ;
③、④、⑦氢化物稳定性由强到弱的顺序是___________________________________ ;
(3)①与⑤按原子个数1:1所成的化合物的电子式为__________________________ ;该化合物与水反应的离子方程式为________________________________________________ 。
(4)⑥号元素最高氧化物水化物与⑤号元素最高价氧化物水化物反应的离子方程式为__________________________ ;
(5)请设计一个实验方案,比较⑨、⑩的单质氧化性的强弱:________________ 。

用化学符号回答下列问题:
(1)表中最活泼的金属与最活泼的非金属形成的物质是
(2)⑤、⑥、⑧的最高价水化物的碱性由强到弱的顺序是
③、④、⑦氢化物稳定性由强到弱的顺序是
(3)①与⑤按原子个数1:1所成的化合物的电子式为
(4)⑥号元素最高氧化物水化物与⑤号元素最高价氧化物水化物反应的离子方程式为
(5)请设计一个实验方案,比较⑨、⑩的单质氧化性的强弱:
10-11高一下·安徽蚌埠·期中 查看更多[1]
(已下线)2010—2011学年安徽蚌埠二中第二学期高一期中考试化学试卷
更新时间:2016-12-09 01:40:18
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下图是元素周期表的部分,针对表中的10种元素,用元素符号或化学式回答相关问题:
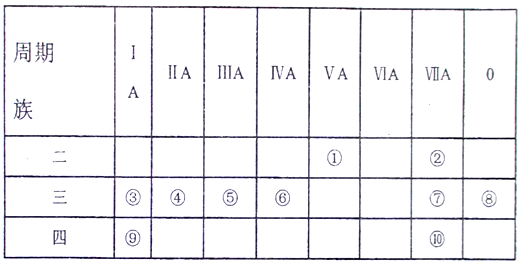
(1)画出④的阳离子结构示意图_________ 。
(2)这些元素中的最高价氧化物对应的水化物中,酸性最强的是______ ,碱性最强的是_____ 。
(3) 将⑦单质通入③与⑩组成的化合物的水溶液中,发生反应的离子方程式为_________ 。
(4)写出下列物质的电子式:
①形成的单质_________ ②与⑨形成的物质_________
用电子式表示④与⑦所组成物质的形成过程_______________ 。

(1)画出④的阳离子结构示意图
(2)这些元素中的最高价氧化物对应的水化物中,酸性最强的是
(3) 将⑦单质通入③与⑩组成的化合物的水溶液中,发生反应的离子方程式为
(4)写出下列物质的电子式:
①形成的单质
用电子式表示④与⑦所组成物质的形成过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。
回答下列问题:
(1)L的元素符号为________ ;M在元素周期表中的位置为________________ ;五种元素的原子半径从大到小的顺序是____________________ (用元素符号表示)。
(2) Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为___ ,B的分子式为____________ 。
(3)硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为_______ ,其最高价氧化物对应的水化物化学式为_______ 。
回答下列问题:
(1)L的元素符号为
(2) Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为
(3)硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】已知X、Y、Z、W四种元素是短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W是该元素所在周期原子半径最大的元素,W原子的质子数等于Y、Z原子的最外层电子数之和。Y与X形成的分子中有3个共价键,该分子中含有10个电子。Z原子最外层电子数是次外层电子数的3倍,试判断:
(1)Y和W两种元素的元素符号为Y________ ,W________ 。
(2)W2Z2的电子式为________________ 。
(3)①由X、Y、Z所形成的常见离子化合物是__________________ (写化学式)。
②该化合物与W的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为___________ 。
③化合物WY3的晶体结构中含有的化学键为________ (选填序号)。
A.只含离子键 B.只含共价键 C.既含离子键又含共价键
④X与W形成的化合物与水反应时,水作________ (填“氧化剂”或“还原剂”)。
(1)Y和W两种元素的元素符号为Y
(2)W2Z2的电子式为
(3)①由X、Y、Z所形成的常见离子化合物是
②该化合物与W的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为
③化合物WY3的晶体结构中含有的化学键为
A.只含离子键 B.只含共价键 C.既含离子键又含共价键
④X与W形成的化合物与水反应时,水作
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】现有8种短周期元素的性质,数据如下表所列:
回答下列问题:
(1)③的元素符号是______ ,⑧的元素名称是________ ,①在元素周期表中的位置 是______ 。
(2)在这 8 种元素中,最高价氧化物对应的水化物中,酸性最强的化合物其分子式是______ ;碱性最强的化合物电子式是_________ ,它属于_________ 化合物(填 “离子”或“共价”)。
(3)比较④和⑦的氢化物的稳定性强弱___________ (用化学式表示)。
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:________ 。
(5)写出单质③在单质①中燃烧的化学方程式__________ 。
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径 (10-10 m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(1)③的元素符号是
(2)在这 8 种元素中,最高价氧化物对应的水化物中,酸性最强的化合物其分子式是
(3)比较④和⑦的氢化物的稳定性强弱
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:
(5)写出单质③在单质①中燃烧的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,a、b、c…为部分元素。回答下列问题:
(1)请写出上述元素d3+的核外电子排布式____________________ ;
(2)请写出e元素的原子电子轨道表示式_____________ ;
(3)ya3分子的电子式________ ,其分子的空间构型是____________ ;
(4)b、e两种元素中,金属性较强的是_______ ,第一电离能大的是___________ (填元素符号);
(5)h的i形成hi2分子杂化类型是____________ ;fh32-的空间构型为_____________ 。
| a | |||||||||||||||||
| f | y | h | i | ||||||||||||||
| b | e | j | |||||||||||||||
| c | d | g | l | ||||||||||||||
(1)请写出上述元素d3+的核外电子排布式
(2)请写出e元素的原子电子轨道表示式
(3)ya3分子的电子式
(4)b、e两种元素中,金属性较强的是
(5)h的i形成hi2分子杂化类型是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.按要求回答下列问题:
(1)某粒子有1个原子核,核中有17个质子、20个中子,核外有18个电子,该粒子的化学符号是_ 。
(2)写出下列物质的电子式:
______ ,
______ ,
____ 。
(3)用电子式表示下列化合物的形成过程: :
:____ . :
:____ 。
Ⅱ.如图为元素周期表的一部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
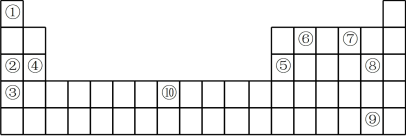
(1)②③④三种元素最高价氧化物对应水化物的碱性由强到弱的顺序是____ (填化学式)。
(2)10种元素中,原子半径最小的是______ (填序号)。
(3)元素⑦的简单氢化物与元素⑧的单质反应的离子方程式为______ 。
(4)元素②和⑤的最高价氧化物对应水化物相互反应的化学方程式为______ 。
(5)元素⑩的原子序数为______ ,其单质与元素⑦的简单氢化物在高温下反应的化学方程式为___ 。
(6)元素②的单质易溶于元素⑥与⑧形成的化合物中,所得溶液颜色为______ 色。
(1)某粒子有1个原子核,核中有17个质子、20个中子,核外有18个电子,该粒子的化学符号是
(2)写出下列物质的电子式:



(3)用电子式表示下列化合物的形成过程:
 :
: :
:Ⅱ.如图为元素周期表的一部分,列出了10种元素在元素周期表中的位置,试回答下列问题:

(1)②③④三种元素最高价氧化物对应水化物的碱性由强到弱的顺序是
(2)10种元素中,原子半径最小的是
(3)元素⑦的简单氢化物与元素⑧的单质反应的离子方程式为
(4)元素②和⑤的最高价氧化物对应水化物相互反应的化学方程式为
(5)元素⑩的原子序数为
(6)元素②的单质易溶于元素⑥与⑧形成的化合物中,所得溶液颜色为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】请回答下列问题。
(1)离子半径
___________  (填“>”或“<”)。
(填“>”或“<”)。
(2)C、O对应简单气态氢化物的稳定性强的是___________ (用化学式表示),该氢化物由固态变为气态克服的微粒间作用力有___________ 。
(3)O元素基态原子中能量最高的电子占据的原子轨道呈___________ 形。
(4)检验K元素常用的方法___________ 。
(5)元素C、H组成的化合物R是合成烈性炸药TNT的原料,写出R的结构简式___________ 。
(6)钛被誉为“21世纪的金属”,其化合物广泛用于国防、电讯器材、医疗器械和化工设备等领域。钛的某配合物可用于催化环烯烃聚合,其结构如图所示:
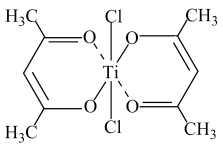
①钛的配位数为___________ 。
②该配合物中存在的化学键有___________ (填序号)。
a.离子键 b.配位键 c.金属键 d.共价键
(1)离子半径

 (填“>”或“<”)。
(填“>”或“<”)。(2)C、O对应简单气态氢化物的稳定性强的是
(3)O元素基态原子中能量最高的电子占据的原子轨道呈
(4)检验K元素常用的方法
(5)元素C、H组成的化合物R是合成烈性炸药TNT的原料,写出R的结构简式
(6)钛被誉为“21世纪的金属”,其化合物广泛用于国防、电讯器材、医疗器械和化工设备等领域。钛的某配合物可用于催化环烯烃聚合,其结构如图所示:

①钛的配位数为
②该配合物中存在的化学键有
a.离子键 b.配位键 c.金属键 d.共价键
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下图所示是元素周期表的一部分,根据①~⑧在周期表中的位置按题目要求回答:

(1)在元素①~⑧中,非金属性最强的元素是____________ (填元素名称)。
(2)在元素①~⑧中,原子半径最大的是___________ (填元素名称)。
(3)元素⑤⑥⑦的最高价氧化物对应水化物,按碱性从强到弱的顺序排列是____________ (用化学式表示)。
(4)用电子式表示元素①和⑧组成的化合物的形成过程____________ 。
(5)为验证ⅦA族部分元素非金属性的递变规律,设计了如图所示装置进行实验,请回答:

①仪器A的名称是_____ , A中发生反应的离子方程式是_______ 。
②棉花中浸有的NaOH溶液的作用是(用离子方程式表示)___________ 。
③为验证溴与碘非金属性强弱:通入少量⑧的单质,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到____ 。
④ⅦA族元素非金属性随元素核电荷数增加而逐渐减弱的原因:同主族元素从上到下,______ ,得电子能力逐渐减弱。

(1)在元素①~⑧中,非金属性最强的元素是
(2)在元素①~⑧中,原子半径最大的是
(3)元素⑤⑥⑦的最高价氧化物对应水化物,按碱性从强到弱的顺序排列是
(4)用电子式表示元素①和⑧组成的化合物的形成过程
(5)为验证ⅦA族部分元素非金属性的递变规律,设计了如图所示装置进行实验,请回答:

①仪器A的名称是
②棉花中浸有的NaOH溶液的作用是(用离子方程式表示)
③为验证溴与碘非金属性强弱:通入少量⑧的单质,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到
④ⅦA族元素非金属性随元素核电荷数增加而逐渐减弱的原因:同主族元素从上到下,
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】煤、石油、天然气目前依然是我国的主要能源。它们在氧气不足时会不完全燃烧:2C+O2 2CO,烃在氧气不足时也会不完全燃烧。
2CO,烃在氧气不足时也会不完全燃烧。
(1)完成下列方程式:2CxHy+___ O2 aCO +
aCO +___ CO2+___ H2O
(2)H原子的电子排布式是“1s1”,它未表明电子运动状态的方面是________ (填编号)。
a.电子层b.电子亚层c.电子云的伸展方向d.电子的自旋
(3)上述反应中半径最大的原子核外有______ 种能量不同的电子,写出其最外层轨道表示式______ 。
(4)石油和煤的综合利用中,下列说法错误的是______ 。
a.近年我国在新疆等地发现的石油矿藏超几十亿吨说明石油取之不尽
b.石油裂解目的是提高汽油的产量和质量
c.煤的液化和煤的气化都属于化学变化、石油的减压分馏属于物理变化
d.石油、煤、天然气都可以通过管道运输节约运输成本
(5)碳元素与氧元素的非金属性强弱的是C______ O(填“>”或“<”)。
(6)写出一个事实比较碳与硫非金属性强弱______ 。
(7)煤的气化是煤高效洁净利用的方向之一。在一定温度下的恒容密闭容器中建立下列化学平衡:C(s)+H2O(g)⇌CO(g)+H2(g)—Q,该反应的平衡常数表达式______ ,可认定该可逆反应在一定条件下已达到化学平衡状态的是______ 。(选填序号)
a.体系的压强不再发生变化b.生成n mol CO的同时生成n mol H2
c. v正(CO)=v逆(H2) d. 1mol H-H键断裂同时断裂1mol H-O键
 2CO,烃在氧气不足时也会不完全燃烧。
2CO,烃在氧气不足时也会不完全燃烧。(1)完成下列方程式:2CxHy+
 aCO +
aCO +(2)H原子的电子排布式是“1s1”,它未表明电子运动状态的方面是
a.电子层b.电子亚层c.电子云的伸展方向d.电子的自旋
(3)上述反应中半径最大的原子核外有
(4)石油和煤的综合利用中,下列说法错误的是
a.近年我国在新疆等地发现的石油矿藏超几十亿吨说明石油取之不尽
b.石油裂解目的是提高汽油的产量和质量
c.煤的液化和煤的气化都属于化学变化、石油的减压分馏属于物理变化
d.石油、煤、天然气都可以通过管道运输节约运输成本
(5)碳元素与氧元素的非金属性强弱的是C
(6)写出一个事实比较碳与硫非金属性强弱
(7)煤的气化是煤高效洁净利用的方向之一。在一定温度下的恒容密闭容器中建立下列化学平衡:C(s)+H2O(g)⇌CO(g)+H2(g)—Q,该反应的平衡常数表达式
a.体系的压强不再发生变化b.生成n mol CO的同时生成n mol H2
c. v正(CO)=v逆(H2) d. 1mol H-H键断裂同时断裂1mol H-O键
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】有四种短周期元素A、B、C、D,它们的核电荷数依次增大。A与C,B与D分别是同主族元素。B、D质子数之和是A、C质子数之和的2倍。这四种元素中A、C、D的单质均可在B的单质中燃烧。
(1)A的元素名称是________ ,C的元素符号是________ 。
(2)D元素位于元素周期表的第______ 周期第______ 族。
(3)C元素的单质在B的单质中燃烧的产物的化学式是________ 。
(1)A的元素名称是
(2)D元素位于元素周期表的第
(3)C元素的单质在B的单质中燃烧的产物的化学式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】七种短周期主族元素①~⑦,其原子序数依次增大,②元素是地壳中含量最多的,⑤元素为两性元素,④⑦两元素组成的化合物是我们日常生活必须的调味品,②和⑥元素的原子序数之和是①和④两元素原子序数之和的两倍。请用化学用语回答下列问题:
(1)③、⑤、⑥的简单离子半径由大到小的顺序为______________ 。
(2)⑥和⑦的最高价氧化物对应的水化物的酸性强弱为________ >_______ 。
(3)写出二氧化硅与含上述某种元素的酸反应的化学方程式_________________ 。
(4)由⑤和空气、海水构成的原电池中,其正极反应式为________________ 。
(5)由上述元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气体。

①写出D溶液与G反应的化学方程式________________________________ 。
②混合物X中的某物质不溶于水,但既能溶于酸又能溶于碱,写出能解释它在苛性钠溶液中发生反应的原因的电离方程式_________________________________ 。
③写出电解A溶液的离子方程式_______________________________ 。
(1)③、⑤、⑥的简单离子半径由大到小的顺序为
(2)⑥和⑦的最高价氧化物对应的水化物的酸性强弱为
(3)写出二氧化硅与含上述某种元素的酸反应的化学方程式
(4)由⑤和空气、海水构成的原电池中,其正极反应式为
(5)由上述元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气体。

①写出D溶液与G反应的化学方程式
②混合物X中的某物质不溶于水,但既能溶于酸又能溶于碱,写出能解释它在苛性钠溶液中发生反应的原因的电离方程式
③写出电解A溶液的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】表是现行中学化学教科书中元素周期表的一部分,除标出的元素外。表中的每个编号表示一种元素,请根据要求回答问题:____________ (填元素符号)。
(2)①与⑤两种元素相比较,原子半径较大的是______ (填元素符号);其非金属性较强的是 ______ (填元素符号);其最高正价氧化物水化物酸性较强的酸是_____ (填分子式)。
(3)⑥元素的单质可以用来制取漂白粉,其有效成分是______ (填化学式)。
③与⑥两种元素所形成化合物的电子式是____________ 。
(4)写出元素③的最高价氧化物对应的水化物与元素④的最高价氧化物对应的水化物相互反应的化学方程式________________________ 。
(5)②与⑥元素的氢化物的稳定性______ 大于______ (填分子式)。

(2)①与⑤两种元素相比较,原子半径较大的是
(3)⑥元素的单质可以用来制取漂白粉,其有效成分是
③与⑥两种元素所形成化合物的电子式是
(4)写出元素③的最高价氧化物对应的水化物与元素④的最高价氧化物对应的水化物相互反应的化学方程式
(5)②与⑥元素的氢化物的稳定性
您最近一年使用:0次



