按下列要求填空
①向碳酸氢钙溶液中加入少量氢氧化钠溶液的离子方程式:________________________ 。
氯化铝溶液与NaHCO3溶液混合的离子方程式:_____________________________________ 。
②在KClO3+ 6HCl =" KCl" + 3Cl2↑ + 3H2O的反应中,被氧化的氯原子与被还原的氯原子的物质的量之比是_______________ 。
③强酸性的未知无色溶液中可能含有大量的Cl-、S2-、NO3-、CO32-、NH4+、Cu2+、Fe3+、Ag+等,现已检出有Ag+,你认为其中____________ 离子还需要鉴定是否存在,请写出检验该离子的离子方程式_____________________ 。
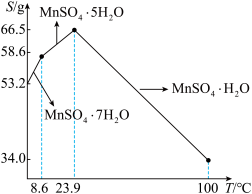
④某化合物的相对分子质量为m,在t℃时AmL该化合物的饱和溶液为Bg,将其蒸干后得到固体Cg。该化合物在t℃时的溶解度为____________ g,该饱和溶液中溶质的物质的量浓度为___________ mol/L。
①向碳酸氢钙溶液中加入少量氢氧化钠溶液的离子方程式:
氯化铝溶液与NaHCO3溶液混合的离子方程式:
②在KClO3+ 6HCl =" KCl" + 3Cl2↑ + 3H2O的反应中,被氧化的氯原子与被还原的氯原子的物质的量之比是
③强酸性的未知无色溶液中可能含有大量的Cl-、S2-、NO3-、CO32-、NH4+、Cu2+、Fe3+、Ag+等,现已检出有Ag+,你认为其中
④某化合物的相对分子质量为m,在t℃时AmL该化合物的饱和溶液为Bg,将其蒸干后得到固体Cg。该化合物在t℃时的溶解度为
10-11高三·河南新乡·阶段练习 查看更多[1]
(已下线)2012届河南省卫辉市第一中学高三第一次月考化学试卷
更新时间:2016-12-09 01:59:43
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下图为A、B两种固体物质的溶解度随温度变化的曲线。请回答:
(1)30 ℃时,A、B两物质的溶解度________ 。
(2)20 ℃时,A物质的溶解度________ B物质的溶解度(填“>”、“<”或“=”)。
(3)40 ℃时,将A、B各15 g分别加到均盛有50 g水的两只小烧杯中,充分搅拌后,________ 物质有剩余(填“A”或“B”)。
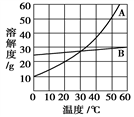
(4)现有50 ℃时A物质的不饱和溶液在不减少溶剂的情况下,欲使其变成饱和溶液,下列措施肯定不能实现的是________ (填序号)。
①降低温度 ②升高温度 ③加入A物质
(1)30 ℃时,A、B两物质的溶解度
(2)20 ℃时,A物质的溶解度
(3)40 ℃时,将A、B各15 g分别加到均盛有50 g水的两只小烧杯中,充分搅拌后,

(4)现有50 ℃时A物质的不饱和溶液在不减少溶剂的情况下,欲使其变成饱和溶液,下列措施肯定不能实现的是
①降低温度 ②升高温度 ③加入A物质
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】小明同学绘制了A、B、C三种固体物质的溶解度曲线如图。
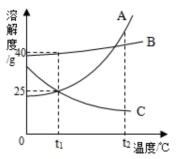
(1)曲线A和C的交点表示的含义是___________________ 。
(2)t1℃时将35 gB物质加入100 g水中,经充分溶解所形成的溶液是_________ (选填“饱和”或“不饱和”)溶液。

(1)曲线A和C的交点表示的含义是
(2)t1℃时将35 gB物质加入100 g水中,经充分溶解所形成的溶液是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】按要求书写下列反应的离子方程式:
(1)往澄清石灰水中通入少量二氧化碳:___________ 。
(2)锌粒投入稀H2SO4中:___________ 。
(3)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:___________ 。
(4)将过量的二氧化碳气体通入烧碱溶液中,然后将反应后的溶液分成二等份,分别加入与所得溶液溶质等物质的量的硝酸、氢氧化钙溶液。请分别写出发生反应的离子方程式:
①___________ 。
②___________ 。
(1)往澄清石灰水中通入少量二氧化碳:
(2)锌粒投入稀H2SO4中:
(3)向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性,请写出发生反应的离子方程式:
(4)将过量的二氧化碳气体通入烧碱溶液中,然后将反应后的溶液分成二等份,分别加入与所得溶液溶质等物质的量的硝酸、氢氧化钙溶液。请分别写出发生反应的离子方程式:
①
②
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】海水中含有80多种元素,是重要的物质资源宝库,同时海水具有强大的自然调节能力,为解决环境污染问题提供了广阔的空间。
(1)①已知不同 条件下,水溶液中碳元素的存在形态如下图所示。下列说法正确的是
条件下,水溶液中碳元素的存在形态如下图所示。下列说法正确的是___________ (填字母序号)。
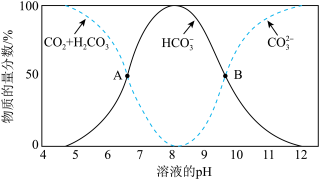
a. 时,溶液中含碳元素的微粒主要是
时,溶液中含碳元素的微粒主要是
b.A点,溶液中 和
和 浓度相同
浓度相同
c.当 时,溶液显酸性
时,溶液显酸性
②向上述 的水溶液中加入
的水溶液中加入 溶液,发生反应的离子方程式是
溶液,发生反应的离子方程式是___________ 。
(2)海水 稳定在7.9-8.4之间,可用于烟道气中
稳定在7.9-8.4之间,可用于烟道气中 和
和 的吸收剂。
的吸收剂。
①海水中含有的 可以吸收烟道气中的
可以吸收烟道气中的 同时为海水脱钙(海水中有钙离子),生产
同时为海水脱钙(海水中有钙离子),生产 。写出此反应的离子方程式:
。写出此反应的离子方程式:___________ 。
②海水中含有的 可用于吸收
可用于吸收 (二者1:1反应),该过程的离子反应方程式是
(二者1:1反应),该过程的离子反应方程式是___________ 。
(3)洗涤烟气后的海水呈酸性,需处理后再行排放。与新鲜海水混合同时鼓入大量空气排出部分 ,是一种处理的有效方式。此过程中,空气中的
,是一种处理的有效方式。此过程中,空气中的 将酸性海水中的
将酸性海水中的 氧化,该反应的离子方程式是
氧化,该反应的离子方程式是___________ 。
(1)①已知不同
 条件下,水溶液中碳元素的存在形态如下图所示。下列说法正确的是
条件下,水溶液中碳元素的存在形态如下图所示。下列说法正确的是
a.
 时,溶液中含碳元素的微粒主要是
时,溶液中含碳元素的微粒主要是
b.A点,溶液中
 和
和 浓度相同
浓度相同c.当
 时,溶液显酸性
时,溶液显酸性②向上述
 的水溶液中加入
的水溶液中加入 溶液,发生反应的离子方程式是
溶液,发生反应的离子方程式是(2)海水
 稳定在7.9-8.4之间,可用于烟道气中
稳定在7.9-8.4之间,可用于烟道气中 和
和 的吸收剂。
的吸收剂。①海水中含有的
 可以吸收烟道气中的
可以吸收烟道气中的 同时为海水脱钙(海水中有钙离子),生产
同时为海水脱钙(海水中有钙离子),生产 。写出此反应的离子方程式:
。写出此反应的离子方程式:②海水中含有的
 可用于吸收
可用于吸收 (二者1:1反应),该过程的离子反应方程式是
(二者1:1反应),该过程的离子反应方程式是(3)洗涤烟气后的海水呈酸性,需处理后再行排放。与新鲜海水混合同时鼓入大量空气排出部分
 ,是一种处理的有效方式。此过程中,空气中的
,是一种处理的有效方式。此过程中,空气中的 将酸性海水中的
将酸性海水中的 氧化,该反应的离子方程式是
氧化,该反应的离子方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求书写反应的化学方程式或离子方程式:
(1)用酸性(NH2)2CO水溶液吸收NOx,吸收过程中存在HNO2与(NH2)2CO生成N2和CO2的反应。写出该反应的化学方程式:__ 。
(2)为实现燃煤脱硫,向煤中加入浆状Mg(OH)2,使燃烧产生的SO2转化为稳定的镁化合物,写出该反应的化学方程式:__ 。
(3)45~50℃时,向CuCl悬浊液中持续通入空气得到Cu2(OH)2Cl2·3H2O,该反应的化学方程式为__ 。
(4)NaClO溶液与Ag反应的产物为AgCl、NaOH和O2,该反应的化学方程式为__ 。
(5)NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2,已知HCN、HOCN中N元素的化合价相同。写出发生反应的离子方程式:__ 。
(1)用酸性(NH2)2CO水溶液吸收NOx,吸收过程中存在HNO2与(NH2)2CO生成N2和CO2的反应。写出该反应的化学方程式:
(2)为实现燃煤脱硫,向煤中加入浆状Mg(OH)2,使燃烧产生的SO2转化为稳定的镁化合物,写出该反应的化学方程式:
(3)45~50℃时,向CuCl悬浊液中持续通入空气得到Cu2(OH)2Cl2·3H2O,该反应的化学方程式为
(4)NaClO溶液与Ag反应的产物为AgCl、NaOH和O2,该反应的化学方程式为
(5)NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2,已知HCN、HOCN中N元素的化合价相同。写出发生反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】为不断满足人民群众对美好生活的需要,水资源保护已经成为我国生态建设的重要领域。水处理技术目的在于使废水经过技术处理后达到再次使用或者排放的水质要求,被广泛应用于工业、农业、环保、餐饮等各个行业,与人们的日常生活密切相关。
I.某河道两旁甲、乙两厂排放的工业废水中,共含K+、Ag+、Fe3+、Cl-、OH-、NO 六种离子。其中甲厂含有三种离子且废水呈明显碱性,乙厂废水中则含有另外的三种离子。
六种离子。其中甲厂含有三种离子且废水呈明显碱性,乙厂废水中则含有另外的三种离子。
(1)乙厂废水中含有的三种离子为_______ 。
(2)将甲厂和乙厂的废水按适当的比例排放,混合后可使废水中的某些离子转化为沉淀,发生沉淀反应的离子方程式为Ag++Cl-=AgC1↓和_______ 。经沉淀后的废水主要含_______ (填化学式),可作为复合肥料,灌溉农田。
II.含氰废水(主要成分为NaCN)毒性大,排放前必须进行严格处理,碱性氯化法处理含氰废水的流程如下图所示。
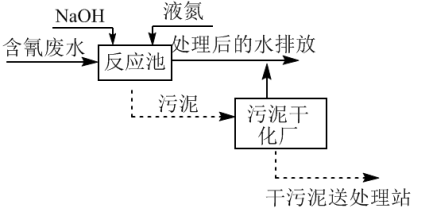
(3)CN-在反应池中转化为对环境友好的物质,且为空气的成分。补充完整反应池中发生反应的化学方程式:2NaCN+8NaOH+_______ Cl2=10NaCl + 2CO2↑+_______ +4H2O。
I.某河道两旁甲、乙两厂排放的工业废水中,共含K+、Ag+、Fe3+、Cl-、OH-、NO
 六种离子。其中甲厂含有三种离子且废水呈明显碱性,乙厂废水中则含有另外的三种离子。
六种离子。其中甲厂含有三种离子且废水呈明显碱性,乙厂废水中则含有另外的三种离子。(1)乙厂废水中含有的三种离子为
(2)将甲厂和乙厂的废水按适当的比例排放,混合后可使废水中的某些离子转化为沉淀,发生沉淀反应的离子方程式为Ag++Cl-=AgC1↓和
II.含氰废水(主要成分为NaCN)毒性大,排放前必须进行严格处理,碱性氯化法处理含氰废水的流程如下图所示。

(3)CN-在反应池中转化为对环境友好的物质,且为空气的成分。补充完整反应池中发生反应的化学方程式:2NaCN+8NaOH+
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】有一包固体粉末,由CaCO3、Na2SO4、KCl、Ba (NO3)2、CuSO4中的三种物质组成,取样品进行如下实验:
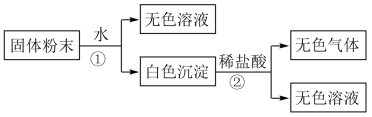
(1)写出实验过程中发生反应的化学方程式:__________________________ 。
(2)固体粉末中一定不存在的物质是________ ;一定存在的物质是_______ ;
(3)将固体粉末可能的组合填入下表:(可以不填满,也可以再补充。)
(4)请设计一个实验进一步确定混合物的组成,简述实验步骤、现象和结论。
______________________________________________________________

(1)写出实验过程中发生反应的化学方程式:
(2)固体粉末中一定不存在的物质是
(3)将固体粉末可能的组合填入下表:(可以不填满,也可以再补充。)
| 序号 | 化学式 |
| Ⅰ | |
| Ⅱ | |
| Ⅲ |
(4)请设计一个实验进一步确定混合物的组成,简述实验步骤、现象和结论。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】碘是生命体中的必需元素,请根据如下有关碘及其化合物的性质,回答下列问题:
(1)实验室中制取少量碘可采用如下方法:KI + CuSO4 → A (白色)↓+ K2SO4 + I2。
16.0 g CuSO4与过量KI反应后可得19.1 g 的A,写出A的化学式:____________ 。
工业生产中,可用智利硝石(含有NaIO3)为原料,与NaHSO3溶液反应后生成碘,写出此反应的离子方程式:____________________________________ 。
(2)单质碘与氟气反应可制得IF5,实验表明液态IF5具有一定的导电性,研究人员发现产生这一现象的可能原因在于IF5的自偶电离(如:2H2O H3O++OH-),生成的阳离子为IF4+,则阴离子为
H3O++OH-),生成的阳离子为IF4+,则阴离子为________ 。
(3)将单质碘与铝屑置于管式电炉中,隔绝空气加热至500℃得到棕色片状固体(AlI3),此固体溶于Na2CO3溶液可产生白色沉淀和气体。请写出AlI3和Na2CO3溶液反应的离子方程式:_____________________________________________ 。
(4)设计以下实验方案判断加碘食盐中碘的存在形式为I-、IO3-,或两者同时存在。请对以下试验方案进行预测和分析。
首先取试样加水溶解,分成三份试样:
①第一份试样加酸酸化,如果加淀粉溶液后试样溶液变蓝,说明试样中同时存在I-和IO3-,该过程反应的离子方程式为____________________________ 。
②第二份试样酸化后加_____ 溶液,如果加入淀粉溶液后试样溶液变蓝,说明试样中存在I-。
③第三份试样酸化后,如果直接使____________ 试纸变蓝,说明试样存在IO3-离子。
(1)实验室中制取少量碘可采用如下方法:KI + CuSO4 → A (白色)↓+ K2SO4 + I2。
16.0 g CuSO4与过量KI反应后可得19.1 g 的A,写出A的化学式:
工业生产中,可用智利硝石(含有NaIO3)为原料,与NaHSO3溶液反应后生成碘,写出此反应的离子方程式:
(2)单质碘与氟气反应可制得IF5,实验表明液态IF5具有一定的导电性,研究人员发现产生这一现象的可能原因在于IF5的自偶电离(如:2H2O
 H3O++OH-),生成的阳离子为IF4+,则阴离子为
H3O++OH-),生成的阳离子为IF4+,则阴离子为(3)将单质碘与铝屑置于管式电炉中,隔绝空气加热至500℃得到棕色片状固体(AlI3),此固体溶于Na2CO3溶液可产生白色沉淀和气体。请写出AlI3和Na2CO3溶液反应的离子方程式:
(4)设计以下实验方案判断加碘食盐中碘的存在形式为I-、IO3-,或两者同时存在。请对以下试验方案进行预测和分析。
首先取试样加水溶解,分成三份试样:
①第一份试样加酸酸化,如果加淀粉溶液后试样溶液变蓝,说明试样中同时存在I-和IO3-,该过程反应的离子方程式为
②第二份试样酸化后加
③第三份试样酸化后,如果直接使
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氮,磷,硫,氯等非金属元素的单质和化合物在工农业生产中有重要应用。回答下列问题:
(1)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸( ),反应的化学方程式为
),反应的化学方程式为_______ ,某厂废液中含有2%~5%的 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为
转化为 的是
的是_______ (填标号)。
A. B.
B. C.
C. D.浓
D.浓
(2) 及
及 均可将溶液中的
均可将溶液中的 还原为银,从而可用于化学镀银。
还原为银,从而可用于化学镀银。
① 是一种一元中强酸,
是一种一元中强酸, 为
为_______ (填“正盐”或“酸式盐”)
②利用 进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为
进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为_______ (填化学式)。
(3)硫代硫酸钠晶体 ,又名大苏打、海波,是一种用途非常广泛的化学试剂,遇酸立即分解,生成淡黄色沉淀,放出的气体能使品红溶液褪色,试写出硫代硫酸钠溶液与稀硫酸反应的离子方程式
,又名大苏打、海波,是一种用途非常广泛的化学试剂,遇酸立即分解,生成淡黄色沉淀,放出的气体能使品红溶液褪色,试写出硫代硫酸钠溶液与稀硫酸反应的离子方程式_______ 。
(4)氯气与氢氧化钠在70℃时反应,生成物中 和NaClO的物质的量之比为2:1的离子方程式为
和NaClO的物质的量之比为2:1的离子方程式为_______ 。
(1)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(
 ),反应的化学方程式为
),反应的化学方程式为 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为
转化为 的是
的是A.
 B.
B. C.
C. D.浓
D.浓
(2)
 及
及 均可将溶液中的
均可将溶液中的 还原为银,从而可用于化学镀银。
还原为银,从而可用于化学镀银。①
 是一种一元中强酸,
是一种一元中强酸, 为
为②利用
 进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为
进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为(3)硫代硫酸钠晶体
 ,又名大苏打、海波,是一种用途非常广泛的化学试剂,遇酸立即分解,生成淡黄色沉淀,放出的气体能使品红溶液褪色,试写出硫代硫酸钠溶液与稀硫酸反应的离子方程式
,又名大苏打、海波,是一种用途非常广泛的化学试剂,遇酸立即分解,生成淡黄色沉淀,放出的气体能使品红溶液褪色,试写出硫代硫酸钠溶液与稀硫酸反应的离子方程式(4)氯气与氢氧化钠在70℃时反应,生成物中
 和NaClO的物质的量之比为2:1的离子方程式为
和NaClO的物质的量之比为2:1的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】硫的多种化合物在工业中有重要的应用。
(1)连二亚硫酸钠(Na2S2O4)又称保险粉,是最适合木浆造纸的漂白剂,其水溶液性质不稳定,有极强的还原性。
①Na2S2O4中S元素的化合价为__________ 。
②Na2S2O4暴露于空气中易吸收氧气和水蒸气而变质,发生反应时,当氧化剂和还原剂的物质的量之比为l:2时,产物为___________ (填化学式)。
③将甲酸和NaOH溶液混合,再通入SO2气体,会得到保险粉,此时甲酸被氧化为CO2。该反应的化学方程式为____________________ 。
(2)铬会造成环境污染.某酸性废水中含有Cr2O72-,处理时可用焦亚硫酸钠(Na2S2O5)将Cr2O72-转化为毒性较低的Cr3+,再调节pH至8,使铬元素沉降,分离出污泥后测得废水中Cr3+浓度为0.52mg·L-1,达到排放标准。
①Na2S2O5参加反应的离子方程式为____________ 。
②处理后的废水中Cr3+的物质的量浓度为__________ mol·L-1。
(1)连二亚硫酸钠(Na2S2O4)又称保险粉,是最适合木浆造纸的漂白剂,其水溶液性质不稳定,有极强的还原性。
①Na2S2O4中S元素的化合价为
②Na2S2O4暴露于空气中易吸收氧气和水蒸气而变质,发生反应时,当氧化剂和还原剂的物质的量之比为l:2时,产物为
③将甲酸和NaOH溶液混合,再通入SO2气体,会得到保险粉,此时甲酸被氧化为CO2。该反应的化学方程式为
(2)铬会造成环境污染.某酸性废水中含有Cr2O72-,处理时可用焦亚硫酸钠(Na2S2O5)将Cr2O72-转化为毒性较低的Cr3+,再调节pH至8,使铬元素沉降,分离出污泥后测得废水中Cr3+浓度为0.52mg·L-1,达到排放标准。
①Na2S2O5参加反应的离子方程式为
②处理后的废水中Cr3+的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】用电弧法合成碳纳米管,常伴有大量杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式为:
2K2Cr2O7+3C+8H2SO4=2Cr2(SO4)3+2K2SO4+8H2O+3CO2↑。
(1)用双线桥法表示出电子转移方向和数目___________ 。
(2)此反应的氧化产物和还原产物的物质的量之比为___________ 。
(3)要使10mL1.0mol·L-1K2Cr2O7溶液被还原,至少要加入___________ mL2.0mol·L-1的H2SO4溶液,消耗C的质量为___________ g。
(4)若产生6.72LCO2(标准状况下)气体,该反应转移电子的物质的量为___________ mol。
(5)H2SO4在上述反应中表现出来的性质是___________。
2K2Cr2O7+3C+8H2SO4=2Cr2(SO4)3+2K2SO4+8H2O+3CO2↑。
(1)用双线桥法表示出电子转移方向和数目
(2)此反应的氧化产物和还原产物的物质的量之比为
(3)要使10mL1.0mol·L-1K2Cr2O7溶液被还原,至少要加入
(4)若产生6.72LCO2(标准状况下)气体,该反应转移电子的物质的量为
(5)H2SO4在上述反应中表现出来的性质是___________。
| A.酸性 | B.氧化性 | C.吸水性 | D.脱水性 |
您最近一年使用:0次