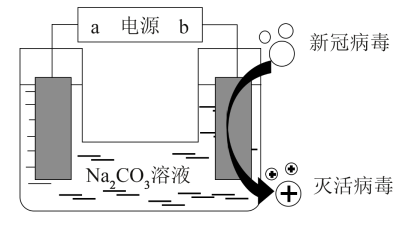
SO2和NOx是大气污染物的主要成分。防止空气污染,保卫“兰州蓝”是兰州市一项重要民生工程。利用下图所示装置(电极均为惰性电极)可以吸收SO2还可以用阴极排出的溶液吸收NO2。下列说法错误的是
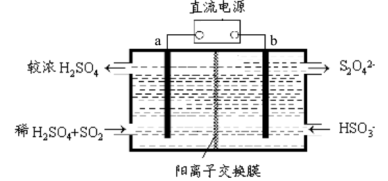

| A.电极a应连接电源的正极 |
| B.电极b上的电极反应式为2HSO3-+2e-+2H+=S2O42-+2H2O |
| C.反应过程中,H+从a极室流向b极室 |
| D.每吸收标况下22.4LSO2,在b极室生成2NA个S2O42- |
更新时间:2018-04-12 11:52:42
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】电化学原理在生产生活中广泛存在,下列说法正确的是
| A.钢铁发生析氢腐蚀或吸氧腐蚀时,负极都是铁失去电子变成Fe2+ |
| B.铁表面的镀锌层破损后,就完全失去了对铁的保护作用 |
| C.将地下金属管道连接直流电源的负极,属于牺牲阳极法 |
| D.电解精炼铜时,电解质溶液中铜离子浓度基本保持不变 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】利用 电池可将雾霾中的
电池可将雾霾中的 、
、 转化为硫酸铵,其回收利用装置如图所示。电池工作时的总反应为
转化为硫酸铵,其回收利用装置如图所示。电池工作时的总反应为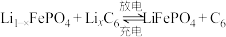 ,充放电时,
,充放电时, 在正极材料上嵌入或脱嵌,随之在石墨中发生了
在正极材料上嵌入或脱嵌,随之在石墨中发生了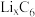 的生成与解离,下列有关说法错误的是
的生成与解离,下列有关说法错误的是

 电池可将雾霾中的
电池可将雾霾中的 、
、 转化为硫酸铵,其回收利用装置如图所示。电池工作时的总反应为
转化为硫酸铵,其回收利用装置如图所示。电池工作时的总反应为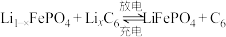 ,充放电时,
,充放电时, 在正极材料上嵌入或脱嵌,随之在石墨中发生了
在正极材料上嵌入或脱嵌,随之在石墨中发生了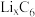 的生成与解离,下列有关说法错误的是
的生成与解离,下列有关说法错误的是
| A.转化为硫酸铵时,M与b相接,N与a相接 |
B.电池工作时,负极电极反应式为: |
C.该装置实际工作过程中需要在C处补充适量 |
D.理论上当消耗2.24L(标准状况) 时,电池中两池质量差改变2.8g 时,电池中两池质量差改变2.8g |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列方程式能正确解释相应事实的是
A.用Cu作电极电解饱和食盐水: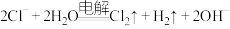 |
B.向饱和 溶液中通入 溶液中通入 气体: 气体: |
C.向碘化亚铁溶液中滴加少量氯气: |
D.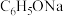 溶液中通入少量 溶液中通入少量 : : |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】资源再利用有利于保护生态,某实验小组研究电催化 和含氮废水(
和含氮废水( )在常温常压下合成尿素,即向一定浓度的
)在常温常压下合成尿素,即向一定浓度的 溶液中通入
溶液中通入 至饱和,在电极.上反应生成
至饱和,在电极.上反应生成 ,电解原理如图所示。下列有关说法错误的是
,电解原理如图所示。下列有关说法错误的是
 和含氮废水(
和含氮废水( )在常温常压下合成尿素,即向一定浓度的
)在常温常压下合成尿素,即向一定浓度的 溶液中通入
溶液中通入 至饱和,在电极.上反应生成
至饱和,在电极.上反应生成 ,电解原理如图所示。下列有关说法错误的是
,电解原理如图所示。下列有关说法错误的是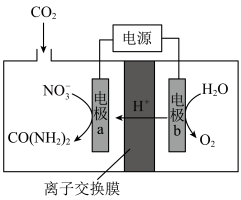
| A.离子交换膜为质子交换膜 |
| B.电极b发生氧化反应,为电解池的阳极 |
C.每消耗44g  ,理论上可在b处得到4mol ,理论上可在b处得到4mol  |
D.电极a的电极反应式为 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】现有阳离子交换膜、阴离子交换膜、石墨电极和如图所示的电解槽。利用氯碱工业中的离子交换膜技术原理,可通过电解 溶液来生产
溶液来生产 溶液和
溶液和 溶液。下列说法中不正确的是
溶液。下列说法中不正确的是

 溶液来生产
溶液来生产 溶液和
溶液和 溶液。下列说法中不正确的是
溶液。下列说法中不正确的是
A.阳极反应式为 |
| B.从A口流出的是硫酸溶液 |
C.b是阳离子交换膜,允许 通过 通过 |
D. 溶液从E口加入 溶液从E口加入 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列关于电解饱和食盐水过程的说法正确的是( )
| A.电解饱和食盐水的工厂可以生产盐酸 |
| B.与电源正极相连的电极区有NaOH生成 |
| C.与电源负极相连的电极上有氧气生成 |
D.电解饱和食盐水的过程中 浓度减小 浓度减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】现代技术可利用电解法制H2O2并用产生的H2O2处理废氨水,其装置如图所示。下列说法正确的是
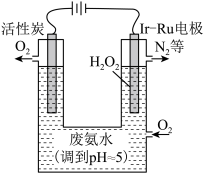

| A.该过程的总反应为:3H2O2+8H++4NH3•H2O=8H2O+N2↑+2NH4+ |
| B.Ir-Ru惰性电极有吸附O2的作用,该电极上的反应为:O2+2H++2e-=H2O2 |
| C.理论上电路中每转移6mol电子,最多可以处理NH3•H2O的物质的量为1mol |
| D.为了不影响H2O2的产量,需要向废氨水中加入适量硝酸调节溶液的pH约为5,则所得的废氨水溶液中c(NH4+)>c(NO3-) |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】用惰性电极电解物质的量浓度相同、体积比为1:3的CuSO4和NaCl的混合溶液,不可能发生的反应式
| A.2Cu2++2H2O电解2Cu+4H++O2↑ |
| B.Cu2++2Cl-电解Cu+Cl2↑ |
| C.2Cl-+2H2O电解2OH-+H2↑+Cl2↑ |
| D.2H2O电解2H2↑+O2↑ |
您最近半年使用:0次