在下列物质转化中,A是一种正盐,D的相对分子质量比C的相对分子质量大16,E是酸,当X无论是强酸还是强碱时,都有如下的转化关系:
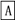
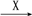
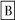
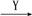
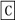
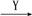
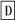
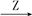
当X是强酸时,A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E均含另外同一种元素。请回答:
(1)A是________ ,Y是________ ,Z是________ 。
(2)当X是强酸时,B是________ E是________ 。写出B生成C的化学方程式:_________________ 。写出C生成D的化学方程式:__________________ 。
(3)当X是强碱时,B是________ E是________ 。
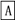
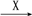
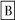
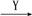
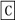
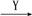
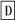
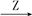
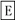
当X是强酸时,A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E均含另外同一种元素。请回答:
(1)A是
(2)当X是强酸时,B是
(3)当X是强碱时,B是
更新时间:2018-04-24 19:49:46
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】现有3种化合物A、B、C均含短周期元素R,其转化关系如下图所示。
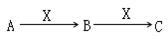
(1)若A由第三周期2种元素组成。常温下,0.1mol/L X溶液的pH=13,则R在周期中的位置是___________ 。X中阴离子的电子式是_________ ,B转化为C的离子方程式是__________ 。
(2)若常温下A、B、C、X均为气态物质,1mol A中含有共价键的数目约为1.806×1024,X为单质,A与X反应生成B的化学方程式是___________ ;在一定条件下,A可与C反应消除C对大气的污染,该反应的化学方程式是____________ 。
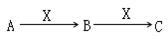
(1)若A由第三周期2种元素组成。常温下,0.1mol/L X溶液的pH=13,则R在周期中的位置是
(2)若常温下A、B、C、X均为气态物质,1mol A中含有共价键的数目约为1.806×1024,X为单质,A与X反应生成B的化学方程式是
您最近一年使用:0次
【推荐2】有甲、乙、丙、丁、戊五种短周期元素,原子序数依次增大,其常见化合价依次为+1、-2、+1、+3、-1。它们形成的物质间的转化关系如下图所示。常温下用惰性电极电解(有阳离子交换膜) 的A溶液。
的A溶液。
(1)己元素与丙元素同主族,比丙原子多2个电子层,则己的原子序数为________ ;推测相同条件下丙、己单质分别与水反应剧烈程度的依据是__________________________________________________ 。
(2)甲、乙、戊按原子个数比1︰1︰1形成的化合物Y具有漂白性,其电子式为_______________ 。
(3)上图转化关系中不属于氧化还原反应的有(填编号)_______ 。
(4)接通如图电路片刻后,向烧杯中滴加一种试剂即可检验铁电极被腐蚀,此反应的离子方程式为_____________________ 。___________ ;反应②的离子方程式为_________
(6)若上图中各步反应均为恰好完全转化,则混合物X中含有的物质(除水外)有___________
 的A溶液。
的A溶液。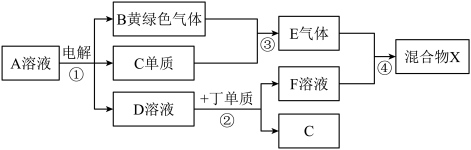
(1)己元素与丙元素同主族,比丙原子多2个电子层,则己的原子序数为
(2)甲、乙、戊按原子个数比1︰1︰1形成的化合物Y具有漂白性,其电子式为
(3)上图转化关系中不属于氧化还原反应的有(填编号)
(4)接通如图电路片刻后,向烧杯中滴加一种试剂即可检验铁电极被腐蚀,此反应的离子方程式为

(6)若上图中各步反应均为恰好完全转化,则混合物X中含有的物质(除水外)有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】各物质间的转化关系如下图所示,请完成下列空白。

(1)写出D和F的化学式:D________ ;F ________ 。
(2)写出E转变成F的化学方程式:________________________ 。
(3)向G溶液中加入A,写出反应的离子方程式:________________________ ;向B溶液中通入 ,写出反应的离子方程式:
,写出反应的离子方程式:________________________ 。
(4)证明某溶液中不含 ,而可能含有
,而可能含有 ,进行如下实验操作的最佳顺序为
,进行如下实验操作的最佳顺序为
①加入足量氯水 ②加入足量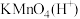 溶液 ③加入少量
溶液 ③加入少量 溶液
溶液
(5)A和水蒸气反应的化学方程式为________________________ 。

(1)写出D和F的化学式:D
(2)写出E转变成F的化学方程式:
(3)向G溶液中加入A,写出反应的离子方程式:
 ,写出反应的离子方程式:
,写出反应的离子方程式:(4)证明某溶液中不含
 ,而可能含有
,而可能含有 ,进行如下实验操作的最佳顺序为
,进行如下实验操作的最佳顺序为 ①加入足量氯水 ②加入足量
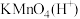 溶液 ③加入少量
溶液 ③加入少量 溶液
溶液| A.①③ | B.③② | C.③① | D.①②③ |
您最近一年使用:0次
【推荐1】硫代硫酸钠(Na2S2O3)是重要的化工原料易溶于水,在中性或碱性环境下稳定,在酸性溶液水,分解产生S、SO2。
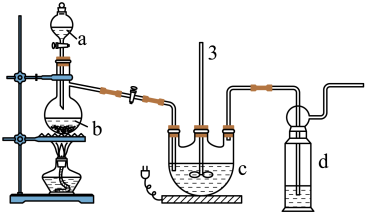
Ⅰ.Na2S2O3的制备。工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得,实验室模拟该工业过程的装置如图所示,其C中试剂为Na2S和Na2SO3的混合液。
(1)b中反应的离子方程式为_____ 。
(2)反应开始后,c中先有浑浊产生,后又变澄清。此浑浊物是_____ 。
(3)为了保证硫代硫酸钠的产量,实验中通入的SO2,不能过量,原因是_____ 。
(4)制备得到的Na2S2O3中可能含有Na2SO3、Na2SO4等杂质。设计实验,检测产品中是否存在Na2SO4:取少量产品_____ 。
Ⅱ.探究Na2S2O3与金属阳离子的氧化还原反应。
资料:ⅰ.Fe3++3S2O
 Fe(S2O3)
Fe(S2O3) (紫黑色)
(紫黑色)
ⅱ.Ag2S2O3为白色沉淀,Ag2S2O3可溶于过量的S2O
(5)根据实验①的现象,初步判断最终Fe3+被S2O 还原为Fe2+,通过
还原为Fe2+,通过_____ (填操作、试剂和现象),进一步证实生成了Fe2+。从化学反应速率和平衡的角度解释实验Ⅰ的现象:_____ 。
(6)同浓度氧化性:Ag+>Fe3+。实验②中Ag+未发生氧化还原反应的原因是_____ 。
(7)进一步探究Ag+和S2O 反应。
反应。
实验③中白色絮状沉淀最后变为黑色沉淀(Ag2S)的化学方程式如下,填入合适的物质和系数:_____ 。
Ag2S2O3+_____=Ag2S+_____
(8)根据以上实验,Na2S2O3与金属阳离子发生氧化还原反应和_____ 有关(写出两条)。

Ⅰ.Na2S2O3的制备。工业上可用反应:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得,实验室模拟该工业过程的装置如图所示,其C中试剂为Na2S和Na2SO3的混合液。
(1)b中反应的离子方程式为
(2)反应开始后,c中先有浑浊产生,后又变澄清。此浑浊物是
(3)为了保证硫代硫酸钠的产量,实验中通入的SO2,不能过量,原因是
(4)制备得到的Na2S2O3中可能含有Na2SO3、Na2SO4等杂质。设计实验,检测产品中是否存在Na2SO4:取少量产品
Ⅱ.探究Na2S2O3与金属阳离子的氧化还原反应。
资料:ⅰ.Fe3++3S2O

 Fe(S2O3)
Fe(S2O3) (紫黑色)
(紫黑色)ⅱ.Ag2S2O3为白色沉淀,Ag2S2O3可溶于过量的S2O

| 装置 | 编号 | 试剂X | 实验现象 |
 | ① | Fe(NO3)3溶液 | 混合后溶液先变成紫黑色,30s后溶液几乎变为无色 |
| ② | AgNO3溶液 | 先生成白色絮状沉淀,振荡后,沉淀溶解,得到无色溶液 |
(5)根据实验①的现象,初步判断最终Fe3+被S2O
 还原为Fe2+,通过
还原为Fe2+,通过(6)同浓度氧化性:Ag+>Fe3+。实验②中Ag+未发生氧化还原反应的原因是
(7)进一步探究Ag+和S2O
 反应。
反应。| 装置 | 编号 | 试剂X | 实验现象 |
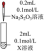 | ② | AgNO3溶液 | 先生成白色絮状沉淀,沉淀很快变成黄色、棕色,最后为黑色沉淀。 |
Ag2S2O3+_____=Ag2S+_____
(8)根据以上实验,Na2S2O3与金属阳离子发生氧化还原反应和
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】某黑色物质甲只含两种元素,为探究物质甲的组成和性质,设计并完成如下实验。其中气态氢化物乙在标况下的密度为 1.518 g·L-1,甲和乙中相同元素的化合价相同。

(1)甲的组成元素_____________ 。
(2)写出甲与足量浓盐酸反应的离子方程式______________ 。
(3)气体乙在过量空气中充分燃烧后,再将混合气体通入BaCl2溶液,出现白色沉淀。写出该过程中总反应的离子方程式_________________ 。

(1)甲的组成元素
(2)写出甲与足量浓盐酸反应的离子方程式
(3)气体乙在过量空气中充分燃烧后,再将混合气体通入BaCl2溶液,出现白色沉淀。写出该过程中总反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】物质的类别和核心元素的化合价是研究物质性质的两个角度。请根据图所示回答下列问题:

(1)X与Y反应可生成淡黄色固体,反应的化学方程式____________________ 。
(2)欲制备Na2S2O3,从氧化还原角度分析,下列选项中合理的反应物是______ (填序号)。
a.Na2SO3与S b.Na2S与S
c.SO2与Na2SO4 d.Na2SO3与Na2SO4
(3)7.7g锌镁合金与一定量浓硫酸恰好完全反应,生成SO2与H2的混合气体3.36L(标准状况),反应中转移的电子的物质的量为___________ 。
(4)处理SO2废气的一种工艺如图所示:
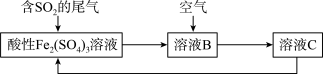
①SO2和酸性Fe2(SO4)3溶液反应的离子方程式是________________________ 。
②溶液B与空气发生反应生成溶液C,其中氧化剂是______________ 。
③推断Fe3+、O2和SO42-的氧化性由强到弱的顺序是______________ 。

(1)X与Y反应可生成淡黄色固体,反应的化学方程式
(2)欲制备Na2S2O3,从氧化还原角度分析,下列选项中合理的反应物是
a.Na2SO3与S b.Na2S与S
c.SO2与Na2SO4 d.Na2SO3与Na2SO4
(3)7.7g锌镁合金与一定量浓硫酸恰好完全反应,生成SO2与H2的混合气体3.36L(标准状况),反应中转移的电子的物质的量为
(4)处理SO2废气的一种工艺如图所示:

①SO2和酸性Fe2(SO4)3溶液反应的离子方程式是
②溶液B与空气发生反应生成溶液C,其中氧化剂是
③推断Fe3+、O2和SO42-的氧化性由强到弱的顺序是
您最近一年使用:0次



