某些化学键的键能如下表所示(单位kJ·mol-1):
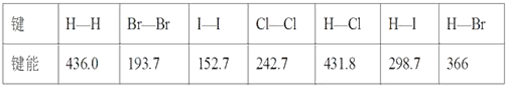
(1)1 mol H2在2 mol Cl2中燃烧,放出的热量为____ kJ。
(2)在一定条件下,1 mol H2与足量的Cl2、Br2、I2分别反应,放出热量由多到少的是________ 。
A.Cl2>Br2>I2 B.I2>Br2>Cl2
预测1 mol H2在足量F2中燃烧比在足量Cl2中燃烧放热________________ (填“多”或“少”)。

(1)1 mol H2在2 mol Cl2中燃烧,放出的热量为
(2)在一定条件下,1 mol H2与足量的Cl2、Br2、I2分别反应,放出热量由多到少的是
A.Cl2>Br2>I2 B.I2>Br2>Cl2
预测1 mol H2在足量F2中燃烧比在足量Cl2中燃烧放热
更新时间:2018-05-02 02:32:19
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。该反应进行过程中能量的变化(单位为kJ·mol-1)如图所示。

请回答下列问题:
(1)观察图象可知上述反应过程中,断裂反应物中的化学键吸收的总能量_____ (填“大于”“小于”或“等于”)形成生成物中的化学键释放的总能量。
(2)甲醇的结构类似于乙醇,试写出甲醇的结构式:______ 。甲醇分子中的化学键类型是______ (填“离子键“共价键”)。
(3)科研人员开发出一种新型甲醇燃料电池。其电解质溶液是KOH溶液,在该电池的负极发生反应的物质是________ ,发生的是________ (填"氧化"或"还原")反应。
(4)欲使合成甲醇的化学反应速率加快,请写出两条措施:________ ;

请回答下列问题:
(1)观察图象可知上述反应过程中,断裂反应物中的化学键吸收的总能量
(2)甲醇的结构类似于乙醇,试写出甲醇的结构式:
(3)科研人员开发出一种新型甲醇燃料电池。其电解质溶液是KOH溶液,在该电池的负极发生反应的物质是
(4)欲使合成甲醇的化学反应速率加快,请写出两条措施:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】2021年9月7日11时01分,长征四号丙遥四十运载火箭在太原卫星发射中心点火升空,成功将高光谱观测卫星(又名高分五号02星)送入预定轨道。该星将全面提升我国大气、水体、陆地的高光谱观测能力,满足我国在环境综合监测等方面的迫切需求。该系列火箭各级全部使用 和偏二甲肼(
和偏二甲肼( )作推进剂。
)作推进剂。
Ⅰ.完成下列问题
(1) 与偏二甲肼燃烧产物只有
与偏二甲肼燃烧产物只有 、
、 、
、 ,并放出大量热,已知10.0g液态偏二甲肼与液态
,并放出大量热,已知10.0g液态偏二甲肼与液态 完全燃烧可放出425kJ热量,该反应的热化学方程式为
完全燃烧可放出425kJ热量,该反应的热化学方程式为___________ 。
Ⅱ.目前火箭推进剂中较普遍的组合是肼( )和
)和 ,两者反应生成
,两者反应生成 和水蒸气。已知:
和水蒸气。已知:
①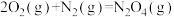

②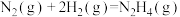

③

(2) 和
和 反应的热化学方程式为
反应的热化学方程式为___________ 。
(3) 和
和 可作为火箭推进剂的主要原因是
可作为火箭推进剂的主要原因是___________ 。
(4)试用化学反应能量图表示该反应过程中能量的变化___________ 。
(5)已知相关反应的化学键键能数据如表所示:
则使1mol 分子中化学键完全断裂时需要吸收的能量是
分子中化学键完全断裂时需要吸收的能量是___________ kJ。
(6)有人认为若用氟气代替 作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
已知:


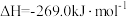
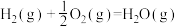
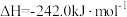
①写出肼和氟气反应的热化学方程式:___________ 。
②尽管氟气与肼反应释放的能量更大,但是氟气至今未被应用在火箭上,主要的原因是___________ 。
 和偏二甲肼(
和偏二甲肼( )作推进剂。
)作推进剂。Ⅰ.完成下列问题
(1)
 与偏二甲肼燃烧产物只有
与偏二甲肼燃烧产物只有 、
、 、
、 ,并放出大量热,已知10.0g液态偏二甲肼与液态
,并放出大量热,已知10.0g液态偏二甲肼与液态 完全燃烧可放出425kJ热量,该反应的热化学方程式为
完全燃烧可放出425kJ热量,该反应的热化学方程式为Ⅱ.目前火箭推进剂中较普遍的组合是肼(
 )和
)和 ,两者反应生成
,两者反应生成 和水蒸气。已知:
和水蒸气。已知:①
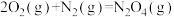

②
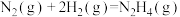

③


(2)
 和
和 反应的热化学方程式为
反应的热化学方程式为(3)
 和
和 可作为火箭推进剂的主要原因是
可作为火箭推进剂的主要原因是(4)试用化学反应能量图表示该反应过程中能量的变化
(5)已知相关反应的化学键键能数据如表所示:
| 化学键 | N—H | N—N | N≡N | O—H |
| E/(kJ/mol) | 390 | 190 | 946 | 460 |
 分子中化学键完全断裂时需要吸收的能量是
分子中化学键完全断裂时需要吸收的能量是(6)有人认为若用氟气代替
 作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。已知:



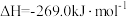
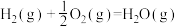
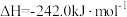
①写出肼和氟气反应的热化学方程式:
②尽管氟气与肼反应释放的能量更大,但是氟气至今未被应用在火箭上,主要的原因是
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】氢气是一种清洁能源,氢气的制取是氢能源利用领域的研究热点;氢气也是重要的化工原料。
(1)纳米级的Cu2O可作为太阳光分解水的催化剂。一定温度下,在2L密闭容器中加入纳米级Cu2O并通入0.10mol水蒸气发生反应:2H2O(g) 2H2(g)+O2(g) ΔH=+484 kJ·mol-1,不同时段产生O2的量见表格:
2H2(g)+O2(g) ΔH=+484 kJ·mol-1,不同时段产生O2的量见表格:
上述反应过程中能量转化形式为光能转化为____ 能,达平衡过程中至少需要吸收光能___ kJ(保留三位小数)。
(2)氢气是合成氨工业的原料,合成塔中每产生2 molNH3,放出92.2kJ热量。已知:

则1 molN—H键断裂吸收的能量约等于_____ 。
(1)纳米级的Cu2O可作为太阳光分解水的催化剂。一定温度下,在2L密闭容器中加入纳米级Cu2O并通入0.10mol水蒸气发生反应:2H2O(g)
 2H2(g)+O2(g) ΔH=+484 kJ·mol-1,不同时段产生O2的量见表格:
2H2(g)+O2(g) ΔH=+484 kJ·mol-1,不同时段产生O2的量见表格:| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
上述反应过程中能量转化形式为光能转化为
(2)氢气是合成氨工业的原料,合成塔中每产生2 molNH3,放出92.2kJ热量。已知:

则1 molN—H键断裂吸收的能量约等于
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】卤素单质及其化合物在生产、生活、化工、医药、材料等领域中有着非常广泛的应用。回答下列问题:
(1)基态Br原子的价层电子轨道表示式为__________ 。
(2)下列现象中,不能用“相似相溶”原理解释的是__________(填序号)。
(3)卤族元素除F元素外,Cl、Br、I均可形成多种含氧酸根,① ;②
;②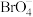 ;③
;③ 中键角最大的是
中键角最大的是__________ (填序号)。
(4)光气( )在有机合成中常作氯化剂,分子中所有原子均满足8电子稳定结构,
)在有机合成中常作氯化剂,分子中所有原子均满足8电子稳定结构, 分子中
分子中 键和
键和 键的个数比为
键的个数比为__________ 。
(5)请在下图含溴有机物的结构简式中,用星号(*)标出含有的手性碳原子__________ 。
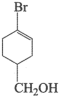
(6)已知:羧酸的酸性可用 的数值来衡量。室温下,
的数值来衡量。室温下, ;
; ,依据数据分析,酸性:
,依据数据分析,酸性:
__________  (填“>”“<”或“=”),请从键的极性角度解释原因
(填“>”“<”或“=”),请从键的极性角度解释原因__________ 。
(1)基态Br原子的价层电子轨道表示式为
(2)下列现象中,不能用“相似相溶”原理解释的是__________(填序号)。
A.HCl易溶于 | B. 易溶于NaOH溶液 易溶于NaOH溶液 |
C. 易溶于 易溶于 | D. 易溶于 易溶于 |
 ;②
;②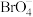 ;③
;③ 中键角最大的是
中键角最大的是(4)光气(
 )在有机合成中常作氯化剂,分子中所有原子均满足8电子稳定结构,
)在有机合成中常作氯化剂,分子中所有原子均满足8电子稳定结构, 分子中
分子中 键和
键和 键的个数比为
键的个数比为(5)请在下图含溴有机物的结构简式中,用星号(*)标出含有的手性碳原子

(6)已知:羧酸的酸性可用
 的数值来衡量。室温下,
的数值来衡量。室温下, ;
; ,依据数据分析,酸性:
,依据数据分析,酸性:
 (填“>”“<”或“=”),请从键的极性角度解释原因
(填“>”“<”或“=”),请从键的极性角度解释原因
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ.已知氢分子的形成过程示意图如图所示,请据图回答问题。

(1)H—H键的键长为___________ ,①~⑤中,体系能量由高到低的顺序是___________ 。
(2)下列说法中正确的是___________ (填字母)。
A.氢分子中含有一个π键
B.由①到④,电子在核间出现的概率增大
C.由④到⑤,必须消耗外界的能量
D.氢分子中含有一个极性共价键
Ⅱ.几种常见化学键的键能如下表所示。
请回答下列问题:
(1)试比较Si—C键与Si—Si键的键能大小:X_______ (填“>”“<”或“=”)226kJ·mol-1。
(2)H2被认为是21世纪人类最理想的燃料,而又有科学家提出硅是“21世纪的能源”“未来的石油”等观点。结合Ⅰ中图象,试计算每千克H2燃烧(生成水蒸气)放出的热量约为___________ ;每摩尔硅完全燃烧放出的热量约为________ (已知1molSi中含有2molSi—Si键,1molSiO2中含有4molSi—O键)。

(1)H—H键的键长为
(2)下列说法中正确的是
A.氢分子中含有一个π键
B.由①到④,电子在核间出现的概率增大
C.由④到⑤,必须消耗外界的能量
D.氢分子中含有一个极性共价键
Ⅱ.几种常见化学键的键能如下表所示。
| 化学键 | Si—O | H—O | O==O | Si—Si | Si—C |
| 键能/kJ·mol-1 | 452 | 462.8 | 497.3 | 226 | X |
请回答下列问题:
(1)试比较Si—C键与Si—Si键的键能大小:X
(2)H2被认为是21世纪人类最理想的燃料,而又有科学家提出硅是“21世纪的能源”“未来的石油”等观点。结合Ⅰ中图象,试计算每千克H2燃烧(生成水蒸气)放出的热量约为
您最近半年使用:0次



 (
(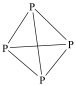 )形式存在的原因
)形式存在的原因

