铜有两种常见的氧化物CuO和Cu2O。某学习小组取0.98 g(用精密天平测量)Cu(OH)2固体加热,有铜的氧化物生成,其质量随温度变化如图甲所示;另外,某同学绘制了三条表示金属氧化物与其所含金属元素的质量的关系曲线,如图乙所示。则下列分析正确的是( )
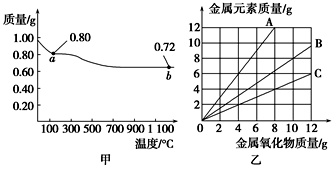

| A.图甲中a点和b点对应物质的化学式分别为Cu2O和CuO |
| B.图甲整个过程中共生成0.26 g水 |
| C.图乙三条曲线中,表示CuO和其中所含Cu元素质量关系的曲线是A |
| D.图甲中,a到b的过程中有0.01 mol电子发生了转移 |
2012·山西·一模 查看更多[14]
(已下线)【绍兴新东方】绍兴高中化学00015浙江省绍兴市2020-2021学年高一上学期期末调测化学试题人教版(2019)高一必修第一册第三章 铁 金属材料 高考挑战区(已下线)2019年1月17日 《每日一题》高考二轮复习-铜及其化合物【全国百强校】黑龙江省牡丹江市第一高级中学2019届高三上学期开学摸底考试化学试题2【全国百强校】黑龙江省牡丹江市第一高级中学2019届高三上学期开学摸底考试化学试题1(已下线)解密05 金属及其化合物(教师版)——备战2018年高考化学之高频考点解密吉林省长春市2018届高三上学期第二次月考化学试题吉林省实验中学2018届高三上学期第二次月考化学试题2017届河南省南阳市第一中学高三上学期第三次月考化学试卷(已下线)2012届山西省山大附中高三第一次模拟试题理综化学试卷 (已下线)2014届河北冀州中学高三上学期期中考试往届化学试卷2014届河北省衡水中学高三上学期一调考试化学试卷(已下线)2012届山西省山大附中高三第一次模拟试题理综化学试卷
更新时间:2018-08-28 22:21:30
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】生活污水中的氮和磷主要以铵盐和磷酸盐的形式存在,可用电解法从溶液中除去。有Cl-存在时,除氮原理如图1所示,主要依靠有效氯(HClO、ClO-)将NH4+或NH3氧化为N2。在不同pH条件下进行电解时,氮的去除率和水中有效氯浓度与溶液pH的关系如图2所示。
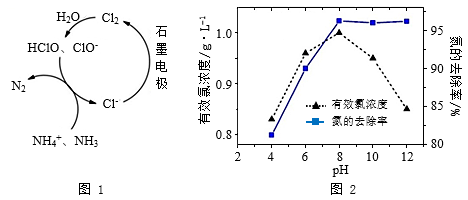
下列说法不正确 的是( )

下列说法
| A.pH=3时,主要发生ClO-氧化NH3的反应 |
| B.pH>8时,有效氯浓度随pH的增大而减小 |
| C.pH>8时,NH4+转变为NH3∙H2O,且有利于NH3逸出 |
| D.pH<8时,氮的去除率随pH的减小而下降的原因是c(HClO)减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】H2O与D2O的pKw(p/Cw=-lgKw)与温度的关系如图所示,下列有关说法正确的是


| A.常温下,向D2O中加入DCl,pKw变大 |
| B.25℃时,纯D2O的pH等于7 |
| C.25℃时,pH=7的液体一定是纯H2O |
| D.D2O的电离过程为吸热过程 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】298K时,将n(HA)+n(Aˉ)=0.lmol的HA、NaA混合物溶于水形成1L溶液,溶液中c(HA)、c(Aˉ)与pH的关系如图所示。下列叙述中正确的是
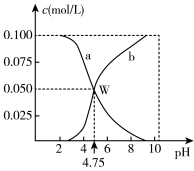

| A.a线表示的是c(Aˉ)的变化 |
| B.pH=6 时,c(Na+)+c(HA)>0. 1mol/L |
| C.298K时,Aˉ的水解平衡常数(K)的数量级为10-10 |
| D.若将等物质的量的HA、NaA溶于水中,所得溶液pH恰好为4.75 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】分别取V L含有Na2SO4和Al2(SO4)3的混合溶液两等份,一份加入含a mol NaOH的溶液,恰好使Al3+完全转化为AlO2-;另一份加入含b mol BaCl2的溶液,恰好使SO42-完全沉淀为BaSO4。则原混合溶液中Na+的浓度为 ( )
| A.8b-3a/2V mol•L-1 | B.8b-3a/4V mol•L-1 |
| C.a-2b/V mol•L-1 | D.a-2b/2V mol•L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】实验室按如图装置测定纯碱(含少量NaCl)的纯度。下列说法不正确的是
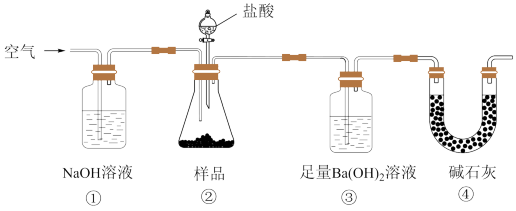

| A.装置③中发生的反应写作离子方程式为Ba2++2OH-+CO2=H2O+BaCO3↓ |
| B.装置①、④的作用是防止空气中的CO2进入装置③ |
| C.滴入盐酸前,应将装置中含有CO2的空气排尽 |
| D.反应结束时,不需要再通入空气将装置②中CO2转移到装置③中 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】某活动小组为测定样品中NaBH4的纯度,设计了如下的实验步骤:
步骤l:取5.0gNaBH4样品(杂质不参与反应),将样品溶于NaOH溶液后配成500mL溶液,取25.00mL置于碘量瓶中,加入60.00mL0.1000mol/L的KIO3溶液充分反应(反应为3NaBH4+4KIO3=3NaBO2+4KI+6H2O);
步骤2:向步骤1所得溶液中加入过量的KI溶液,用稀硫酸调节pH,使过量KIO3转化为I2,冷却后在暗处放置数分钟;
步骤3:向步骤2所得溶液中加入某种缓冲溶液调pH至5.0,加入几滴指示剂,用0.1000mol/L的Na2S2O3标准溶液滴定至终点,消耗标准溶液的体积为20.70mL(反应为I2+2Na2S2O3=2NaI+Na2S4O6)。
下列说法正确的是
步骤l:取5.0gNaBH4样品(杂质不参与反应),将样品溶于NaOH溶液后配成500mL溶液,取25.00mL置于碘量瓶中,加入60.00mL0.1000mol/L的KIO3溶液充分反应(反应为3NaBH4+4KIO3=3NaBO2+4KI+6H2O);
步骤2:向步骤1所得溶液中加入过量的KI溶液,用稀硫酸调节pH,使过量KIO3转化为I2,冷却后在暗处放置数分钟;
步骤3:向步骤2所得溶液中加入某种缓冲溶液调pH至5.0,加入几滴指示剂,用0.1000mol/L的Na2S2O3标准溶液滴定至终点,消耗标准溶液的体积为20.70mL(反应为I2+2Na2S2O3=2NaI+Na2S4O6)。
下列说法正确的是
| A.NaBH4中H元素化合价为+1价 |
B.步骤2反应的离子方程式为 +I-+6H+=I2+3H2O +I-+6H+=I2+3H2O |
| C.步骤3中加入几滴酚酞作指示剂 |
| D.样品中NaBH4的纯度为64.47% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】通过测定混合气中O2的含量可计算已变质的Na2O2(含Na2CO3)纯度的实验装置如图(Q为弹性良好的气囊)。下列分析错误的是
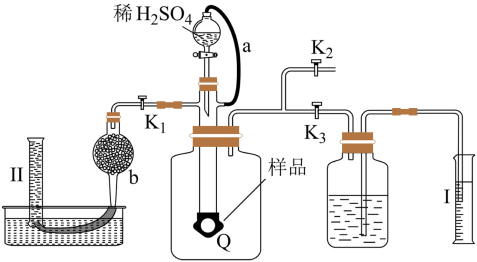

| A.b球形干燥管中装有碱石灰,用于除去气体中的二氧化碳 |
| B.测定气体总体积必须关闭K1、K2,打开K3 |
| C.读完气体总体积后,关闭K3,缓缓打开K1、K2;可观察到Q气球慢慢缩小 |
| D.量筒I用于测二氧化碳的量,干燥管中装入碱石灰,量筒II用于测氧气的量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】实验室按如下装置测定纯碱(含少量NaCl)的纯度。下列说法不正确的是( )
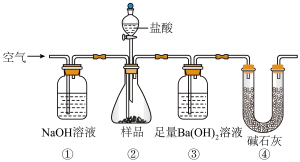

| A.滴入盐酸前,应将装置中含有CO2的空气排尽 |
| B.装置①、④的作用是防止空气中的CO2进入装置③ |
| C.必须在装置②、③间添加盛有饱和NaHCO3溶液的洗气瓶 |
| D.反应结束时,应再通入空气将装置②中CO2转移到装置③中 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】要测定某Na2CO3和NaHCO3混合物中Na2CO3的质量分数可采取不同的方法,取a克样品与一定量稀盐酸(过量)充分反应后,下列说法正确的是
| A.逸出气体若用碱石灰吸收,增重b克。则测定混合物中Na2CO3的质量分数偏小 |
| B.把所得溶液加热蒸干,并灼烧至恒重,得b克固体。蒸干过程中若未搅拌,则所测Na2CO3的质量分数可能偏大 |
| C.某NaOH标准溶液露置于空气中一段时间后,以甲基橙为指示剂,仍用此碱液滴定上述反应后的溶液,则所测Na2CO3的质量分数偏大 |
| D.产生的气体冷却至室温后,若测定其体积时忘记调平量气管和水准管内液面,则导致Na2CO3的质量分数偏小 |
您最近一年使用:0次



