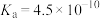氢氧燃料电池是一种新型的化学电源,其构造如图一所示:a、b两个电极均由多孔碳制成,通入的气体由孔隙中逸出,并在电极表面放电。

(1)a电极反应式是_______________________ ;
(2)该燃料电池生成了360 kg的水,则电路中通过了_____________ mol的电子。
(3)用如图二所示电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极反应式是___________________ 。
②Y电极的材料是______________ 。

(1)a电极反应式是
(2)该燃料电池生成了360 kg的水,则电路中通过了
(3)用如图二所示电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①X电极反应式是
②Y电极的材料是
更新时间:2018-09-02 17:51:16
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒。当氧气和氢气分别连续不断地从两极通入燃料电池时,便可在闭合回路中不断地产生电流。这被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高率的特点。试回答下列问题:写出氢氧燃料电池工作时的电极反应式负极:___ ,正极:___ 。


您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】I.图为铜锌原电池的装置请回答:
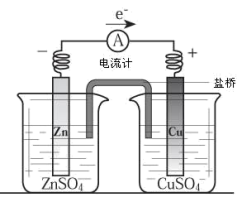
(1)铜是_________ 极,铜片上现象是_____________________
(2)锌为________ 极,电极反应式为_____________________
(3)电池反应式(离子反应)为____________________________________
II.氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,吸附气体的能力强,性质稳定,请回答:
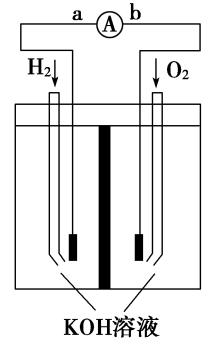
(4)在导线中电子流动方向为_________ (用a、b表示)。
(5)负极反应式为___________ 。正极反应式为___________ 。
(6)电极表面镀铂粉的原因为_____________________________________ 。

(1)铜是
(2)锌为
(3)电池反应式(离子反应)为
II.氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀一层细小的铂粉,吸附气体的能力强,性质稳定,请回答:

(4)在导线中电子流动方向为
(5)负极反应式为
(6)电极表面镀铂粉的原因为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】氢气是未来最理想的能源,科学家最近研制出利用太阳能在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O==2H2↑+O2↑。制得的氢气可用于燃料电池。试回答下列问题:
(1)分解海水时,实现了从_____ 能转变为_____ 能,二氧化钛作____ 。生成的氢气用于燃料电池时,实现____ 能转变为____ 能。水分解时,断裂的化学键为_______ 键,分解海水的反应属于______ 反应(填“放热”或“吸热”)。
(2)某种氢氧燃料电池是用固体金属化物陶瓷作电解质,两极上发生的电极反应分别为:A极:2H2+2O2--4e-==2H2O;B极:O2+4e-==2O2-.则A极是电池的___________ 极;电子从该极_______ (填“流入”或“流出”)。
(3)有人以化学反应:2Zn+O2+4H+==2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则原电池的负极材料是________ ,表示正极的电极反应为__________ 。
(1)分解海水时,实现了从
(2)某种氢氧燃料电池是用固体金属化物陶瓷作电解质,两极上发生的电极反应分别为:A极:2H2+2O2--4e-==2H2O;B极:O2+4e-==2O2-.则A极是电池的
(3)有人以化学反应:2Zn+O2+4H+==2Zn2++2H2O为基础设计一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则原电池的负极材料是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】若要在铁制品表面镀镍,电镀液用硫酸镍溶液,则镍应与电源的___ 极相连,铁制品应与电源的___ 极相连。阴极和阳极上的电极反应分别为___ 、__ 。电镀过程中硫酸镍溶液中溶质的浓度会___ (填“增大”“减小”或“不变”)。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】粗铜精炼
应用_______ 原理,以待精炼的铜作_______ ,以纯铜作_______ ,用硫酸铜溶液作电解质溶液.
应用
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】某锂电池的反应式为FePO4+Li LiFePO4,回答下列问题:
LiFePO4,回答下列问题:
(1)该蓄电池放电过程中发生还原反应的物质是___________ (写化学式),充电时外电路中转移了 电子,则阴极产物的质量为
电子,则阴极产物的质量为___________ g。
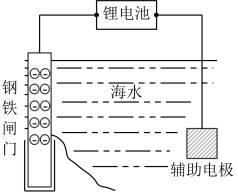
(2)为防止水体中的钢铁制品发生化学腐蚀,可采用外加电源的阴极保护法,下图是以海水中的钢铁闸门为例的保护图示,则锂电池___________ (填“正极”或“负极”)接钢铁闸门。
(3)若以该锂电池为电源,电解 稀溶液,制备
稀溶液,制备 和
和 ,则阴极的电极反应式为
,则阴极的电极反应式为___________ 。
(4)若利用该电源精炼铜。粗铜精炼过程中,因阳极杂质逐渐溶解,电解质溶液中 、
、 的浓度会逐渐增大,而这些杂质离子则会影响后续精炼。某同学设计下图所示的除杂方案:
的浓度会逐渐增大,而这些杂质离子则会影响后续精炼。某同学设计下图所示的除杂方案:
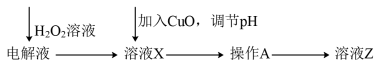
已知有关氢氧化输沉淀的pH如下表:
加入H2O2溶液时发生反应的离子方程式为___________ ;调节pH=5.0时,则沉淀的离子主要是___________ (填离子符号);操作A的名称是___________ 。该同学的方案中未除去的杂质金属阳离子是___________ 。
 LiFePO4,回答下列问题:
LiFePO4,回答下列问题:(1)该蓄电池放电过程中发生还原反应的物质是
 电子,则阴极产物的质量为
电子,则阴极产物的质量为(2)为防止水体中的钢铁制品发生化学腐蚀,可采用外加电源的阴极保护法,下图是以海水中的钢铁闸门为例的保护图示,则锂电池

(3)若以该锂电池为电源,电解
 稀溶液,制备
稀溶液,制备 和
和 ,则阴极的电极反应式为
,则阴极的电极反应式为(4)若利用该电源精炼铜。粗铜精炼过程中,因阳极杂质逐渐溶解,电解质溶液中
 、
、 的浓度会逐渐增大,而这些杂质离子则会影响后续精炼。某同学设计下图所示的除杂方案:
的浓度会逐渐增大,而这些杂质离子则会影响后续精炼。某同学设计下图所示的除杂方案:
已知有关氢氧化输沉淀的pH如下表:
| 氢氧化物 | Fe(OH)3 | Cu(OH)2 | Zn(OH)2 | Fe(OH)2 |
| 开始沉淀时的pH | 2.3 | 5.6 | 6.2 | 7.5 |
| 完全沉淀时的pH | 3.9 | 6.4 | 8.0 | 9.7 |
加入H2O2溶液时发生反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极)。电解一段时间后,若在电解池中C极一侧出来的气体无色无味,D极一侧出来的气体呈黄绿色有刺激性气味。请回答以下问题:

(1)已知铅蓄电池在放电时发生的反应:Pb+PbO2+4H++2SO42-=2PbSO4+2H2O,则A极的电极反应为___________________________ ;
(2)电解饱和食盐水的离子反应方程式是__________________ ;
(3)电极C的电极反应是_____________________________________________ ;
(4)电解时为防止两种气体产物混合,用阳离子交换膜做隔膜。则电解时Na+从______ 极区移向_____ 极区(填“C”或“D”);
(5)若电路上有0.2mol电子的电量通过,则铅蓄电池中消耗硫酸_________ mol。

(1)已知铅蓄电池在放电时发生的反应:Pb+PbO2+4H++2SO42-=2PbSO4+2H2O,则A极的电极反应为
(2)电解饱和食盐水的离子反应方程式是
(3)电极C的电极反应是
(4)电解时为防止两种气体产物混合,用阳离子交换膜做隔膜。则电解时Na+从
(5)若电路上有0.2mol电子的电量通过,则铅蓄电池中消耗硫酸
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】回答下列问题:
Ⅰ.25℃时,某些弱电解质的电离常数如表所示,回答下列问题。
(1)25℃时, 盐酸的pH约为
盐酸的pH约为______ ,该溶液中水电离出的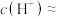
______  。
。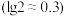
(2)少量的 通入
通入 溶液中,发生反应的离子方程式为
溶液中,发生反应的离子方程式为______ 。
(3) 发生水解反应的水解平衡常数
发生水解反应的水解平衡常数 表达式为
表达式为______ ;25℃时, 的水解平衡常数
的水解平衡常数
______ 其电离平衡常数 (填“>”或“<”),故
(填“>”或“<”),故 溶液显
溶液显______ 性。
Ⅱ.请分析如下电化学装置,回答下列问题:

(4)甲池为______ (填“原电池”“电解池”或“电镀池”),通入 电极的电极反应式正确的为
电极的电极反应式正确的为______ 。
A. B.
B.
C.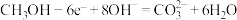 D.
D.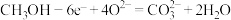
(5)当甲池中消耗 为1.12L(标准状况下)时,理论上乙池中B极质量增加
为1.12L(标准状况下)时,理论上乙池中B极质量增加______ g。
(6)丙池中发生的总反应化学方程式为______ ;为了防止丙池中两极产物相互反应,实际生产中在两极之间设有______ 离子交换膜(填“阴”或“阳”或“质子”)。
Ⅰ.25℃时,某些弱电解质的电离常数如表所示,回答下列问题。
弱电解质 |
|
| HClO |
电离常数 |
|
|
|
(1)25℃时,
 盐酸的pH约为
盐酸的pH约为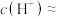
 。
。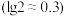
(2)少量的
 通入
通入 溶液中,发生反应的离子方程式为
溶液中,发生反应的离子方程式为(3)
 发生水解反应的水解平衡常数
发生水解反应的水解平衡常数 表达式为
表达式为 的水解平衡常数
的水解平衡常数
 (填“>”或“<”),故
(填“>”或“<”),故 溶液显
溶液显Ⅱ.请分析如下电化学装置,回答下列问题:

(4)甲池为
 电极的电极反应式正确的为
电极的电极反应式正确的为A.
 B.
B.
C.
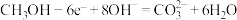 D.
D.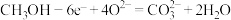
(5)当甲池中消耗
 为1.12L(标准状况下)时,理论上乙池中B极质量增加
为1.12L(标准状况下)时,理论上乙池中B极质量增加(6)丙池中发生的总反应化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】根据下图,回答下列问题:
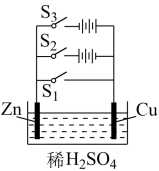
(1)若闭合S1,装置属于___________ ,锌极作___________ 。
(2)若闭合S2,装置属于___________ ,锌极上的反应为___________ 。
(3)若闭合S3,装置属于___________ ,总反应为___________ 。

(1)若闭合S1,装置属于
(2)若闭合S2,装置属于
(3)若闭合S3,装置属于
您最近一年使用:0次