除去下列物质中所含杂质(括号内为杂质),写出除去杂质的试剂。
(1)Fe2O3(Al2O3)______________ 。
(2)Cl2(HCl)_________________ 。
(3)FeCl2(FeCl3)_____________ 。
(4)CO2(HCl)_____________ 。
(1)Fe2O3(Al2O3)
(2)Cl2(HCl)
(3)FeCl2(FeCl3)
(4)CO2(HCl)
更新时间:2018-09-05 10:39:08
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】为了除去粗盐中含有的可溶性杂质CaCl2、MgCl2和Na2SO4,需进行下列实验操作,请在( )中填写所使用和除杂试剂的化学式,在 中填写实验操作名称。写出符合下列条件的离子方程式
中填写实验操作名称。写出符合下列条件的离子方程式
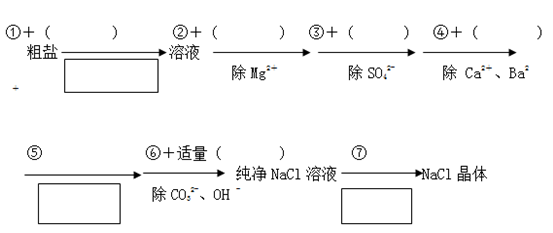
(1)①___________ 、 ____________ ;②_______________________ ;③____________ ;④____________ ;⑤____________ ;⑥____________ ;⑦____________ 。
(2)除去Mg2+的离子方程式_______________________________________________
(3)除去SO42-的离子方程式______________________________________________
 中填写实验操作名称。写出符合下列条件的离子方程式
中填写实验操作名称。写出符合下列条件的离子方程式
(1)①
(2)除去Mg2+的离子方程式
(3)除去SO42-的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】电子工业常用FeCl3溶液腐蚀印刷电路板上的铜箔。某研究小组设计以下流程从腐蚀废液中回收铜,并重新获得FeCl3溶液。

(1)FeCl3溶液腐蚀铜箔的离子方程式为___ 。
(2)试剂①为___ (写化学式),试剂②需过量的原因是___ 。
(3)证明“滤液”中不含Fe3+的方法为___ 。
(4)“反应”步骤中的离子方程式为___ 。
(5)向沸水中加入1mol•L-1FeCl3溶液至液体呈透明的红褐色,该分散系具有的独特性质是___ (写出一条)。

(1)FeCl3溶液腐蚀铜箔的离子方程式为
(2)试剂①为
(3)证明“滤液”中不含Fe3+的方法为
(4)“反应”步骤中的离子方程式为
(5)向沸水中加入1mol•L-1FeCl3溶液至液体呈透明的红褐色,该分散系具有的独特性质是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】玫瑰精油被称为“液体黄金”是多种天然有机化合物的混合物,在食品,化妆品,医药,保健品等领域有重大的应用价值和经济价值。常见的玫瑰精油提取过程如下:
I.水蒸气提取法:
(1)第①步装置如下图所示。

在左侧炉中加入水。通过投料口将碾碎的玫瑰花加入,放在带孔隔板上。加热生成的水蒸气将玫瑰花中的精油带出。最终在收集瓶中得到油水混合物。将玫瑰花碾碎的意义是_______ ,水泵中的水应从_______ (填“甲”或“乙”)口流入
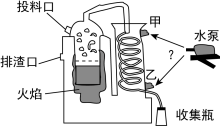
(2)第②步操作要用到的主要仪器是_______ 。
Ⅱ.萃取法

(3)步骤①用到酒精浸泡玫瑰花的原因是_______ ,步骤②的操作为_______ 。
(4)水蒸气提取法和萃取法各有优劣。你会选择哪种方法提取玫瑰精油?写出你选择的理由_______ 。
I.水蒸气提取法:
(1)第①步装置如下图所示。

在左侧炉中加入水。通过投料口将碾碎的玫瑰花加入,放在带孔隔板上。加热生成的水蒸气将玫瑰花中的精油带出。最终在收集瓶中得到油水混合物。将玫瑰花碾碎的意义是

(2)第②步操作要用到的主要仪器是
Ⅱ.萃取法

(3)步骤①用到酒精浸泡玫瑰花的原因是
(4)水蒸气提取法和萃取法各有优劣。你会选择哪种方法提取玫瑰精油?写出你选择的理由
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】某废催化剂(主要含有WO3、V2O5、V2O4、V2O3、少量杂质Fe2O3、SiO2等)是能源行业产生的难处理多金属危险废物,其回收利用已成为当前研究的热点和重点。一种处理流程如下:

已知草酸晶体(H2C2O4·2H2O)的溶解度随温度的变化如图所示。草酸酸浸时控制温度为90℃,理由是___________ ,实验室中宜选用的加热方式为___________ (“水浴加热”或“油浴加热”)。


已知草酸晶体(H2C2O4·2H2O)的溶解度随温度的变化如图所示。草酸酸浸时控制温度为90℃,理由是

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】为将混有K2SO4、MgSO4的KNO3固体提纯并获得KNO3溶液,方案如下:
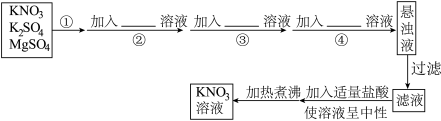
(1)实验操作①为___________ ,为提高该操作速度通常采用的方法是___________ 。
(2)若操作②加入的试剂为KOH溶液,则③④步加入试剂依次发生反应的化学方程式为:___________ 、___________ 。
(3)该同学设计的实验方案不严密,请纠正并说明理由___________ 。
(4)如何判断SO 已除尽,简述实验操作
已除尽,简述实验操作___________ 。

(1)实验操作①为
(2)若操作②加入的试剂为KOH溶液,则③④步加入试剂依次发生反应的化学方程式为:
(3)该同学设计的实验方案不严密,请纠正并说明理由
(4)如何判断SO
 已除尽,简述实验操作
已除尽,简述实验操作
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物,试回答下列问题:
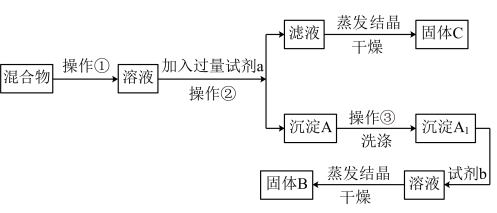
供选试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸
(1)操作①的名称是____ ,操作②的名称是____ 。
(2)试剂a是_____ (填化学式,下同),试剂b是_____ 。固体B是_____ 。
(3)加入试剂a所发生反应的化学方程式为__________ 。加入试剂b所发生反应的化学方程式为___________ 。
(4)该方案能否达到实验目的:______ 。(填“能”或“不能”)若不能,应如何改进?(若能,此问不用回答)_____ 。

供选试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸
(1)操作①的名称是
(2)试剂a是
(3)加入试剂a所发生反应的化学方程式为
(4)该方案能否达到实验目的:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】四氧化三锰(Mn3O4)广泛应用于生产软磁材料、催化材料制备领域。一种以低品位锰矿(含MnCO3、Mn2O3、MnOOH及少量Fe2O3、Al2O3、SiO2)为原料生产Mn3O4的工艺流程如图:已知:(NH4)2SO4 NH3↑+NH4HSO4
NH3↑+NH4HSO4

回答下列问题:
(1)MnOOH中Mn的化合价为______ 。
(2)“溶浸”中Mn2O3参与反应的离子方程式为_______ 。
(3)“滤渣2”的主要成分有________ 。
(4)“母液”溶质的主要成分是_______ ,循环利用该物质的方案是________ 。
(5)氧化”时,将固体加入水中,70℃水浴加热,通空气氧化,将固体全部转化为Mn3O4。Mn(OH)2生成Mn3O4的化学方程式为____ 。反应后溶液pH____ (填“增大”、“减小”或“不变”)。
 NH3↑+NH4HSO4
NH3↑+NH4HSO4
回答下列问题:
(1)MnOOH中Mn的化合价为
(2)“溶浸”中Mn2O3参与反应的离子方程式为
(3)“滤渣2”的主要成分有
(4)“母液”溶质的主要成分是
(5)氧化”时,将固体加入水中,70℃水浴加热,通空气氧化,将固体全部转化为Mn3O4。Mn(OH)2生成Mn3O4的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐2】石墨在材料领域有重要应用。某初级石墨中含SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质。设计的提纯与综合利用工艺如下:

(注:SiCl4的沸点为57.6 ℃,金属氯化物的沸点均高于150 ℃)
(1)向反应器中通入Cl2前,需通一段时间N2,主要目的是__________________ 。
(2)高温反应后,石墨中氧化物杂质均转变为相应的氯化物。气体Ⅰ中的碳氧化物主要为________ 。由气体Ⅱ中某物质得到水玻璃的化学反应方程式为_____________________________________ 。
(3)步骤①为:搅拌、________ 。所得溶液Ⅳ中的阴离子有________________ 。
(4)100 kg初级石墨最多可获得Ⅴ的质量为________ kg。

(注:SiCl4的沸点为57.6 ℃,金属氯化物的沸点均高于150 ℃)
(1)向反应器中通入Cl2前,需通一段时间N2,主要目的是
(2)高温反应后,石墨中氧化物杂质均转变为相应的氯化物。气体Ⅰ中的碳氧化物主要为
(3)步骤①为:搅拌、
(4)100 kg初级石墨最多可获得Ⅴ的质量为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】石墨在材料领域有重要应用。某初级石墨中含SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质。设计的提纯和综合应用流程如下:

(注:SiCl4的沸点是57.6ºC,金属氯化物的沸点均高于150ºC)
(1)已知1mol石墨完全转化为金刚石需要吸收1.9kJ的能量。请写出石墨转化为金刚石的热化学反应方程式:_________________________ 。
(2)①向反应器中通入Cl2前,需通一段时间的N2。高温反应后,石墨中的氧化物杂质均转变为相应氯化物。80℃冷凝的目的是:_____________________ 。②由活性炭得到气体Ⅱ的化学反应方程式为:_____________________ 。
(3)加入过量NaOH溶液得到溶液IV的离子反应方程式为:_________________________ 。
(4)用化学反应原理解释得到沉淀V的过程中乙酸乙酯和加热的作用:________ 。1kg初级石墨最多可获得V的质量为_______________ kg。

(注:SiCl4的沸点是57.6ºC,金属氯化物的沸点均高于150ºC)
(1)已知1mol石墨完全转化为金刚石需要吸收1.9kJ的能量。请写出石墨转化为金刚石的热化学反应方程式:
(2)①向反应器中通入Cl2前,需通一段时间的N2。高温反应后,石墨中的氧化物杂质均转变为相应氯化物。80℃冷凝的目的是:
(3)加入过量NaOH溶液得到溶液IV的离子反应方程式为:
(4)用化学反应原理解释得到沉淀V的过程中乙酸乙酯和加热的作用:
您最近一年使用:0次



