有一种透明溶液,其中可能含有Fe3+、Fe2+、Mg2+、Al3+、Cu2+,Na+,NH4+中的一种或几种,加入一种淡黄色固体粉末时,加热有刺激性气味的气体放出,同时产生白色沉淀,生成物的物质的量(纵轴)与所加淡黄色粉末的物质的量(横轴)的关系如图所示,试回答下列问题:

(1)淡黄色固体粉末的名称是____ ,所含化学键是______ ;
(2)溶液中一定没有的离子是______ ;
(3)溶液中一定存在的离子是,它们的物质的量分别为__________ .

(1)淡黄色固体粉末的名称是
(2)溶液中一定没有的离子是
(3)溶液中一定存在的离子是,它们的物质的量分别为
2019高三·全国·专题练习 查看更多[1]
(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第5讲 数形结合思想的应用【教学案】
更新时间:2018-09-14 20:46:13
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】某溶液中可能含有 、
、 、
、 、
、 、
、 、
、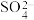 等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的质量随加入的NaOH的物质的量的变化如图所示:
等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的质量随加入的NaOH的物质的量的变化如图所示:

(1)由此可知,该溶液中肯定含有的离子是______________________________________ ,且各离子的物质的量之比为___________________________________________
(2)该溶液中肯定不含的阳离子是________________ 。
(3)写出NaOH的物质的量从8mol到9mol发生的离子反应方程式:____________________________
 、
、 、
、 、
、 、
、 、
、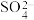 等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的质量随加入的NaOH的物质的量的变化如图所示:
等离子,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的质量随加入的NaOH的物质的量的变化如图所示: 
(1)由此可知,该溶液中肯定含有的离子是
(2)该溶液中肯定不含的阳离子是
(3)写出NaOH的物质的量从8mol到9mol发生的离子反应方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是___________ 。
①因为NH4HCO3受热易分解,故可用作氮肥
②下列物质间的转化能够实现:N2 NH3
NH3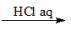 NH4Cl(aq)
NH4Cl(aq)
③NH4Cl溶液与Ca(OH)2溶液混合的离子方程式为H++OH-===H2O
④用生石灰与浓氨水制得的气体能使湿润的红色石蕊试纸变蓝,说明NH3为碱性气体
⑤检验溶液中是否含有 :取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体
:取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体
⑥加热盛有NH4Cl的试管,试管底部有固体消失,试管口有晶体凝结,说明NH4Cl固体可以升华
⑦实验室用NH4Cl制取氨气:
⑧施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用,是因为K2CO3与NH4Cl反应生成氨气会降低肥效
⑨加热NH4Cl和Ca(OH)2混合物,并将产生的气体通入酚酞溶液中,酚酞溶液变成红色
⑩测0.1mol/L氨水的pH为11的,氨水的电离方程式:NH3·H2O
 +OH-
+OH-
⑪向Al2(SO4)3溶液中加入过量氨水的离子方程式:Al3++3NH3·H2O=Al(OH)3↓+3
⑫NH3、O2和HNO3三种物质中,任意两种物质在一定条件下均能发生反应
①因为NH4HCO3受热易分解,故可用作氮肥
②下列物质间的转化能够实现:N2
 NH3
NH3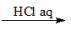 NH4Cl(aq)
NH4Cl(aq)③NH4Cl溶液与Ca(OH)2溶液混合的离子方程式为H++OH-===H2O
④用生石灰与浓氨水制得的气体能使湿润的红色石蕊试纸变蓝,说明NH3为碱性气体
⑤检验溶液中是否含有
 :取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体
:取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体⑥加热盛有NH4Cl的试管,试管底部有固体消失,试管口有晶体凝结,说明NH4Cl固体可以升华
⑦实验室用NH4Cl制取氨气:

⑧施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用,是因为K2CO3与NH4Cl反应生成氨气会降低肥效
⑨加热NH4Cl和Ca(OH)2混合物,并将产生的气体通入酚酞溶液中,酚酞溶液变成红色
⑩测0.1mol/L氨水的pH为11的,氨水的电离方程式:NH3·H2O

 +OH-
+OH-⑪向Al2(SO4)3溶液中加入过量氨水的离子方程式:Al3++3NH3·H2O=Al(OH)3↓+3

⑫NH3、O2和HNO3三种物质中,任意两种物质在一定条件下均能发生反应
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】某同学设计了如图所示装置(夹持仪器省略)进行系列实验,实验时将药品A逐滴加入到固体B中,请根据下列实验回答问题:

(1)若A为水,B为过氧化钠,C中盛有酸化过的FeCl2溶液,旋开活塞E后,烧瓶中发生反应的化学方程式为_________ ,C中的现象为___________________ ;
(2)利用上述装置可以验证物质的性质,如设计证明氧化性:KMnO4>Cl2并制取漂白液(有效成分为NaClO),则A为浓盐酸,B为高锰酸钾C中发生反应的离子方程式为________ D装置的作用是:___________ 也可设计证明酸性的强弱:H2SO4>H2CO3>H2SiO3则A为硫酸、B为纯碱、C中盛有水玻璃,则小试管中的现象是_____________ ;
(3)利用上述装置可以验证SO2的性质,若A为浓硫酸,B为亚硫酸钠固体,那么C中盛有__________ 溶液时可验证其具有漂白性;而C中盛有_________ 溶液时可验证其具有还原性。

(1)若A为水,B为过氧化钠,C中盛有酸化过的FeCl2溶液,旋开活塞E后,烧瓶中发生反应的化学方程式为
(2)利用上述装置可以验证物质的性质,如设计证明氧化性:KMnO4>Cl2并制取漂白液(有效成分为NaClO),则A为浓盐酸,B为高锰酸钾C中发生反应的离子方程式为
(3)利用上述装置可以验证SO2的性质,若A为浓硫酸,B为亚硫酸钠固体,那么C中盛有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)写出乙醇和乙酸反应的化学反应方程式__________________ ;
(2)写出苯发生硝化反应的方程式_______________ ;
(3)写出过氧化钠和二氧化碳反应的方程式_____________________ ;
(2)写出苯发生硝化反应的方程式
(3)写出过氧化钠和二氧化碳反应的方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下表是元素周期表的一部分,请参照元素①~⑦在表中的位置,请用化学用语回答下列问题:

(1)①~⑦元素中原子半径最大的是_______ 半径最小的是_______ (用元素符号表示);
(2)②、⑦两种元素所形成的气态氢化物中最稳定的是_______ (用化学式表示);
(3)③的单质着火时不能用水来灭火,原因之一是其燃烧的产物能与水反应,该反应的化学方程式为_______ ,该反应中产生标准状况下22.4 L的气体时,转移的电子的数目为_______ (用含 的代数式表示);
的代数式表示);
(4)写出③和④两种元素的最高价氧化物对应水化物反应的离子方程式_______ ;
(5)⑦元素单质的新制水溶液中能起杀菌消毒作用,光照易分解的弱酸是_______ 。(用化学式表示)

(1)①~⑦元素中原子半径最大的是
(2)②、⑦两种元素所形成的气态氢化物中最稳定的是
(3)③的单质着火时不能用水来灭火,原因之一是其燃烧的产物能与水反应,该反应的化学方程式为
 的代数式表示);
的代数式表示);(4)写出③和④两种元素的最高价氧化物对应水化物反应的离子方程式
(5)⑦元素单质的新制水溶液中能起杀菌消毒作用,光照易分解的弱酸是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】向20 mL某浓度的AlCl3溶液中滴加2 mol•L-1的NaOH溶液时,得到Al(OH)3沉淀的质量(g)与所滴加NaOH溶液的体积(mL)关系如图所示,试回答下列问题:

(1)图中A点表示沉淀的化学式是_____ ,其物质的量是_____ 。
(2)反应至A点时消耗NaOH溶液的体积为________ 。
(3)AlCl3溶液的浓度为________ 。
(4)假设溶液中有0. 39克Al(OH)3沉淀,则此时用去NaOH溶液体积为____ 。

(1)图中A点表示沉淀的化学式是
(2)反应至A点时消耗NaOH溶液的体积为
(3)AlCl3溶液的浓度为
(4)假设溶液中有0. 39克Al(OH)3沉淀,则此时用去NaOH溶液体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某溶液中只含有以下离子中的全部或部分: Ag+、Fe3+、Al3+、H+、SO42-、CO32-、OH-、Cl-,取该溶液做以下实验:
①观察溶液外观, 溶液有颜色;
②取少量该溶液加入Ba(NO3)2溶液, 无现象;
③取该溶液 100 mL,向其中逐滴滴加 1 mol/L的NaOH溶液至过量,生成沉淀物质的量与所加入的 NaOH 溶液的体积关系如图所示。根据实验回答以下问题:
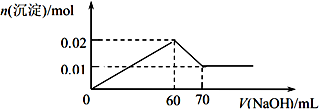
(1)检验溶液中阴离子的离子方程式为________________________________ 。
(2)根据以上实验推断,溶液中各离子的物质的量浓度分别为________________________________ 。
(3)若取以上溶液 100 mL,加入足量氨水后过滤,再将所得沉淀洗涤、灼烧,所得固体残留物的物质的量为_____________ mol。
①观察溶液外观, 溶液有颜色;
②取少量该溶液加入Ba(NO3)2溶液, 无现象;
③取该溶液 100 mL,向其中逐滴滴加 1 mol/L的NaOH溶液至过量,生成沉淀物质的量与所加入的 NaOH 溶液的体积关系如图所示。根据实验回答以下问题:

(1)检验溶液中阴离子的离子方程式为
(2)根据以上实验推断,溶液中各离子的物质的量浓度分别为
(3)若取以上溶液 100 mL,加入足量氨水后过滤,再将所得沉淀洗涤、灼烧,所得固体残留物的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.下面是同学们熟悉的物质:①SO2②P4③NaBr④CCl4⑤Na2CO3⑥NH4Cl⑦NaHSO4⑧Ne⑨Na2O2⑩H2O2。
(1)其中只含有共价键的非极性化合物有_______ (填序号,下同)
(2)含有非极性共价键的离子化合物_______ ;
(3)不含共价键的化合物_______ ;
(4)含有极性键和非极性键的化合物是_______ ;
(5)将NaHSO4加热到熔融,写出其熔融状态的电离方程式:_______ 。
II.写出用下图所示装置写出制备Cl2、NH3的化学方程式。(依据条件需要装置可以加热)

(6)制备Cl2_______ 。
(7)制备NH3_______ 。
(1)其中只含有共价键的非极性化合物有
(2)含有非极性共价键的离子化合物
(3)不含共价键的化合物
(4)含有极性键和非极性键的化合物是
(5)将NaHSO4加热到熔融,写出其熔融状态的电离方程式:
II.写出用下图所示装置写出制备Cl2、NH3的化学方程式。(依据条件需要装置可以加热)

(6)制备Cl2
(7)制备NH3
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下列几种物质:①MgCl2 ②H2O ③Al ④H2O2 ⑤Na2O2 ⑥Ca(OH)2 ⑦HClO ⑧I2 ⑨He
(1)只含有离子键的是(选填序号,下同)_______________ ;
(2)含有共价键的离子化合物是_____________ ;
(3)共价化合物是__________ ;
(4)熔融状态时和固态时,都能导电的是_______________ ;
(5)HClO的电子式____________ 。
(6)用电子式表示MgCl2的形成过程_______________________________________________
(1)只含有离子键的是(选填序号,下同)
(2)含有共价键的离子化合物是
(3)共价化合物是
(4)熔融状态时和固态时,都能导电的是
(5)HClO的电子式
(6)用电子式表示MgCl2的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据元素周期律回答:
(1)比较原子半径的大小(填“>”或“<”,下同):K___________ Ca,Si___________ N;
(2)比较酸碱性的强弱:HNO3___________ H3PO4,Mg(OH)2___________ Al(OH)3;
(3)比较氢化物的热稳定性:H2S___________ H2O,NH3___________ HF。
(4)①N2②MgCl2③NH3④Na2O2⑤Ne,这些物质中,只含有非极性键的是___________ ;只含有离子键的是___________ ;既含有共价键又含有离子键的是___________ ;只含有极性键的是___________ ;无化学键的是___________ 。写出②的形成过程:___________ 。
(1)比较原子半径的大小(填“>”或“<”,下同):K
(2)比较酸碱性的强弱:HNO3
(3)比较氢化物的热稳定性:H2S
(4)①N2②MgCl2③NH3④Na2O2⑤Ne,这些物质中,只含有非极性键的是
您最近一年使用:0次



