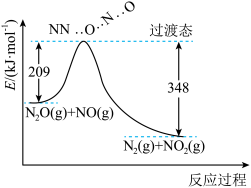
已知有化合价变化的化学反应叫做氧化还原反应。航天飞机用高氯酸铵(NH4ClO4)与铝粉的混合物为固体燃料,点燃时铝粉氧化放热引发高氯酸铵反应,其方程式可表示为:2NH4ClO4(s) N2(g)+4H2O(g)+Cl2(g)+2O2(g) △H=-Q kJ/mol下列叙述不正确的是
N2(g)+4H2O(g)+Cl2(g)+2O2(g) △H=-Q kJ/mol下列叙述不正确的是
 N2(g)+4H2O(g)+Cl2(g)+2O2(g) △H=-Q kJ/mol下列叙述不正确的是
N2(g)+4H2O(g)+Cl2(g)+2O2(g) △H=-Q kJ/mol下列叙述不正确的是| A.上述反应属于氧化还原反应 |
| B.上述反应瞬间产生大量高温气体推动航天飞机飞行 |
| C.反应从能量变化上看,化学能完全转变为热能 |
| D.在反应中气体的体积明显增大 |
更新时间:2018-10-02 09:07:14
|
相似题推荐
【推荐1】已知:可逆反应N2(g)+3H2(g)  2NH3(g) △H=-92.4kJ/mol。现有甲、乙完全相同的恒容密闭容器,向甲容器中加入1molN2(g)和3molH2(g),在一定条件下发生反应,达到平衡时放出热量为Q1kJ。在相同条件下,向乙容器中加入2molNH3(g)并发生反应,达到平衡时吸收热量为Q2kJ,若Q1=3Q2,下列叙述中正确的是
2NH3(g) △H=-92.4kJ/mol。现有甲、乙完全相同的恒容密闭容器,向甲容器中加入1molN2(g)和3molH2(g),在一定条件下发生反应,达到平衡时放出热量为Q1kJ。在相同条件下,向乙容器中加入2molNH3(g)并发生反应,达到平衡时吸收热量为Q2kJ,若Q1=3Q2,下列叙述中正确的是
 2NH3(g) △H=-92.4kJ/mol。现有甲、乙完全相同的恒容密闭容器,向甲容器中加入1molN2(g)和3molH2(g),在一定条件下发生反应,达到平衡时放出热量为Q1kJ。在相同条件下,向乙容器中加入2molNH3(g)并发生反应,达到平衡时吸收热量为Q2kJ,若Q1=3Q2,下列叙述中正确的是
2NH3(g) △H=-92.4kJ/mol。现有甲、乙完全相同的恒容密闭容器,向甲容器中加入1molN2(g)和3molH2(g),在一定条件下发生反应,达到平衡时放出热量为Q1kJ。在相同条件下,向乙容器中加入2molNH3(g)并发生反应,达到平衡时吸收热量为Q2kJ,若Q1=3Q2,下列叙述中正确的是| A.Q1+Q2=92.4 |
| B.达平衡时甲、乙中NH3的体积分数乙>甲 |
| C.达到平衡后,再向乙中加入0.25molN2(g)、0.75molH2(g)和1.5molNH3(g),平衡向生成N2的方向移动 |
| D.达平衡时甲中N2的转化率为25% |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知:
①2C(s)+O2(g)===2CO(g) ΔH=-220 kJ·mol-1
②氢气燃烧的能量变化示意图:

下列说法正确的是
①2C(s)+O2(g)===2CO(g) ΔH=-220 kJ·mol-1
②氢气燃烧的能量变化示意图:

下列说法正确的是
| A.1 mol C(s)完全燃烧放出110 kJ的热量 |
B.H2(g)+ O2(g)===H2O(g) ΔH=-480 kJ·mol-1 O2(g)===H2O(g) ΔH=-480 kJ·mol-1 |
| C.C(s)+H2O(g)===CO(g)+H2(g) ΔH=+130 kJ·mol-1 |
| D.欲分解2 mol H2O(g),至少需要提供240 kJ的热量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列关于对燃烧现象的认识中,不正确的是
| A.燃烧一定是氧化还原反应 | B.燃烧一定发光放热 |
| C.燃烧一定是化学反应 | D.燃烧一定有氧气参与 |
您最近一年使用:0次
单选题
|
适中
(0.64)
名校
【推荐2】已知1 mol红磷转化为1 mol白磷,吸收18.39 kJ热量.
①4P(红,s)+5O2(g)=2P2O5(s) ΔH1
②P4(白,s)+5O2(g)=2P2O5(s) ΔH2
则ΔH1与ΔH2的关系正确的是
①4P(红,s)+5O2(g)=2P2O5(s) ΔH1
②P4(白,s)+5O2(g)=2P2O5(s) ΔH2
则ΔH1与ΔH2的关系正确的是
| A.ΔH1=ΔH2 | B.ΔH1>ΔH2 | C.ΔH1<ΔH2 | D.无法确定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】 稀溶液中存在如下平衡:
稀溶液中存在如下平衡:
Ⅰ.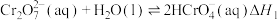
Ⅱ.
关于该溶液的说法不正确 的是(温度变化忽略不计)
 稀溶液中存在如下平衡:
稀溶液中存在如下平衡:Ⅰ.
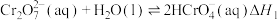
Ⅱ.

关于该溶液的说法
| A.加水稀释,溶液中离子总数增加 |
B.加入少量浓 溶液,Ⅰ和Ⅱ均向正反应方向移动 溶液,Ⅰ和Ⅱ均向正反应方向移动 |
C.加入少量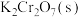 ,溶液颜色不再变化时, ,溶液颜色不再变化时,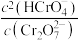 比原溶液中的小 比原溶液中的小 |
D.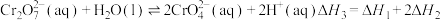 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH1=-890.3 kJ·mol-1;2H2(g)+O2(g)=2H2O(l)ΔH2=-571.6 kJ·mol-1。CO2与H2反应生成甲烷气体与液态水的热化学方程式为CO2(g)+4H2(g)=CH4(g)+2H2O(l)ΔH3,则ΔH3为
| A.-252.9 kJ·mol-1 | B.+252.9 kJ·mol-1 | C.-604.5 kJ·mol-1 | D.+604.5 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知下列反应:
则反应④的ΔH4为
| 反应序号 | 化学反应 | 反应热 |
| ① | Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) | ΔH1=-26.7kJ·mol-1 |
| ② | 3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) | ΔH2=-50.8kJ·mol-1 |
| ③ | Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) | ΔH3=-36.5kJ·mol-1 |
| ④ | FeO(s)+CO(g)=Fe(s)+CO2(g) | ΔH4 |
| A.+7.3kJ·mol-1 | B.-7.3kJ·mol-1 |
| C.+43.8kJ·mol-1 | D.-43.8kJ·mol-1 |
您最近一年使用:0次