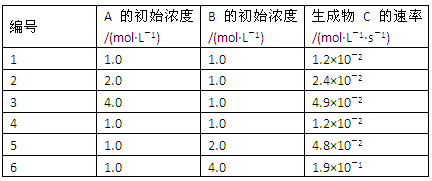
有一化学反应aA+bB=C,根据影响化学反应速率的因素可得v(C)=kcm(A)cn(B)。其中k是与温度有关的常数,为测k、m、n的值,在298 K时,将A、B溶液按不同的浓度混合,得到下列实验数据:
(1)根据上表可求得:m=_______ ,n=______ ,k=________ 。
(2) 当c(A)=c(B)=2.0mol/L时,用B表示的初始反应速率为___________________ 。
(1)根据上表可求得:m=
(2) 当c(A)=c(B)=2.0mol/L时,用B表示的初始反应速率为
更新时间:2018-10-05 09:09:34
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
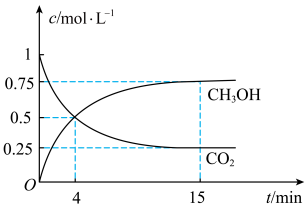
【推荐1】C、N、S的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的不利影响。在500℃下合成甲醇的反应原理为:CO2(g)+3H2(g) CH3OH(g)+H2O(g),在1 L 的密闭容器中,充入1 mol CO2和3 mol H2,压强为p0 ,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。(可逆反应的平衡常数可以用平衡浓度计算,也可以用平衡分压Kp代替平衡浓度,计算分压=总压×物质的量分数)
CH3OH(g)+H2O(g),在1 L 的密闭容器中,充入1 mol CO2和3 mol H2,压强为p0 ,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。(可逆反应的平衡常数可以用平衡浓度计算,也可以用平衡分压Kp代替平衡浓度,计算分压=总压×物质的量分数)
①反应进行到4 min 时,υ(正)__ (填“>”“<”或“=”)υ(逆)。0~4 min,H2的平均反应速率υ(H2)=__ mol·L-1·min-1。
②CO2平衡时的体积分数为_____ ,该温度下Kp为_____ (用含有p0的式子表示)。
 CH3OH(g)+H2O(g),在1 L 的密闭容器中,充入1 mol CO2和3 mol H2,压强为p0 ,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。(可逆反应的平衡常数可以用平衡浓度计算,也可以用平衡分压Kp代替平衡浓度,计算分压=总压×物质的量分数)
CH3OH(g)+H2O(g),在1 L 的密闭容器中,充入1 mol CO2和3 mol H2,压强为p0 ,测得CO2(g)和CH3OH(g)的浓度随时间变化如图所示。(可逆反应的平衡常数可以用平衡浓度计算,也可以用平衡分压Kp代替平衡浓度,计算分压=总压×物质的量分数)①反应进行到4 min 时,υ(正)
②CO2平衡时的体积分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】用纯净的CaCO3与100mL稀盐酸反应制取CO2,实验过程中CO2体积变化记录如图所示(CO2的体积已折算为保准状况下的体积),回答下列问题:

①0~3min中,_______ 段(选择OE、EF、FG)表示的平均反应速率最大,OE、EF、FG三段中,该反应用CO2表示的平均反应速率之比为______ 。
②用盐酸表示EF段中该反应的平均反应速率为________ mol/(L∙min)。

①0~3min中,
②用盐酸表示EF段中该反应的平均反应速率为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】T°C时,将6mol A(g)和2molB(g)充入2L的恒容密闭容器中发生反应:3A(g)+B(g)⇌mC(g)+2D(s)。测得2s内C(g)的平均反应速率为0.3 mol·L-1·s-1,且2s末D(g)的物质的量为1.2 mol。
请回答下列问题:
(1)m=_____
(2)2s内用物质A表示的平均反应速率为______ 。
(3)2s末时物质B的转化率为_____
(4)从2s末开始到C的浓度变为1.2 mol·L-1时所用的时间____ 2s(填"大于”“小于”或”等于”)
请回答下列问题:
(1)m=
(2)2s内用物质A表示的平均反应速率为
(3)2s末时物质B的转化率为
(4)从2s末开始到C的浓度变为1.2 mol·L-1时所用的时间
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】一定温度下,向容积为10L的密闭容器内通入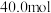
 和
和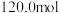
 ,经2s后达到平衡状态,平衡时
,经2s后达到平衡状态,平衡时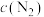 为
为 。
。
(1)达到平衡时氨气的物质的量浓度为:________ 。
(2)用 的浓度变化表示2s内的平均速率
的浓度变化表示2s内的平均速率
________ 。
(3)达到平衡时氮气的转化率是________ 。
(4)平衡时混合气体中氨的体积分数(和物质的量分数相同)是________ 。
(5)平衡时氮气、氢气、氨气的分子数之比为________ 。
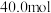
 和
和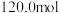
 ,经2s后达到平衡状态,平衡时
,经2s后达到平衡状态,平衡时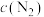 为
为 。
。(1)达到平衡时氨气的物质的量浓度为:
(2)用
 的浓度变化表示2s内的平均速率
的浓度变化表示2s内的平均速率
(3)达到平衡时氮气的转化率是
(4)平衡时混合气体中氨的体积分数(和物质的量分数相同)是
(5)平衡时氮气、氢气、氨气的分子数之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】在2 L密闭容器中进行反应:aX(s)+bY(g) cP(g)+dQ(g),式中a、b、c、d为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
cP(g)+dQ(g),式中a、b、c、d为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
已知2 min内v(Q)=0.075 mol·L-1·min-1,v(P)∶v(Y)=2∶5。
(1)试确定以下物质的相关量:起始时n(Y)=______ ,2min末时n(Q)=______ 。
(2)上述反应的化学方程式为_________
(3)用Y表示2 min内的反应速率为______ 。2min末,Q在混合气体的体积分数为_____
(4)在保持温度和容积不变的情况下,下列关于上述反应的叙述不 正确的是_____
a.2 min内用X表示的反应速率为0.05mol·L-1·min-1
b.向容器内充入稀有气体Ar(不参与反应),会导致体系压强增大,反应速率加快
c.随着反应的进行,混合气体的平均相对分子质量不再改变即说明反应已经达到平衡
d.随着反应的进行,混合气体的密度不再改变即说明反应已经达到平衡
e.随着反应的进行,混合气体的压强不再改变即说明反应已经达到平衡
 cP(g)+dQ(g),式中a、b、c、d为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
cP(g)+dQ(g),式中a、b、c、d为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:| 物质 时间 | X | Y | P | Q |
| 起始/mol | 0.5 | 1.0 | 1.5 | |
| 2min末/mol | 0.7 | 2.7 | 0.8 | |
| 3min末/mol | 2.7 |
(1)试确定以下物质的相关量:起始时n(Y)=
(2)上述反应的化学方程式为
(3)用Y表示2 min内的反应速率为
(4)在保持温度和容积不变的情况下,下列关于上述反应的叙述
a.2 min内用X表示的反应速率为0.05mol·L-1·min-1
b.向容器内充入稀有气体Ar(不参与反应),会导致体系压强增大,反应速率加快
c.随着反应的进行,混合气体的平均相对分子质量不再改变即说明反应已经达到平衡
d.随着反应的进行,混合气体的密度不再改变即说明反应已经达到平衡
e.随着反应的进行,混合气体的压强不再改变即说明反应已经达到平衡
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】某温度时,在2 L的密闭容器中,X、Y、Z(均为气体)的物质的量随时间的变化曲线如图所示。请回答下列问题:

(1)由图中所给数据进行分析,该反应的化学方程式为_______ 。
(2)下列措施能加快反应速率的是_______ (填序号,下同)。
A.恒压时充入He B.恒容时充入He C.恒容时充入X
D.及时分离出Z E.升高温度 F.选择高效的催化剂
(3)能说明该反应已达到平衡状态的是_______ (填字母)。
A.v(X)=v(Y) B.2v正(Y)=v逆(Z) C.容器内压强保持不变
D.容器内混合气体的密度保持不变 E.X、Y、Z的浓度相等
(4)反应从开始至2 min,用X的浓度变化表示的平均反应速率v(X)=_______ 。
(5)将5 mol X与3 mol Y的混合气体通入2 L的密闭容器中并发生上述反应,反应到某时刻各物质的物质的量恰好满足:n(X)=n(Y)=n(Z),则原混合气体X的转化率=_______ 。

(1)由图中所给数据进行分析,该反应的化学方程式为
(2)下列措施能加快反应速率的是
A.恒压时充入He B.恒容时充入He C.恒容时充入X
D.及时分离出Z E.升高温度 F.选择高效的催化剂
(3)能说明该反应已达到平衡状态的是
A.v(X)=v(Y) B.2v正(Y)=v逆(Z) C.容器内压强保持不变
D.容器内混合气体的密度保持不变 E.X、Y、Z的浓度相等
(4)反应从开始至2 min,用X的浓度变化表示的平均反应速率v(X)=
(5)将5 mol X与3 mol Y的混合气体通入2 L的密闭容器中并发生上述反应,反应到某时刻各物质的物质的量恰好满足:n(X)=n(Y)=n(Z),则原混合气体X的转化率=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】将0.1mol MnO2加到10mL过氧化氢(H2O2)的水溶液里(密度为1.1g/mL),在标准状况下放出气体的体积和时间的关系如图:

(1)a、b、c三点反应速率快慢顺序为_______ ,反应速率变化的可能原因是______________ 。
(2)计算过氧化氢的起始物质的量浓度是多少?_______________
(3)假设反应过程中溶液的体积保持不变,则用H2O2表示该反应1—3分钟内的平均速率为多少?_________________

(1)a、b、c三点反应速率快慢顺序为
(2)计算过氧化氢的起始物质的量浓度是多少?
(3)假设反应过程中溶液的体积保持不变,则用H2O2表示该反应1—3分钟内的平均速率为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】I.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
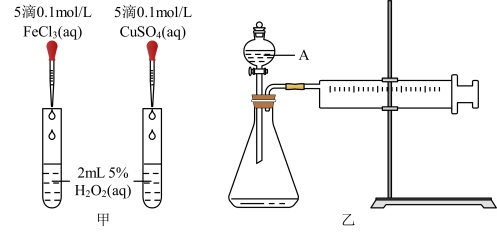
(1)定性分析:如图甲可通过观察__________ 的快慢,定性比较得出结论。有同学提出将FeCl3改为0. 05mol·L-1 Fe2 (SO4)3更为合理,其理由是____________ 。
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是________ 。
II.某温度时,在一个2L的密闭容器中, A、B、C三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(3)该反应的化学方程式为________ ;
(4)从开始至2min,A的平均反应速率为________ ;

(1)定性分析:如图甲可通过观察
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。实验中需要测量的数据是
II.某温度时,在一个2L的密闭容器中, A、B、C三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(3)该反应的化学方程式为
(4)从开始至2min,A的平均反应速率为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】对氮及其化合物的研究具有重要意义。
(1)在1L密闭容器中,4mol氨气在一定条件下分解生成生成氮气和氢气。2min时反应吸收热量为46.1KJ,此时氨气的转化率为25%。该反应的热化学方程式为____________ 。
(2)某恒温恒压条件下,向容积为VL的密闭容器中,起始充入lmolN2、3molH2、16molNH3,发生N2(g)+3H2(g) 2NH3(g)。达到平衡后,N2、H2、NH3的物质的量分别amol、bmol、cmol,此时容器的容积为1.1VL,回答下列问题:
2NH3(g)。达到平衡后,N2、H2、NH3的物质的量分别amol、bmol、cmol,此时容器的容积为1.1VL,回答下列问题:
① 起始时反应速率V(正)______ V(逆)(填“>”“<”或“=”)
② 平衡时a=________ , b=________ .
③ 若平衡后再充入3.6mol NH3,重新建立平衡时容器的容积为________ .
(1)在1L密闭容器中,4mol氨气在一定条件下分解生成生成氮气和氢气。2min时反应吸收热量为46.1KJ,此时氨气的转化率为25%。该反应的热化学方程式为
(2)某恒温恒压条件下,向容积为VL的密闭容器中,起始充入lmolN2、3molH2、16molNH3,发生N2(g)+3H2(g)
 2NH3(g)。达到平衡后,N2、H2、NH3的物质的量分别amol、bmol、cmol,此时容器的容积为1.1VL,回答下列问题:
2NH3(g)。达到平衡后,N2、H2、NH3的物质的量分别amol、bmol、cmol,此时容器的容积为1.1VL,回答下列问题:① 起始时反应速率V(正)
② 平衡时a=
③ 若平衡后再充入3.6mol NH3,重新建立平衡时容器的容积为
您最近一年使用:0次



