Ⅰ.实验是化学研究的一种重要手段,现有下图所示A-G七种仪器,请根据要求填空。
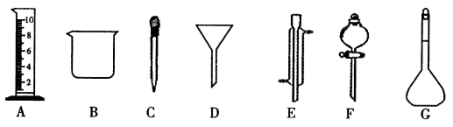
(1)写出仪器名称:E_____________ ,F_____________ 。
(2)上述仪器中实验之前需检查装置是否会漏水的是______________ (填仪对应字母)。
(3)下列实验操作中用到仪器D的是_________ (选填下列选项的编号字母 )。
A.分离水和CCl4的混合物 B.分离水和酒精的混合物 C.分离水和泥砂的混合物
Ⅱ.某课外兴趣小组需要200 mL1 mol/L的Na2CO3溶液,请回答下列问题:
(1)配制溶液所需仪器及药品:
(2)配制时,其正确的操作顺序是(用字母表示,每个操作只能用一次)______________ 。
A.将已冷却的溶液沿玻璃棒注入容量瓶中
B.用托盘天平准确称量所需Na2CO3的质量,倒入烧杯中,再加入适量水,用玻璃棒慢慢搅动,使其溶解(必要时可加热)
C.用适量水洗涤烧杯2~3次,洗涤液均注入容量瓶中,振荡
D.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
E.将容量瓶盖紧,振荡,摇匀
F.继续往容量瓶内小心加水,直到液面接近刻度1~2 cm处
(3)若出现如下情况,对所配溶液浓度将有何影响 (填“偏高”、“偏低”或“无影响”)?
没有进行C操作________ ;配制溶液时,容量瓶未干燥_________ ;定容时俯视刻度线_________ 。
(4)在实验操作的摇匀过程中,不慎洒出几滴,此时应采取的措施是_______________ 。

(1)写出仪器名称:E
(2)上述仪器中实验之前需检查装置是否会漏水的是
(3)下列实验操作中用到仪器D的是
A.分离水和CCl4的混合物 B.分离水和酒精的混合物 C.分离水和泥砂的混合物
Ⅱ.某课外兴趣小组需要200 mL1 mol/L的Na2CO3溶液,请回答下列问题:
(1)配制溶液所需仪器及药品:
| 应称取Na2CO3的质量 | 应选用容量瓶的规格 | 除容量瓶外还需要的其它玻璃仪器是上图中的量筒、烧杯、 |
A.将已冷却的溶液沿玻璃棒注入容量瓶中
B.用托盘天平准确称量所需Na2CO3的质量,倒入烧杯中,再加入适量水,用玻璃棒慢慢搅动,使其溶解(必要时可加热)
C.用适量水洗涤烧杯2~3次,洗涤液均注入容量瓶中,振荡
D.改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
E.将容量瓶盖紧,振荡,摇匀
F.继续往容量瓶内小心加水,直到液面接近刻度1~2 cm处
(3)若出现如下情况,对所配溶液浓度将有何影响 (填“偏高”、“偏低”或“无影响”)?
没有进行C操作
(4)在实验操作的摇匀过程中,不慎洒出几滴,此时应采取的措施是
更新时间:2018-10-10 07:56:54
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室常用18 mol/L的浓硫酸配制稀硫酸,现欲用该浓硫酸配制1.00 mol/L的硫酸溶液100 mL,其操作如下:
①洗涤烧杯和玻璃棒2-3次,将洗涤液转入容量瓶中
②用量筒量取一定体积的浓硫酸
③将稀释、冷却后的硫酸转入100 mL容量瓶中
④加水至液面接近刻度线1-2 cm处然后定容、摇匀、装瓶(贴上标签)
⑤将浓硫酸沿着玻璃棒缓缓加入到盛有一定量水的烧杯中,并不断搅拌、稀释、冷却
完成下列填空:
(1)第②步操作中应用量筒量取___________ mL浓硫酸;应选择___________ mL量筒(填“5”、“10”或“50”)。
(2)本实验用到的基本仪器已有烧杯、量筒、玻璃棒,还缺少的仪器是___________ 。
(3)正确的操作顺序是②___________ ④(用序号填写)。
(4)若浓硫酸稀释后未冷却至室温就完成溶液配制,则配制的硫酸浓度将___________ (填“偏大"或“偏小”)。若定容时液面高过刻度线则应该___________ ,配制好的溶液需装入细口瓶,瓶上应该贴有___________ 、___________ 等字样的标签。
①洗涤烧杯和玻璃棒2-3次,将洗涤液转入容量瓶中
②用量筒量取一定体积的浓硫酸
③将稀释、冷却后的硫酸转入100 mL容量瓶中
④加水至液面接近刻度线1-2 cm处然后定容、摇匀、装瓶(贴上标签)
⑤将浓硫酸沿着玻璃棒缓缓加入到盛有一定量水的烧杯中,并不断搅拌、稀释、冷却
完成下列填空:
(1)第②步操作中应用量筒量取
(2)本实验用到的基本仪器已有烧杯、量筒、玻璃棒,还缺少的仪器是
(3)正确的操作顺序是②
(4)若浓硫酸稀释后未冷却至室温就完成溶液配制,则配制的硫酸浓度将
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某实验小组用0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸进行中和热的测定。
Ⅰ.配制0.50 mol·L-1 NaOH溶液
(1)若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体_____ g。
(2)从下表中选择,称量NaOH固体所需要的仪器是(填字母)________ 。
Ⅱ.测定稀硫酸和稀氢氧化钠溶液中和热的实验装置如图所示。

(1)若生成1 mol H2O时反应放出的热量为57.3 kJ,写出该反应的热化学方程式:__________ 。
(2)取50 mL NaOH溶液和30 mL硫酸进行实验,实验数据如下表。
①请填写下表中的空白:
②用上述实验数值计算结果为____ kJ•mol-1,与57.3 kJ•mol-1有偏差,产生偏差的原因可能是_____ (填字母)。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
Ⅰ.配制0.50 mol·L-1 NaOH溶液
(1)若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体
(2)从下表中选择,称量NaOH固体所需要的仪器是(填字母)
| 名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 | 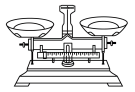 |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |
Ⅱ.测定稀硫酸和稀氢氧化钠溶液中和热的实验装置如图所示。

(1)若生成1 mol H2O时反应放出的热量为57.3 kJ,写出该反应的热化学方程式:
(2)取50 mL NaOH溶液和30 mL硫酸进行实验,实验数据如下表。
①请填写下表中的空白:
| 温度 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②用上述实验数值计算结果为
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】现需要0.2mol/L Na2CO3溶液240mL,实验室除蒸馏水外还提供无水Na2CO3固体和4mol/L Na2CO3溶液两种试剂以配制该溶液。
(1)无论采用何种试剂进行配制,除烧杯、玻璃棒、胶头滴管外,至少还必须用到的一种玻璃仪器是___________ ,在使用该仪器前必须进行的操作是___________ 。
(2)若用无水Na2CO3固体进行配制,需用托盘天平称取无水Na2CO3固体的质量为_______ g;如果用4mol/L Na2CO3溶液稀释配制,需用量筒量取_______ mL。
(3)用4mol/L Na2CO3溶液稀释配制溶液所需的实验步骤有:
a 往烧杯中加入约100mL水进行初步稀释,冷却至室温
b 用量筒量取一定体积4moL/L Na2CO3溶液于一烧杯中
c 计算所需4mol/LNa2CO3溶液的体积
d 盖好瓶塞,反复上下颠倒摇匀后,将溶液转存于试剂瓶中
e 加水至液面离容量瓶刻度线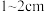 处改用胶头滴管进行定容
处改用胶头滴管进行定容
f 洗涤烧杯和玻璃棒2—3次并将洗涤液注入容量瓶,轻轻摇动容量瓶,使溶液混合均匀
g 将溶液转移入容量瓶
其中正确的操作顺序为___________ 。
(4)配制过程中,以下情形使所得溶液浓度偏高的是___________ 。
A d步骤摇匀后,发现液面低于刻度线,再加水至刻度线
B e步骤中,俯视刻度线
C g步骤前,容量瓶未干燥,有少量蒸馏水
D b步骤中,量取碳酸钠溶液时,仰视读数
(1)无论采用何种试剂进行配制,除烧杯、玻璃棒、胶头滴管外,至少还必须用到的一种玻璃仪器是
(2)若用无水Na2CO3固体进行配制,需用托盘天平称取无水Na2CO3固体的质量为
(3)用4mol/L Na2CO3溶液稀释配制溶液所需的实验步骤有:
a 往烧杯中加入约100mL水进行初步稀释,冷却至室温
b 用量筒量取一定体积4moL/L Na2CO3溶液于一烧杯中
c 计算所需4mol/LNa2CO3溶液的体积
d 盖好瓶塞,反复上下颠倒摇匀后,将溶液转存于试剂瓶中
e 加水至液面离容量瓶刻度线
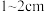 处改用胶头滴管进行定容
处改用胶头滴管进行定容f 洗涤烧杯和玻璃棒2—3次并将洗涤液注入容量瓶,轻轻摇动容量瓶,使溶液混合均匀
g 将溶液转移入容量瓶
其中正确的操作顺序为
(4)配制过程中,以下情形使所得溶液浓度偏高的是
A d步骤摇匀后,发现液面低于刻度线,再加水至刻度线
B e步骤中,俯视刻度线
C g步骤前,容量瓶未干燥,有少量蒸馏水
D b步骤中,量取碳酸钠溶液时,仰视读数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】最近小明对水产生了浓厚的兴趣。

(1)在化学课堂上,老师进行了电解水的实验,揭示了水的组成。右图实验中试管1中得到的气体在点燃之前要先进行验纯的原因是_____ 。
(2)小明放学回家后,主动帮妈妈刷碗,发现自来水洗不掉碗碟上的油污,发现加入少许洗涤剂就可以洗干净,是因为洗涤剂有_____ 作用。
(3)周末他取村子里的河水于玻璃杯中,倒入少量肥皂水,用筷子搅拌后发现有大量浮渣漂浮在水面上,无泡沫产生,说明河水是_____ (选填“硬水”或“软水”)。硬水的危害很大,生活中将硬水软化的方法是_____ 。
(4)晚上,小明在电视上看到保护水资源的呼吁。下列做法中,你认为有利于防治水体污染的是_____。
(5)小明从课本学习到水常用作溶剂,实验室配制质量分数为0.9%的氯化钠溶液,小明用量筒量取蒸馏水读数时,仰视凹液面的最低处,会引起所配溶液的溶质质量分数_____ (选填“大于”、“小于”或“等于”)0.9%。

(1)在化学课堂上,老师进行了电解水的实验,揭示了水的组成。右图实验中试管1中得到的气体在点燃之前要先进行验纯的原因是
(2)小明放学回家后,主动帮妈妈刷碗,发现自来水洗不掉碗碟上的油污,发现加入少许洗涤剂就可以洗干净,是因为洗涤剂有
(3)周末他取村子里的河水于玻璃杯中,倒入少量肥皂水,用筷子搅拌后发现有大量浮渣漂浮在水面上,无泡沫产生,说明河水是
(4)晚上,小明在电视上看到保护水资源的呼吁。下列做法中,你认为有利于防治水体污染的是_____。
| A.使用节水型马桶 | B.生活污水任意排放 |
| C.合理施用农药和化肥 | D.工业废水处理达标后排放 |
(5)小明从课本学习到水常用作溶剂,实验室配制质量分数为0.9%的氯化钠溶液,小明用量筒量取蒸馏水读数时,仰视凹液面的最低处,会引起所配溶液的溶质质量分数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】亚硫酸钠是重要的化工原料,常用作还原剂、防腐剂、去氯剂等。回答下列问题:
(1)要配制250mL0.5mol/L的Na2SO3溶液,需要用托盘天平称取Na2SO3·7H2O晶体________ g。配制溶液所用到的玻璃仪器有:玻璃棒、烧杯、量筒和_________________ 。
(2)配制过程中所用蒸馏水需煮沸、冷却后才能使用,煮沸蒸馏水的目的是________ 。
(3)下列操作会使所配溶液浓度偏高的是________ 。
A.所选用的溶质已经失去部分结晶水 B.亚硫酸钠晶体与砝码位置放反了
C.转移溶液时玻璃棒靠在刻度线上方 D.定容时俯视容量瓶的刻度线
E.摇匀后溶液低于刻度线,再加入蒸馏水使液面最低点与刻度线相切
(4)Na2SO3放在空气中容易被氧化变质。检验Na2SO3溶液是否变质的方法是_______ 。
(1)要配制250mL0.5mol/L的Na2SO3溶液,需要用托盘天平称取Na2SO3·7H2O晶体
(2)配制过程中所用蒸馏水需煮沸、冷却后才能使用,煮沸蒸馏水的目的是
(3)下列操作会使所配溶液浓度偏高的是
A.所选用的溶质已经失去部分结晶水 B.亚硫酸钠晶体与砝码位置放反了
C.转移溶液时玻璃棒靠在刻度线上方 D.定容时俯视容量瓶的刻度线
E.摇匀后溶液低于刻度线,再加入蒸馏水使液面最低点与刻度线相切
(4)Na2SO3放在空气中容易被氧化变质。检验Na2SO3溶液是否变质的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】实验室欲用氢氧化钠固体配制1.0mol·L-1的氢氧化钠溶液240mL:
(1)配制溶液时,一般可以分为以下几个步骤:
①称量②计算③溶解④摇匀⑤转移⑥洗涤⑦定容⑧冷却⑨摇动
其正确的操作顺序为___ 。必须用到的玻璃仪器有烧杯、胶头滴管、___ 。
(2)某同学欲称量氢氧化钠的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图所示。烧杯的实际质量为___ g,要完成本实验该同学应称出__ g氢氧化钠。

(3)如图是该同学转移溶液的示意图,图中有两处错误,请写出:

①____ ;
②____ 。
(4)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是__ (填字母)。
A.所用氢氧化钠已经潮解
B.溶液未冷却至室温就注入容量瓶中定容
C.在配制过程中未洗涤烧杯和玻璃棒
D.定容时,俯视容量瓶刻度线
(1)配制溶液时,一般可以分为以下几个步骤:
①称量②计算③溶解④摇匀⑤转移⑥洗涤⑦定容⑧冷却⑨摇动
其正确的操作顺序为
(2)某同学欲称量氢氧化钠的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图所示。烧杯的实际质量为

(3)如图是该同学转移溶液的示意图,图中有两处错误,请写出:

①
②
(4)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是
A.所用氢氧化钠已经潮解
B.溶液未冷却至室温就注入容量瓶中定容
C.在配制过程中未洗涤烧杯和玻璃棒
D.定容时,俯视容量瓶刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。

(1)写出下列仪器b的名称为___________ 。
(2)仪器a~e中,使用前必须检查是否漏水的有___________ 。(填序号)
(3)若利用装置分离四氯化碳和酒精的混合物,还缺少的仪器是___________ ,将仪器补充完整后进行实验,冷凝水由___________ 口流出(填f或g)。
(4)现需配制0.1mol/LNaOH溶液450mL,如上右图装置是某同学转移溶液的示意图。
①图中的错误是___________ 。
②配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)___________ 。
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解。
C.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(5)若定容时俯视刻度线对所配溶液浓度将有何影响___________ 。(填“偏高”、“偏低”或“无影响”)。

(1)写出下列仪器b的名称为
(2)仪器a~e中,使用前必须检查是否漏水的有
(3)若利用装置分离四氯化碳和酒精的混合物,还缺少的仪器是
(4)现需配制0.1mol/LNaOH溶液450mL,如上右图装置是某同学转移溶液的示意图。
①图中的错误是
②配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解。
C.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(5)若定容时俯视刻度线对所配溶液浓度将有何影响
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
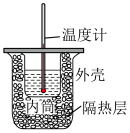
【推荐2】某实验小组用50mL0.50mol·L-1盐酸溶液与50mL0.55mol·L-1NaOH溶液进行中和热的测定,装置如图所示。回答下列问题:
(1)若实验分组共需要1000mLNaOH溶液,实验室在配制该溶液时,则需要称量NaOH固体___________ g。
(2)图中装置缺少的玻璃仪器是___________ 。
(3)NaOH溶液的浓度要稍大于盐酸浓度的原因是___________ 。
(4)请填写表中的平均温度差:
(5)近似认为0.50mol/L盐酸溶液与0.55mol/LNaOH溶液的密度都是1g/mL,中和后生成溶液的比热容c=4.18J·g-1·℃-1,则上述实验测得的中和热△H=___________ (结果保留至小数点后一位)。
(6)上述实验测得放出的热量小于57.3kJ,产生偏差的原因可能是___________ (填字母)。
A.用量筒量取盐酸溶液时仰视读数
B.实验过程中,内筒未加杯盖
C.用测量盐酸的温度计直接测定NaOH溶液的温度

(1)若实验分组共需要1000mLNaOH溶液,实验室在配制该溶液时,则需要称量NaOH固体
(2)图中装置缺少的玻璃仪器是
(3)NaOH溶液的浓度要稍大于盐酸浓度的原因是
(4)请填写表中的平均温度差:
| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | 平均温度差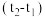 /℃ /℃ | ||
| HCl | NaOH | 平均值 | |||
| 1 | 23.0 | 23.2 | 23.1 | 26.3 | |
| 2 | 23.2 | 23.4 | 23.3 | 27.2 | |
| 3 | 22.9 | 22.9 | 22.9 | 26.0 | |
| 4 | 23.1 | 22.9 | 23.0 | 26.3 | |
(6)上述实验测得放出的热量小于57.3kJ,产生偏差的原因可能是
A.用量筒量取盐酸溶液时仰视读数
B.实验过程中,内筒未加杯盖
C.用测量盐酸的温度计直接测定NaOH溶液的温度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某次实验需用0.4 mol/L NaOH溶液480mL。配制方法如下:
(1)配制该溶液应选用________ mL容量瓶;
(2)用托盘天平准确称量________ g 固体NaOH,应放在________ (仪器)中称量。
(3)将称量好的NaOH固体放在500mL大烧杯中,倒入约100mL蒸馏水,用玻璃棒搅拌,使固体全部溶解,待______________ 后,将烧杯中的溶液注入容量瓶中;
(4)用少量蒸馏水洗涤烧杯________ 次,洗涤后的溶液_______________ ,轻轻晃动容量瓶,使溶液混合均匀;
(5)向容量瓶中加入蒸馏水,到液面接近刻度线__________ 时,改用_________ 加蒸馏水至液面最低点与刻度线相切。盖好瓶塞,上下颠倒混合均匀;
(6)若在配制过程中出现下列情况,将使所配制的NaOH溶液的浓度偏高的是________ ,偏低的是________ ,对实验结果没有影响的是____________ (填各选项的序号)。
A.所用的NaOH中混有少量Na2CO3
B.用带有生锈砝码的托盘天平称量一定质量固体NaOH
C.配制溶液所用的容量瓶洗净后没有烘干
D.固体NaOH在烧杯中溶解后立即将溶液转移到容量瓶内并接着进行后续操作
E.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
F.最后确定NaOH溶液体积(定容)时,俯视观察液面与容量瓶刻度线
G.定容摇匀后静止,发现液面低于刻度线,再加蒸馏水至刻度线
(1)配制该溶液应选用
(2)用托盘天平准确称量
(3)将称量好的NaOH固体放在500mL大烧杯中,倒入约100mL蒸馏水,用玻璃棒搅拌,使固体全部溶解,待
(4)用少量蒸馏水洗涤烧杯
(5)向容量瓶中加入蒸馏水,到液面接近刻度线
(6)若在配制过程中出现下列情况,将使所配制的NaOH溶液的浓度偏高的是
A.所用的NaOH中混有少量Na2CO3
B.用带有生锈砝码的托盘天平称量一定质量固体NaOH
C.配制溶液所用的容量瓶洗净后没有烘干
D.固体NaOH在烧杯中溶解后立即将溶液转移到容量瓶内并接着进行后续操作
E.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
F.最后确定NaOH溶液体积(定容)时,俯视观察液面与容量瓶刻度线
G.定容摇匀后静止,发现液面低于刻度线,再加蒸馏水至刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】Ⅰ.实验室有化学纯的浓硫酸,已知其质量分数为98%,其试剂瓶标签上的部分内容如图:
(1)配制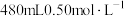 的稀硫酸,需取该浓硫酸
的稀硫酸,需取该浓硫酸_______  。
。
(2)完成此实验需用到的玻璃仪器有量筒、烧杯、玻璃棒、_______ 。
(3)下列操作会使所配硫酸溶液浓度偏高的是_______。
Ⅱ.实验室里需要纯净的氯化钠溶液,现只有混有硫酸钠、碳酸氢铵的氯化钠固体。某学生设计了如下方案:

(4)操作①中发生的化学反应方程式为: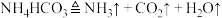 ,则可选择
,则可选择_______ (试管、坩埚、烧杯、蒸发皿)进行加热。
(5)为了达到实验目的,进行操作②后,为证明溶液中 已沉淀完全的方法是
已沉淀完全的方法是_______ 。
(6)为了得到纯净的氯化钠溶液过滤后还需要进行的操作是:_______ 。
硫酸化学纯  品名:硫酸 化学式: 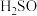 相对分子质量:98 密度:  |
(1)配制
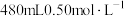 的稀硫酸,需取该浓硫酸
的稀硫酸,需取该浓硫酸 。
。(2)完成此实验需用到的玻璃仪器有量筒、烧杯、玻璃棒、
(3)下列操作会使所配硫酸溶液浓度偏高的是_______。
| A.量取浓硫酸时俯视刻度线 |
| B.稀释硫酸时未冷却至室温,直接转移至容量瓶 |
| C.转移时容量瓶内有少量水 |
| D.定容时仰视刻度线 |
Ⅱ.实验室里需要纯净的氯化钠溶液,现只有混有硫酸钠、碳酸氢铵的氯化钠固体。某学生设计了如下方案:

(4)操作①中发生的化学反应方程式为:
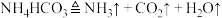 ,则可选择
,则可选择(5)为了达到实验目的,进行操作②后,为证明溶液中
 已沉淀完全的方法是
已沉淀完全的方法是(6)为了得到纯净的氯化钠溶液过滤后还需要进行的操作是:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室需要配制0.50 mol·L-1NaCl溶液480 mL。按下列操作步骤填上适当的文字,以使整个操作完整。
(1)选择仪器。完成本实验所必需的仪器有:托盘天平(带砝码、最小砝码为5 g)、药匙、烧杯、________ 、________ 、________ 以及等质量的两片滤纸。
(2)计算。配制该溶液需取NaCl晶体________ g。
(3)称量。
①天平调平之后,应将天平的游码调至某个位置,请在如图中用一根竖线标出游码左边缘所处的位置:________
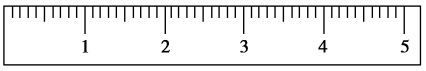
②称量过程中NaCl晶体应放于天平的________ (填“左盘”或“右盘”)。
③称量完毕,将药品倒入烧杯中。
(4)溶解、冷却。该步实验中需要使用玻璃棒,目的是___________________ 。
(5)转移、洗涤。在转移时应使用玻璃棒引流,需要洗涤烧杯2~3次是为了________________ 。
(6)定容。向容量瓶中加水至液面接近刻度线________ 处,改用________ 加水,使溶液凹液面与刻度线相切。
(7)摇匀、装瓶。
(1)选择仪器。完成本实验所必需的仪器有:托盘天平(带砝码、最小砝码为5 g)、药匙、烧杯、
(2)计算。配制该溶液需取NaCl晶体
(3)称量。
①天平调平之后,应将天平的游码调至某个位置,请在如图中用一根竖线标出游码左边缘所处的位置:

②称量过程中NaCl晶体应放于天平的
③称量完毕,将药品倒入烧杯中。
(4)溶解、冷却。该步实验中需要使用玻璃棒,目的是
(5)转移、洗涤。在转移时应使用玻璃棒引流,需要洗涤烧杯2~3次是为了
(6)定容。向容量瓶中加水至液面接近刻度线
(7)摇匀、装瓶。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】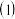 实验室欲用NaOH固体配制
实验室欲用NaOH固体配制 的NaOH溶液
的NaOH溶液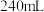 。
。
①本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、250mL容量瓶、还有_________ ;
②要完成本实验该同学应称出____________ 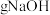 ;
;
③若直接在天平的两个托盘上放两张质量相等的纸片进行称量,则会使得配制结果_______ 。 偏低、偏高或无影响
偏低、偏高或无影响
 铁不能与冷、热水反应,但能与水蒸气反应。老师用如图所示实验装置,完成还原铁粉与水蒸气反应的演示实验。
铁不能与冷、热水反应,但能与水蒸气反应。老师用如图所示实验装置,完成还原铁粉与水蒸气反应的演示实验。
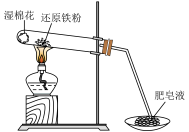
①反应一段时间后,有肥皂泡吹起时,用点燃的火柴靠近肥皂泡,当_________ 时 填实验现象
填实验现象 ,说明“铁与水蒸气”能够进行反应;
,说明“铁与水蒸气”能够进行反应;
②写出该反应的化学方程式,并用单线桥表示出电子转移情况___________ ;
③为了研究一定时间内铁粉的消耗量,他们设计了如下实验:准确称量一定质量的铁粉进行反应,收集并测量反应后生成的气体体积 已折算成标准状况
已折算成标准状况 。收集并测量气体体积应选下图中的
。收集并测量气体体积应选下图中的________ 装置;

若称取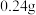 铁粉,然后与水蒸气加热至无气体放出,最好选用
铁粉,然后与水蒸气加热至无气体放出,最好选用__________ 规格的量筒 选填字母序号
选填字母序号 。
。
A.100mL B.200mL C.500mL D.1000mL
 实验室欲用NaOH固体配制
实验室欲用NaOH固体配制 的NaOH溶液
的NaOH溶液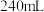 。
。①本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、250mL容量瓶、还有
②要完成本实验该同学应称出
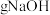 ;
;③若直接在天平的两个托盘上放两张质量相等的纸片进行称量,则会使得配制结果
 偏低、偏高或无影响
偏低、偏高或无影响
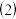 铁不能与冷、热水反应,但能与水蒸气反应。老师用如图所示实验装置,完成还原铁粉与水蒸气反应的演示实验。
铁不能与冷、热水反应,但能与水蒸气反应。老师用如图所示实验装置,完成还原铁粉与水蒸气反应的演示实验。
①反应一段时间后,有肥皂泡吹起时,用点燃的火柴靠近肥皂泡,当
 填实验现象
填实验现象 ,说明“铁与水蒸气”能够进行反应;
,说明“铁与水蒸气”能够进行反应;②写出该反应的化学方程式,并用单线桥表示出电子转移情况
③为了研究一定时间内铁粉的消耗量,他们设计了如下实验:准确称量一定质量的铁粉进行反应,收集并测量反应后生成的气体体积
 已折算成标准状况
已折算成标准状况 。收集并测量气体体积应选下图中的
。收集并测量气体体积应选下图中的
若称取
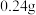 铁粉,然后与水蒸气加热至无气体放出,最好选用
铁粉,然后与水蒸气加热至无气体放出,最好选用 选填字母序号
选填字母序号 。
。A.100mL B.200mL C.500mL D.1000mL
您最近一年使用:0次



