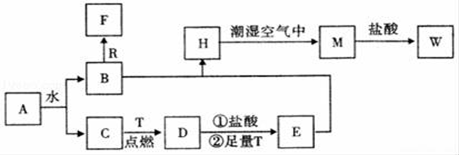
X、Y、Z为三种常见的单质,Z为绿色植物光合作用后的产物之一,A、B为常见化合物.它们在一定条件下可以发生如图反应(均不是在溶液中进行的反应)(以下每个空中只需填入一种物质)
(1)X、Y均为金属时,此反应在工业上称为___ 反应,其反应方程式为 ________
(2)X为金属,Y为非金属时,A为__ B__
(3)X为非金属Y为金属时,A为__ B为_______
(4)X为非金属,Y为非金属时,A为_____ B为______

(1)X、Y均为金属时,此反应在工业上称为
(2)X为金属,Y为非金属时,A为
(3)X为非金属Y为金属时,A为
(4)X为非金属,Y为非金属时,A为

更新时间:2018-10-21 12:51:28
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】化合物X由三种短周期元素组成,为探究其组成和性质,设计完成如下实验:

已知:a.气体A是相对分子质量最小的气体,可作为新能源;
b.固体C是白色胶状沉淀,溶液D可用作黏合剂和防火剂;
c.反应③恰好消耗0.02 mol NaOH
请回答下列问题:
(1)X的组成元素为Cl和___________ (用元素符号表示)。
(2)写出反应①的化学方程式___________ 。
(3)检验溶液D中所含溶质的金属阳离子的实验方法是:___________ 。

已知:a.气体A是相对分子质量最小的气体,可作为新能源;
b.固体C是白色胶状沉淀,溶液D可用作黏合剂和防火剂;
c.反应③恰好消耗0.02 mol NaOH
请回答下列问题:
(1)X的组成元素为Cl和
(2)写出反应①的化学方程式
(3)检验溶液D中所含溶质的金属阳离子的实验方法是:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】物质A~L有如图转化关系,其中A为用途广泛的金属,其合金是制造飞机和宇宙飞船的理想材料,D、E为气体单质。已知一般情况下,难溶性氢氧化物在加热条件下会分解为对应的氧化物和水。试回答下列问题。
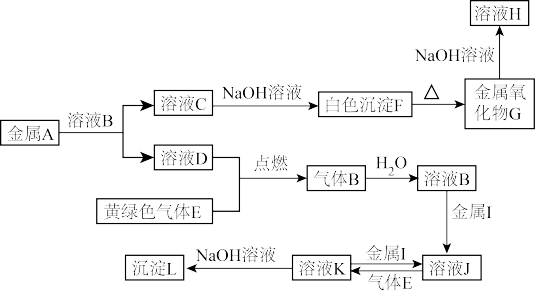
(1)金属A为___________ ,(填写化学式,下同)气体B为___________ ,沉淀L为___________ 。
(2)写出G→H的离子方程式:___________ 。
(3)写出J→K的离子方程式:___________ 。
(4)检验溶液H中的金属阳离子的方法是___________ 。
(5)向200 mL 3 mol·L-1溶液K中加入60 g铁、铜混合物(铁和铜的物质的量之比为1∶1),充分反应后过滤,所得滤液中溶质的物质的量为___________ 。

(1)金属A为
(2)写出G→H的离子方程式:
(3)写出J→K的离子方程式:
(4)检验溶液H中的金属阳离子的方法是
(5)向200 mL 3 mol·L-1溶液K中加入60 g铁、铜混合物(铁和铜的物质的量之比为1∶1),充分反应后过滤,所得滤液中溶质的物质的量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有图示的转换关系, 已知C为密度最小的气体。根据图示转化关系回答:
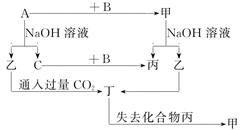
(1)若甲是电解质。写出下列物质的化学式:甲______________ ,丁_______________ 。
写出乙与过量CO2反应的离子方程式:____________________________________________ 。
(2)若甲是非电解质。写出下列物质的化学式:甲_______________ ,乙______________ 。

(1)若甲是电解质。写出下列物质的化学式:甲
写出乙与过量CO2反应的离子方程式:
(2)若甲是非电解质。写出下列物质的化学式:甲
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】晶体硅(熔点1410℃)是良好的半导体材料。由粗硅制纯硅的过程如下:
I.高温下用过量的碳还原二氧化硅制得粗硅;
II.粗硅与干燥的HCl气体反应制得SiHCl3(Si+3HCl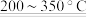 SiHCl3+H2);
SiHCl3+H2);
III.SiHCl3与过量的H2在1100~1200℃的温度下反应制得纯硅,已知SiHCl3能与水剧烈反应。
(1)第一步用焦炭与石英砂制取粗硅,其反应的化学方程式为_______ ;上述反应中的氧化剂是_______ ,还原剂是_______ 。
(2)粗硅与HCl气体反应完全后,经冷凝得到的SiHCl3(沸点33.0℃)中含有少量SiCl4(沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHCl3采用的方法为_______ 。
(3)实验室用SiHCl3与过量的H2反应制取纯硅装置如图所示(加热和夹持装置略去):

①装置B中的试剂是_______ ,装置C中的烧杯需要加热,目的是_______ 。
②反应一段时间后,装置D中观察到的现象是_______ ,装置D不能采用普通玻璃管的原因是_______ ,装置D中发生反应的化学方程式是_______ 。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及_____ 。
I.高温下用过量的碳还原二氧化硅制得粗硅;
II.粗硅与干燥的HCl气体反应制得SiHCl3(Si+3HCl
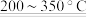 SiHCl3+H2);
SiHCl3+H2);III.SiHCl3与过量的H2在1100~1200℃的温度下反应制得纯硅,已知SiHCl3能与水剧烈反应。
(1)第一步用焦炭与石英砂制取粗硅,其反应的化学方程式为
(2)粗硅与HCl气体反应完全后,经冷凝得到的SiHCl3(沸点33.0℃)中含有少量SiCl4(沸点57.6℃)和HCl(沸点-84.7℃),提纯SiHCl3采用的方法为
(3)实验室用SiHCl3与过量的H2反应制取纯硅装置如图所示(加热和夹持装置略去):

①装置B中的试剂是
②反应一段时间后,装置D中观察到的现象是
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】叠氮化钠( )常用作汽车安全气囊中的药剂。实验室制取叠氮化钠的原理、实验装置及实验步骤如图:
)常用作汽车安全气囊中的药剂。实验室制取叠氮化钠的原理、实验装置及实验步骤如图:

①打开装置D导管上的旋塞,加热制取氨气。
②再加热装置A中的金属钠,使其熔化并与氨气充分反应后,停止加热装置D并关闭旋塞。
③向装置A中b容器内充入加热介质并加热到210∼220℃,然后通入 。
。
④冷却,向产物中加入乙醇(降低 的溶解度),减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。
的溶解度),减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。
已知:Ⅰ. 是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;
是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;
Ⅱ. 熔点210℃,沸点400℃,在水溶液中易水解。
熔点210℃,沸点400℃,在水溶液中易水解。
请回答下列问题:
(1)装置B中盛放的药品为_______ ;步骤①中先加热通 一段时间的目的是
一段时间的目的是_______ 。
(2)步骤②氨气与熔化的钠反应生成 的化学方程式为
的化学方程式为_______ 。
(3)生成 的化学方程式为
的化学方程式为_______ 。
(4)图中仪器a用的是铁质而不用玻璃,其主要原因是_______ 。
(5)步骤④中用乙醚洗涤的主要目的是_______ 。
(6)汽车经撞击后30毫秒内,会引发 迅速分解成两种单质,其中氧化产物和还原产物的质量之比为
迅速分解成两种单质,其中氧化产物和还原产物的质量之比为_______ 。
 )常用作汽车安全气囊中的药剂。实验室制取叠氮化钠的原理、实验装置及实验步骤如图:
)常用作汽车安全气囊中的药剂。实验室制取叠氮化钠的原理、实验装置及实验步骤如图:
①打开装置D导管上的旋塞,加热制取氨气。
②再加热装置A中的金属钠,使其熔化并与氨气充分反应后,停止加热装置D并关闭旋塞。
③向装置A中b容器内充入加热介质并加热到210∼220℃,然后通入
 。
。④冷却,向产物中加入乙醇(降低
 的溶解度),减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。
的溶解度),减压浓缩结晶后,再过滤,并用乙醚洗涤,晾干。已知:Ⅰ.
 是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;
是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚;Ⅱ.
 熔点210℃,沸点400℃,在水溶液中易水解。
熔点210℃,沸点400℃,在水溶液中易水解。请回答下列问题:
(1)装置B中盛放的药品为
 一段时间的目的是
一段时间的目的是(2)步骤②氨气与熔化的钠反应生成
 的化学方程式为
的化学方程式为(3)生成
 的化学方程式为
的化学方程式为(4)图中仪器a用的是铁质而不用玻璃,其主要原因是
(5)步骤④中用乙醚洗涤的主要目的是
(6)汽车经撞击后30毫秒内,会引发
 迅速分解成两种单质,其中氧化产物和还原产物的质量之比为
迅速分解成两种单质,其中氧化产物和还原产物的质量之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某学习小组用如图所示装置测定铝镁合金中铝的质量分数和铝的相对原子质量。

(1)A中试剂为___________________________________________ 。
(2)B中发生反应的化学方程式为______________________________________ 。
(3)若实验用铝镁合金的质量为a g,测得氢气体积为b mL(已换算为标准状况),B中剩余固体的质量为c g,则铝的相对原子质量为________ 。
(4)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将________ (填“偏大”“偏小”或“不受影响”)。

(1)A中试剂为
(2)B中发生反应的化学方程式为
(3)若实验用铝镁合金的质量为a g,测得氢气体积为b mL(已换算为标准状况),B中剩余固体的质量为c g,则铝的相对原子质量为
(4)实验过程中,若未洗涤过滤所得的不溶物,则测得铝的质量分数将
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某实验小组想验证Mg粉和CO2的反应,请从下图中选用所需的仪器(可重复选用)组成一套进行该实验的装置。现提供浓H2SO4、稀盐酸、镁粉、大理石、澄清石灰水,饱和NaHCO3溶液、饱和Na2CO3溶液。(连接和固定仪器用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)。
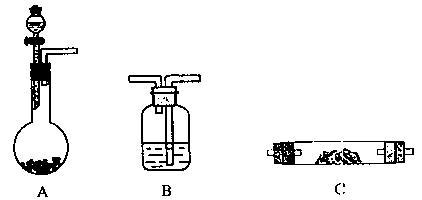
(1)将所选的仪器按连接顺序由上至下依次填入下表,并写出该仪器中应加的试剂__ (可不填满)
(2)A中发生反应的离子方程式为________________________ 。
(3)组装好仪器,检查气密性良好,加入药品。在加热反应管C之前应进行的操作和目的是
__________________________________________________ 。
(4)反应中C装置的主要现象是__________________________________ 。

(1)将所选的仪器按连接顺序由上至下依次填入下表,并写出该仪器中应加的试剂
| 选用的仪器(填字母) | 加入的试剂 |
| A | 稀盐酸、大理石 |
(3)组装好仪器,检查气密性良好,加入药品。在加热反应管C之前应进行的操作和目的是
(4)反应中C装置的主要现象是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A为常见金属,D、E为常见非金属单质,D为黑色固体,E是常温下密度最小的气体,B、F是同种非金属化合物气体,A与氧气转化为C的过程中发出耀眼的白光,A→F之间的转化关系如图:按要求完成下列各题:

(1)写出A与F的化学式:A_______ F_______
(2)下列物质中有一种与B物质不属于同一类,其他与B均属于同一类,这一物质是_______
A.P2O5 B.NO C.Na2O D.SiO2
(3)D高温情况下与水蒸气恰好完全反应生成E和F时,所得气体的平均相对分子质量是_____ g/mol
(4)写出反应①的方程式:_______

(1)写出A与F的化学式:A
(2)下列物质中有一种与B物质不属于同一类,其他与B均属于同一类,这一物质是
A.P2O5 B.NO C.Na2O D.SiO2
(3)D高温情况下与水蒸气恰好完全反应生成E和F时,所得气体的平均相对分子质量是
(4)写出反应①的方程式:
您最近一年使用:0次
【推荐1】四氧化三铁俗称为磁性氧化铁,通常用作颜料、抛光剂和电讯器材等。某化学兴趣小组取磁性氧化铁进行铝热反应实验并对产物进行探究。

(1)取磁性氧化铁按图装置进行铝热反应,引发铝热反应的实验操作是__________ 。
(2)取少许反应生成的“铁块”溶于盐酸,滴加硫氰化钾溶液后溶液不变红,则______ (填“能”或“不能”)说明“铁块”一定不含四氧化三铁,理由是_________ 。
(3)设计一个简单的实验方案,证明上述所得的“铁块”中含有金属铝,该实验所用的试剂是__________ ,反应的离子方程式为___________ 。
(4)请写出此铝热反应的化学方程式:_____________ 。

(1)取磁性氧化铁按图装置进行铝热反应,引发铝热反应的实验操作是
(2)取少许反应生成的“铁块”溶于盐酸,滴加硫氰化钾溶液后溶液不变红,则
(3)设计一个简单的实验方案,证明上述所得的“铁块”中含有金属铝,该实验所用的试剂是
(4)请写出此铝热反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】人类的生产、生活离不开化学。
(1)铝粉与某些金属的氧化物组成的混合物叫铝热剂,铝热剂在高温下发生的反应叫铝热反应,如: ,反应发生时放出大量的热。
,反应发生时放出大量的热。
①信息中的“某些”指___________ (填“比铝活泼”“比铝不活泼”或“任意”)。
②试写出铝粉与 发生铝热反应的化学方程式:
发生铝热反应的化学方程式:___________ 。
(2)从海水中提取溴的工业流程如图:
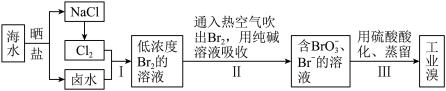
①步骤Ⅰ中发生反应的离子方程式为___________ 。
②步骤Ⅱ用热空气吹出的 被纯碱溶液吸收时,被氧化和被还原的
被纯碱溶液吸收时,被氧化和被还原的 的物质的量之比为
的物质的量之比为___________ 。
(3)海带中含有丰富的碘元素,某化学研究性学习小组用如图流程从海水中提取碘:

①若操作Ⅰ用 溶液(稀硫酸酸化)完成碘元素的转化,则反应的离子方程式为
溶液(稀硫酸酸化)完成碘元素的转化,则反应的离子方程式为___________ 。
②操作Ⅱ的名称为___________ 、___________ ,此过程中可以选用的有机溶剂是___________ (填一种)。
(1)铝粉与某些金属的氧化物组成的混合物叫铝热剂,铝热剂在高温下发生的反应叫铝热反应,如:
 ,反应发生时放出大量的热。
,反应发生时放出大量的热。①信息中的“某些”指
②试写出铝粉与
 发生铝热反应的化学方程式:
发生铝热反应的化学方程式:(2)从海水中提取溴的工业流程如图:

①步骤Ⅰ中发生反应的离子方程式为
②步骤Ⅱ用热空气吹出的
 被纯碱溶液吸收时,被氧化和被还原的
被纯碱溶液吸收时,被氧化和被还原的 的物质的量之比为
的物质的量之比为(3)海带中含有丰富的碘元素,某化学研究性学习小组用如图流程从海水中提取碘:

①若操作Ⅰ用
 溶液(稀硫酸酸化)完成碘元素的转化,则反应的离子方程式为
溶液(稀硫酸酸化)完成碘元素的转化,则反应的离子方程式为②操作Ⅱ的名称为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
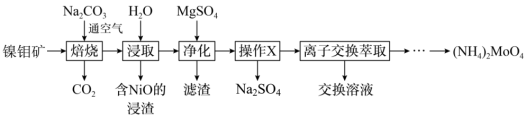
【推荐3】钼(Mo)及其化合物广泛地应用于医疗卫生、国防等领域。某镍钼矿中的镍和钼以 和
和 形式存在,从镍钼矿中分离钼,并得到
形式存在,从镍钼矿中分离钼,并得到 的一种工艺流程。
的一种工艺流程。
已知“浸取”过程中发生如下反应: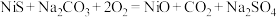
(1) 位于元素周期表第
位于元素周期表第________ 周期第________ 族。
(2)“焙烧”中生成 的反应如下所示,请配平该化学方程式
的反应如下所示,请配平该化学方程式______ 。

上述反应中共价化合物的中心原子杂化方式是________ 杂化。
(3)下列说法正确的是________。(不定项)
 用量对钼浸出率和浸取液中
用量对钼浸出率和浸取液中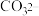 浓度的影响如左下图所示,
浓度的影响如左下图所示, 的溶解度曲线如右下图所示。
的溶解度曲线如右下图所示。

(4)分析实际生产中选择用量为理论用量1.2倍的原因是:________________ 。
(5)为充分分离 ,工艺流程中的“操作
,工艺流程中的“操作 ”应为________。
”应为________。
(6)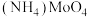 中存在的相互作用有________。
中存在的相互作用有________。
(7)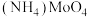 分解可得
分解可得 。高温下,用铝粉还原
。高温下,用铝粉还原 得到金属钼的化学方程式为:
得到金属钼的化学方程式为:________________ 。
 和
和 形式存在,从镍钼矿中分离钼,并得到
形式存在,从镍钼矿中分离钼,并得到 的一种工艺流程。
的一种工艺流程。已知“浸取”过程中发生如下反应:
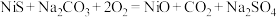

(1)
 位于元素周期表第
位于元素周期表第(2)“焙烧”中生成
 的反应如下所示,请配平该化学方程式
的反应如下所示,请配平该化学方程式
上述反应中共价化合物的中心原子杂化方式是
(3)下列说法正确的是________。(不定项)
A.电负性: | B.离子半径: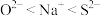 |
C.第一电离能: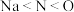 | D.基态 的简化电子排布式 的简化电子排布式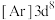 |
 用量对钼浸出率和浸取液中
用量对钼浸出率和浸取液中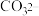 浓度的影响如左下图所示,
浓度的影响如左下图所示, 的溶解度曲线如右下图所示。
的溶解度曲线如右下图所示。
(4)分析实际生产中选择用量为理论用量1.2倍的原因是:
(5)为充分分离
 ,工艺流程中的“操作
,工艺流程中的“操作 ”应为________。
”应为________。| A.蒸发结晶 | B.低温结晶 | C.蒸馏 | D.萃取 |
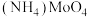 中存在的相互作用有________。
中存在的相互作用有________。| A.分子间作用力 | B.金属键 | C.共价键 | D.离子键 |
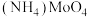 分解可得
分解可得 。高温下,用铝粉还原
。高温下,用铝粉还原 得到金属钼的化学方程式为:
得到金属钼的化学方程式为:
您最近一年使用:0次