向17.6g Cu和CuO组成的混合物中,加入100mL6.0mol·L1稀硝酸溶液,恰好使混合物完全溶解,同时收集到标准状况下NO 2.24L。请回答以下问题:
(1)写出Cu与稀硝酸反应的离子方程式______________________________________ 。
(2)原混合物中铜的质量为______ g。
(3)氧化铜的质量为______ g。
(1)写出Cu与稀硝酸反应的离子方程式
(2)原混合物中铜的质量为
(3)氧化铜的质量为
更新时间:2018-11-15 14:08:46
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】现有一份部分被氧化的铜片(氧化产物为CuO),称取8.64 g该铜片,溶于280 mL 1.00 mol⋅L 稀硝酸中,反应恰好完全进行,收集到无色气体896 mL(已折算为标准状况)。
稀硝酸中,反应恰好完全进行,收集到无色气体896 mL(已折算为标准状况)。
(1)该稀硝酸中所含硝酸的物质的量为___________ 。
(2)8.64 g铜片中CuO的质量为___________ 。
(3)该铜片中,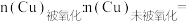
___________ 。
 稀硝酸中,反应恰好完全进行,收集到无色气体896 mL(已折算为标准状况)。
稀硝酸中,反应恰好完全进行,收集到无色气体896 mL(已折算为标准状况)。(1)该稀硝酸中所含硝酸的物质的量为
(2)8.64 g铜片中CuO的质量为
(3)该铜片中,
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】取m克铁粉与1 L 1.2 mol/L的稀HNO3恰好完全反应,反应后的溶液中只含Fe2+且硝酸的还原产物只有NO。则:
(1)m=______________ g。
(2)若将反应后的溶液低温蒸干,析出晶体135 g,则析出晶体的组成可能是_________ 。
a.Fe(NO3)2∙7H2O和Fe(NO3)2∙4H2O
b.Fe(NO3)2∙7H2O和Fe(NO3)2∙H2O
c.Fe(NO3)2∙4H2O和Fe(NO3)2∙H2O
(3)若向反应后的溶液中加入100 mL 1.5 mol/L的稀H2SO4,则标准状态下还能产生NO的体积为______ L。
(1)m=
(2)若将反应后的溶液低温蒸干,析出晶体135 g,则析出晶体的组成可能是
a.Fe(NO3)2∙7H2O和Fe(NO3)2∙4H2O
b.Fe(NO3)2∙7H2O和Fe(NO3)2∙H2O
c.Fe(NO3)2∙4H2O和Fe(NO3)2∙H2O
(3)若向反应后的溶液中加入100 mL 1.5 mol/L的稀H2SO4,则标准状态下还能产生NO的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】ag铁粉和铜粉的混合物加入到100mLbmol•L-1FeCl3溶液中,固体全部溶解,再向此溶液中不断加入铁粉,当铁粉质量加至0.1ag后开始有固体析出,当铁粉加至ag时,剩余固体质量为ag。
(1)a与b的关系为___
(2)ag铁粉和铜粉的混合物中铁粉的质量为___ g(用含a的式子表示)。
(1)a与b的关系为
(2)ag铁粉和铜粉的混合物中铁粉的质量为
您最近一年使用:0次
【推荐2】某合金(仅含铜、铁)中铜和铁的物质的量之和为amol,其中Cu的物质的量分数为b,将其全部投入100mLcmol•L-1的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物)。
(1)若金属全部溶解,则溶液中___ (填“一定”或“不一定")含有Fe3+。
(2)若金属全部溶解,且产生448mL气体(标准状况),则c≥___ 。
(3)若溶液中金属离子只有Fe3+、Cu2+时,则c≥___ (用含a和b的式子表示)。
(1)若金属全部溶解,则溶液中
(2)若金属全部溶解,且产生448mL气体(标准状况),则c≥
(3)若溶液中金属离子只有Fe3+、Cu2+时,则c≥
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
名校
【推荐1】称取4.00g氧化铜和氧化铁固体混合物,加入50.0mL2.00mol·L-1的硫酸充分溶解,往所得溶液中加入5.60g铁粉,充分反应后,得固体的质量为3.04g。请计算:
(1)加入铁粉充分反应后,溶液中溶质的物质的量_________________ 。
(2)固体混合物中氧化铜的质量_________________ 。
(1)加入铁粉充分反应后,溶液中溶质的物质的量
(2)固体混合物中氧化铜的质量
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】取一定量的CuO粉末与0.5 L稀硫酸充分反应后,将一根50 g铁棒插入上述溶液中,至铁棒质量不再变化时,铁棒增重0.24 g, 并收集到224 mL气体(标准状况)。求此CuO粉末的质量____ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】称取铁粉和氧化铜的混合物6.40g,进行如下实验:
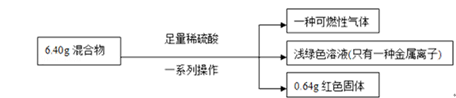
根据实验所得数据,完成下列填空:
(1)原混合物中氧化铜的质量能否确定?____________ (填“能”或“不能”),若能确定,则氧化铜的质量为_________ ;
(2)上述过程中生成气体的名称为_________ ;(折算为标准状况下)的体积为__________ ;
(3)实验中参加反应的硫酸的物质的量为____________ ;
(4)原混合物中铁的质量分数为________ 。

根据实验所得数据,完成下列填空:
(1)原混合物中氧化铜的质量能否确定?
(2)上述过程中生成气体的名称为
(3)实验中参加反应的硫酸的物质的量为
(4)原混合物中铁的质量分数为
您最近一年使用:0次



