稀硝酸和铜反应的化学方程式如下:
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
如果有3.2克铜和硝酸恰好完全反应,试计算:
(1)在标准状况下产生气体的体积是________________ ?
(2)将所得溶液加水配成200mL溶液,则溶液的物质的量浓度是_________ ?
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
如果有3.2克铜和硝酸恰好完全反应,试计算:
(1)在标准状况下产生气体的体积是
(2)将所得溶液加水配成200mL溶液,则溶液的物质的量浓度是
10-11高二上·北京·期末 查看更多[1]
(已下线)2010年北京育园中学高二上学期分班考试化学试题
更新时间:2010-09-20 11:59:54
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】(1)H2SO4的相对分子质量为______ ,它的摩尔质量为______ .
(2)在标准状况下,0.5mol任何气体的体积都约为______ .
(3)4g H2与22.4L(标况)CO2相比,所含分子数目较多的是______ .
(4)0.01mol某气体的质量为0.28g,该气体的摩尔质量为______ ,在标准状况下,该气体的体积是______
(2)在标准状况下,0.5mol任何气体的体积都约为
(3)4g H2与22.4L(标况)CO2相比,所含分子数目较多的是
(4)0.01mol某气体的质量为0.28g,该气体的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】把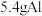 放入
放入 足量氢氧化钠溶液中完全反应,忽略溶液体积变化,试计算:
足量氢氧化钠溶液中完全反应,忽略溶液体积变化,试计算:
(1)生成氢气在标准状况下的体积______________ 。
(2)反应后溶液中四羟基合铝酸钠的物质的量浓度______________ 。
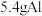 放入
放入 足量氢氧化钠溶液中完全反应,忽略溶液体积变化,试计算:
足量氢氧化钠溶液中完全反应,忽略溶液体积变化,试计算:(1)生成氢气在标准状况下的体积
(2)反应后溶液中四羟基合铝酸钠的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】将一定质量的KOH和Ca(OH)2混合物全部溶于一定量水中形成稀溶液,再缓缓通入CO2气体。生成沉淀的质量随通入CO2的体积(标准状况下)变化如图所示,试计算
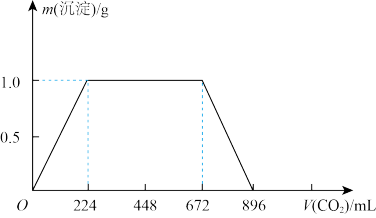
(1)混合物中Ca(OH)2的质量为_________ g
(2)所配溶液中KOH的物质的量为________ mol。

(1)混合物中Ca(OH)2的质量为
(2)所配溶液中KOH的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】浓硫酸与铜在加热时发生反应,生成二氧化硫气体的体积为4.48L(标准状况)。
试计算:
(1)反应后生成硫酸铜的物质的量_______ 。
(2)若将反应后的溶液稀释至500mL,计算该溶液中硫酸铜的物质的量浓度_______ 。
试计算:
(1)反应后生成硫酸铜的物质的量
(2)若将反应后的溶液稀释至500mL,计算该溶液中硫酸铜的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】在18.6g Fe和Zn合金中加入200mL某浓度的稀硫酸恰好完全反应,生成0.3mol H2。则原合金中有_________ mol Fe,稀硫酸的物质的量浓度为__________ mol/L。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)100 mL0.3 mol·L-1 Na2SO4溶液和50 mL0.2 mol·L-1Al2(SO4)3溶液混合后,溶液中 的物质的量浓度约为
的物质的量浓度约为___ (忽略溶液体积变化)。
(2)某结晶水合物的化学式为A·nH2O,其相对分子质量为M,在25℃时,a g晶体溶于b g水中即达饱和,形成密度为ρ g·mL-1的溶液,饱和溶液的物质的量浓度为___ 。
 的物质的量浓度约为
的物质的量浓度约为(2)某结晶水合物的化学式为A·nH2O,其相对分子质量为M,在25℃时,a g晶体溶于b g水中即达饱和,形成密度为ρ g·mL-1的溶液,饱和溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】将20.0 g铜镁合金完全溶解于140 mL某浓度的硝酸中,得到NO2和NO的混合气体8.96 L(标准状况),当向反应后的溶液中加入320 mL 4.0 mol/L NaOH溶液时,金属离子全部转化为沉淀,测得沉淀的质量为37 g。通过计算回答下列问题:
(1)该合金中铜与镁的物质的量之比是_______ 。
(2)该硝酸中HNO3的物质的量浓度是_______ mol/L。
(3)NO2和NO的混合气体中,NO2的体积分数是_______ 。
(4)若将混合气体与水混合完全转化为硝酸,则需要通入的氧气(标准状况)的体积为_______ L。
(1)该合金中铜与镁的物质的量之比是
(2)该硝酸中HNO3的物质的量浓度是
(3)NO2和NO的混合气体中,NO2的体积分数是
(4)若将混合气体与水混合完全转化为硝酸,则需要通入的氧气(标准状况)的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】向Cu和CuO的混合物中加入0.6 L2.0 mol/L的稀硝酸,混合物完全溶解,同时生成标准状况下NO 4.48 L。向所得溶液中加入一定体积1.0 mol/L NaOH溶液,恰好使Cu2+完全沉淀,将沉淀洗涤,充分灼烧后得32.0 g固体。求:
(1)混合物中Cu的质量是____________ 。
(2)混合物消耗HNO3的物质的量是____________ 。
(3)NaOH溶液的体积是____________ 。
(4)Cu2+完全反应后,溶液中NO3-的物质的量浓度是____________ 。
(1)混合物中Cu的质量是
(2)混合物消耗HNO3的物质的量是
(3)NaOH溶液的体积是
(4)Cu2+完全反应后,溶液中NO3-的物质的量浓度是
您最近一年使用:0次

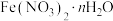 可用作媒染剂、医药、分析试剂、催化剂等,某同学设计实验确定其结晶水数目。用电子天平称取样品17.280g,一定条件下,经热分解测得气体产物中有
可用作媒染剂、医药、分析试剂、催化剂等,某同学设计实验确定其结晶水数目。用电子天平称取样品17.280g,一定条件下,经热分解测得气体产物中有 、
、 、
、 、
、 ,其中水的质量为6.300g,残留的固体产物是
,其中水的质量为6.300g,残留的固体产物是 ,质量为4.800g。
,质量为4.800g。

