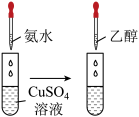
(1)FeCl3是中学实验室常用的试剂,可以用来制备氢氧化铁胶体。
下列制备氢氧化铁胶体的操作方法正确的是____________ (填字母);
A.向饱和氯化铁溶液中滴加少量的氢氧化钠稀溶液
B.加热煮沸氯化铁饱和溶液
C.在氨水中滴加氯化铁浓溶液
D.在沸水中滴加饱和氯化铁溶液,煮沸至液体呈红褐色。
(2)写出Ba(OH)2溶液与少量NaHCO3溶液反应的离子方程式:___________________ 。
(3)写出次氯酸的电子式:________________ ;写出过氧化钠中存在的所有化学键类型:____________________ 。
(4)铁粉中含有铝粉,可加______ 除去杂质,发生的化学方程式为______________ 。
下列制备氢氧化铁胶体的操作方法正确的是
A.向饱和氯化铁溶液中滴加少量的氢氧化钠稀溶液
B.加热煮沸氯化铁饱和溶液
C.在氨水中滴加氯化铁浓溶液
D.在沸水中滴加饱和氯化铁溶液,煮沸至液体呈红褐色。
(2)写出Ba(OH)2溶液与少量NaHCO3溶液反应的离子方程式:
(3)写出次氯酸的电子式:
(4)铁粉中含有铝粉,可加
更新时间:2019-01-23 16:53:18
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)①漂白粉的有效成分的化学式_________________ ;碳酸氢钠的俗称____________________ 。
(2) 的电离方程式
的电离方程式__________________________________________ 。
钠与水反应的离子方程式__________________________________________ 。
(3)向沸水中逐滴加入5~6滴 饱和溶液,继续加热至沸腾,液体呈现
饱和溶液,继续加热至沸腾,液体呈现____________ 色,停止加热,即可制得 胶体。
胶体。
(1)①漂白粉的有效成分的化学式
(2)
 的电离方程式
的电离方程式钠与水反应的离子方程式
(3)向沸水中逐滴加入5~6滴
 饱和溶液,继续加热至沸腾,液体呈现
饱和溶液,继续加热至沸腾,液体呈现 胶体。
胶体。
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有①酒精②石墨③Fe(OH)3胶体④醋酸⑤金刚石⑥熔融NaCl⑦稀硫酸七种物质,若根据物质的组成将它们进行分类,则:
(1)属于混合物的有___________
(2)属于能导电的电解质的有___________
(3)属于非电解质的有___________
(4)②和⑤的关系是___________
(5)制备③的离子方程式___________
(1)属于混合物的有
(2)属于能导电的电解质的有
(3)属于非电解质的有
(4)②和⑤的关系是
(5)制备③的离子方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求回答下列问题:
(1)胶体是一种常见的分散系,将饱和三氯化铁溶液滴入沸水时,得到的液体是______ 色,反应的化学方程式为_______ 。
(2)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2已知该反应中H2O2只发生如下过程:H2O2→O2
①该反应中的氧化剂是________ ,
②该反应中,发生还原反应的过程是___→_____,_____ 。
③写出该反应的化学方程式___________ 。
(1)胶体是一种常见的分散系,将饱和三氯化铁溶液滴入沸水时,得到的液体是
(2)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2已知该反应中H2O2只发生如下过程:H2O2→O2
①该反应中的氧化剂是
②该反应中,发生还原反应的过程是___→_____,
③写出该反应的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】氨气在工农业生产中有重要应用。回答下列问题:
(1)①氮气用于工业合成氨,写出氮气的结构式:___________ ;工业上合成氨气的化学方程式为___________ 。
②NH3的稳定性比PH3___________ (填“强”或“弱”)。
(2)向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。
①浓盐酸液滴附近会出现白烟,发生反应的化学方程式为___________ 。
②浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,该固体可能是___________ (写化学式,一种即可)。
(3)在微生物作用下,蛋白质在水中分解产生的NH3能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为___________ 。
(1)①氮气用于工业合成氨,写出氮气的结构式:
②NH3的稳定性比PH3
(2)向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。
①浓盐酸液滴附近会出现白烟,发生反应的化学方程式为
②浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,该固体可能是
(3)在微生物作用下,蛋白质在水中分解产生的NH3能够被氧气氧化生成亚硝酸(HNO2),反应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】易混易错题组
Ⅰ.使用正确的化学用语填空
(1)写出下列物质的电子式
氮气_______ 过氧化钠 _________ 四氯化碳________
(2)写出下列物质的结构式
二氧化碳________ 过氧化氢 _________ 次氯酸________
(学法题)正确书写化合物的电子式需要注意的问题是_____________
Ⅱ.正确比较下列各组对应关系
(1)已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则这四种元素:
①原子序数由大到小的顺序为:___________
②原子半径由大到小的顺序为:___________
③离子半径由大到小的顺序为:___________
(2)比较下列微粒半径大小,用“>”或“<”填空
①F-________ Cl- ②Fe2+________ Fe3+ ③O2-_________ Mg2+
(学法题)粒子半径大小比较方法(两点即可)___________
Ⅰ.使用正确的化学用语填空
(1)写出下列物质的电子式
氮气
(2)写出下列物质的结构式
二氧化碳
(学法题)正确书写化合物的电子式需要注意的问题是
Ⅱ.正确比较下列各组对应关系
(1)已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则这四种元素:
①原子序数由大到小的顺序为:
②原子半径由大到小的顺序为:
③离子半径由大到小的顺序为:
(2)比较下列微粒半径大小,用“>”或“<”填空
①F-
(学法题)粒子半径大小比较方法(两点即可)
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有下列物质:
①KCl ②CH4 ③NH4NO3 ④I2 ⑤Na2O2 ⑥HClO4 ⑦N2 ⑧CO ⑨SO2 ⑩金刚石 ⑪CH3CH2OH ⑫MgO ⑬MgCl2 ⑭KOH ⑮HCl ⑯Al2O3
请回答下列问题。
(1)两性氧化物是___ (填序号),其电子式为___ 。
(2)最简单的有机化合物是___ (填序号),用电子式表示其形成过程:___ 。
(3)属于共价化合物的是___ (填序号),含有共价键的离子化合物是___ (填序号)。
(4)由两种元素组成,且含有离子键和共价键的化合物为___ (填序号),这两种元素的单质反应生成该化合物的化学方程式为___ 。
①KCl ②CH4 ③NH4NO3 ④I2 ⑤Na2O2 ⑥HClO4 ⑦N2 ⑧CO ⑨SO2 ⑩金刚石 ⑪CH3CH2OH ⑫MgO ⑬MgCl2 ⑭KOH ⑮HCl ⑯Al2O3
请回答下列问题。
(1)两性氧化物是
(2)最简单的有机化合物是
(3)属于共价化合物的是
(4)由两种元素组成,且含有离子键和共价键的化合物为
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)反应Fe2O3+2Al═Al2O3+2Fe在化学上被称为“铝热反应",人们可利用该反应来焊接铁轨,该反应所属基本反应类型是_______ 。在该反应中_______ 元素的化合价升高,该元素的原子_______ 电子,被_______ ;而_______ 元素的化合价降低,该元素的原子_______ 电子,被_______ 。该反应中,Fe2O3发生了_______ 反应,Al发生了_______ 反应,_______ 是氧化剂,_______ 是氧化产物,_______ 是还原剂。
(2)写出Fe2O3与CO在高温下反应的化学方程式,并用双线桥标出电子转移的方向和数目_______ 。
(3)写出Cu和AgNO3溶液反应的离子方程式,并用单线桥标出电子转移的方向和数目_______ 。
(1)反应Fe2O3+2Al═Al2O3+2Fe在化学上被称为“铝热反应",人们可利用该反应来焊接铁轨,该反应所属基本反应类型是
(2)写出Fe2O3与CO在高温下反应的化学方程式,并用双线桥标出电子转移的方向和数目
(3)写出Cu和AgNO3溶液反应的离子方程式,并用单线桥标出电子转移的方向和数目
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铜及其化合物有着广泛的应用。某实验小组探究 的性质。
的性质。
I.实验准备:
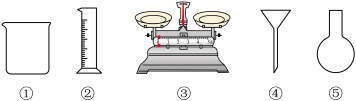
(1)由 固体配制
固体配制 溶液,下列仪器中需要使用的有
溶液,下列仪器中需要使用的有_________ (填序号)。
实验任务:探究 溶液分别与
溶液分别与 、
、 溶液的反应
溶液的反应
查阅资料:
已知:a.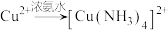 (深蓝色溶液)
(深蓝色溶液)
b. (无色溶液)
(无色溶液) (深蓝色溶液)
(深蓝色溶液)
设计方案并完成实验:
现象分析与验证:
(2)推测实验B产生的无色气体为 ,实验验证:用蘸有碘水的淀粉试纸接近试管口,观察到
,实验验证:用蘸有碘水的淀粉试纸接近试管口,观察到__________ 。
(3)推测实验B中的白色沉淀为 ,实验验证步骤如下:
,实验验证步骤如下:
①实验B完成后,立即过滤、洗涤。
②取少量已洗净的白色沉淀于试管中,滴加足量________ ,观察到沉淀溶解,得到无色溶液,此反应的离子方程式为__________ ;露置在空气中一段时间,观察到溶液变为深蓝色。
(4)对比实验A、B,提出假设: 增强了
增强了 的氧化性。
的氧化性。
①若假设合理,实验B反应的离子方程式为
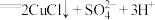 和
和__________ 。
②下述实验C证实了假设合理,装置如图8(两个电极均为碳棒)。实验方案:闭合K,电压表的指针偏转至“X”处;向U形__________ (补全实验操作及现象)。
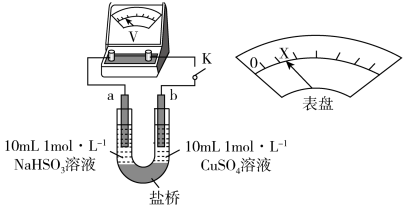
Ⅱ. 能与
能与 、
、 、
、 、
、 等形成配位数为4的配合物。
等形成配位数为4的配合物。
(5)硫酸铜溶液呈蓝色的原因是溶液中存在配离子_________ (填化学式)。
(6)常见配合物的形成实验
 的性质。
的性质。I.实验准备:
(1)由
 固体配制
固体配制 溶液,下列仪器中需要使用的有
溶液,下列仪器中需要使用的有
实验任务:探究
 溶液分别与
溶液分别与 、
、 溶液的反应
溶液的反应查阅资料:
已知:a.
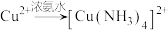 (深蓝色溶液)
(深蓝色溶液)b.
 (无色溶液)
(无色溶液) (深蓝色溶液)
(深蓝色溶液)设计方案并完成实验:
实验 | 装置 | 试剂x | 操作及现象 |
A |
| 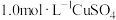 溶液 溶液 | 加入  溶液,得到绿色溶液, 溶液,得到绿色溶液, 未见明显变化。 未见明显变化。 |
B | 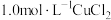 溶液 溶液 | 加入  溶液,得到绿色溶液, 溶液,得到绿色溶液, 时有无色气泡和白色沉淀产生,上层溶液颜色变浅。 时有无色气泡和白色沉淀产生,上层溶液颜色变浅。 |
(2)推测实验B产生的无色气体为
 ,实验验证:用蘸有碘水的淀粉试纸接近试管口,观察到
,实验验证:用蘸有碘水的淀粉试纸接近试管口,观察到(3)推测实验B中的白色沉淀为
 ,实验验证步骤如下:
,实验验证步骤如下:①实验B完成后,立即过滤、洗涤。
②取少量已洗净的白色沉淀于试管中,滴加足量
(4)对比实验A、B,提出假设:
 增强了
增强了 的氧化性。
的氧化性。①若假设合理,实验B反应的离子方程式为

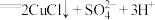 和
和②下述实验C证实了假设合理,装置如图8(两个电极均为碳棒)。实验方案:闭合K,电压表的指针偏转至“X”处;向U形

Ⅱ.
 能与
能与 、
、 、
、 、
、 等形成配位数为4的配合物。
等形成配位数为4的配合物。(5)硫酸铜溶液呈蓝色的原因是溶液中存在配离子
(6)常见配合物的形成实验
实验操作 | 实验现象 | 有关离子方程式 |
| 滴加氨水后,试管中首先出现蓝色沉淀,氨水过量后沉淀逐渐 |  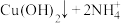   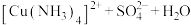 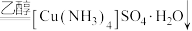 |
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】2021年9月20日是第33个“全国爱牙日”。为了防止龋齿,正确的刷牙方式和选用适宜的牙膏很重要。


(1)牙膏中的摩擦剂碳酸钙可以用石灰石来制备。某同学设计了一种实验室制备碳酸钙的实验方案,其流程图如下:
石灰石 生石灰
生石灰 石灰水
石灰水 碳酸钙
碳酸钙
请写出上述方案中反应③的离子方程式:___________ 。
(2)请你仍用石灰石作为原料(其他试剂自选),设计实验室制备碳酸钙的另一种实验方案。依照(1)所示,将你的实验方案用流程图表示出来:石灰石→___________ ,你设计的方案的优点为___________ 。(答出两条)


(1)牙膏中的摩擦剂碳酸钙可以用石灰石来制备。某同学设计了一种实验室制备碳酸钙的实验方案,其流程图如下:
石灰石
 生石灰
生石灰 石灰水
石灰水 碳酸钙
碳酸钙请写出上述方案中反应③的离子方程式:
(2)请你仍用石灰石作为原料(其他试剂自选),设计实验室制备碳酸钙的另一种实验方案。依照(1)所示,将你的实验方案用流程图表示出来:石灰石→
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求写出下列反应的化学方程式或离子方程式
(1)钢铁工业是国家工业的基础。请回答:
①写出由CO还原赤铁矿(主要成分为Fe2O3)的化学方程式:________________ 。
②在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。
写出铁粉和水蒸气反应的化学方程式:___________________ 。
(2)铝片放入NaOH溶液中有气体生成,写出反应的离子方程式:__________ 。
(1)钢铁工业是国家工业的基础。请回答:
①写出由CO还原赤铁矿(主要成分为Fe2O3)的化学方程式:
②在一定条件下用普通铁粉和水蒸气反应,可以得到铁的氧化物。
写出铁粉和水蒸气反应的化学方程式:
(2)铝片放入NaOH溶液中有气体生成,写出反应的离子方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铝和铁是中学化学常见的金属。请回答下列问题:
(1)常温下,铝和铁放入浓HNO3中会发生_______ ;
A.都反应产生氢气B.只有铝反应产生氢气
C.只有铁反应产生氢气D.都钝化
(2)常温下,铝粉和铁粉分别放入氢氧化钠溶液中,能反应产生氢气的是_______ ,
(3)铝热反应的化学方程式:2Al+Fe2O3 2Fe+Al2O3,其氧化剂是
2Fe+Al2O3,其氧化剂是_________ 。
A.AlB.FeC.Fe2O3D.Al2O3
(1)常温下,铝和铁放入浓HNO3中会发生
A.都反应产生氢气B.只有铝反应产生氢气
C.只有铁反应产生氢气D.都钝化
(2)常温下,铝粉和铁粉分别放入氢氧化钠溶液中,能反应产生氢气的是
(3)铝热反应的化学方程式:2Al+Fe2O3
 2Fe+Al2O3,其氧化剂是
2Fe+Al2O3,其氧化剂是A.AlB.FeC.Fe2O3D.Al2O3
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.写出下列反应的离子方程式:
(1)CuSO4溶液与Ba(OH)2溶液混合:___________ 。
(2)鸡蛋壳(主要成份为碳酸钙)溶解在盐酸中:___________ 。
(3)铝片溶解在氢氧化钠溶液中:___________ 。
Ⅱ.对一份稀溶液作初步分析后发现,溶液无色、澄清,其中可能含有 、Na+、
、Na+、 、H+、
、H+、 、
、 、Cl-中的若干种。然后又作了如下分析,以确定这些离子是否存在。
、Cl-中的若干种。然后又作了如下分析,以确定这些离子是否存在。
①用石蕊试液检测该溶液时,溶液显红色。
②取2 mL该溶液加入稀硝酸酸化的BaCl2溶液,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。
请回答下列问题:
(4)原溶液中一定存在的离子是___________ ,一定不存在的离子是___________ 。
(5)按上述实验操不能确定原溶液中有Cl-,请说明原因:___________ 。
(1)CuSO4溶液与Ba(OH)2溶液混合:
(2)鸡蛋壳(主要成份为碳酸钙)溶解在盐酸中:
(3)铝片溶解在氢氧化钠溶液中:
Ⅱ.对一份稀溶液作初步分析后发现,溶液无色、澄清,其中可能含有
 、Na+、
、Na+、 、H+、
、H+、 、
、 、Cl-中的若干种。然后又作了如下分析,以确定这些离子是否存在。
、Cl-中的若干种。然后又作了如下分析,以确定这些离子是否存在。①用石蕊试液检测该溶液时,溶液显红色。
②取2 mL该溶液加入稀硝酸酸化的BaCl2溶液,结果生成了白色沉淀。
③对②中所得的混合物充分静置后,取其上层澄清的液体用AgNO3溶液和稀硝酸进行检验,结果又生成了白色沉淀。
请回答下列问题:
(4)原溶液中一定存在的离子是
(5)按上述实验操不能确定原溶液中有Cl-,请说明原因:
您最近半年使用:0次



 溶液
溶液