有一包白色固体,可能含有Na2CO3、KNO3、KCl、BaCl2和CuSO4,按下列步骤做实验。①将该固体溶于水得无色溶液。②向溶液中加入AgNO3溶液,得到白色沉淀,再加稀HNO3,白色沉淀部分溶解并有气泡产生,把气体通入澄清石灰水,石灰水变浑浊。根据现象判断:
(1)一定存在的物质是________ 。
(2)一定不存在的物质是________ 。
(3)可能存在的物质是________ 。
(1)一定存在的物质是
(2)一定不存在的物质是
(3)可能存在的物质是
2019高三·全国·专题练习 查看更多[2]
更新时间:2019-02-16 16:58:03
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】试分析回答下列有关实验与计算问题:
(1)利用反应Ca2++H2O2+2NH3+8H2O=CaO2∙8H2O↓+2 ,在碱性环境下制取CaO2∙8H2O的装置如图:
,在碱性环境下制取CaO2∙8H2O的装置如图:
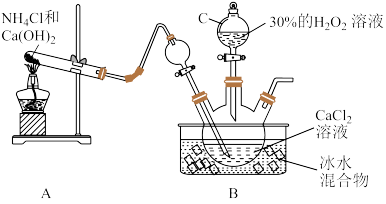
①仪器C的名称为_______ ;反应结束后,经_______ (填操作名称)、洗涤、低温烘干可获得CaO2∙8H2O。
②装置B中用冰水浴控制温度,其可能的原因是_______ 。
(2)S2Cl2遇水会生成SO2、HCl两种气体,某同学设计了如图所示实验方案来测定该混合气体中SO2的体积分数。
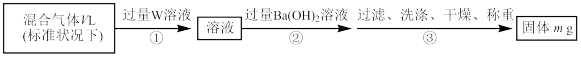
①W溶液可以是_______ (填序号)。
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为_______ (用含V、m的式子表示)。
(1)利用反应Ca2++H2O2+2NH3+8H2O=CaO2∙8H2O↓+2
 ,在碱性环境下制取CaO2∙8H2O的装置如图:
,在碱性环境下制取CaO2∙8H2O的装置如图:
①仪器C的名称为
②装置B中用冰水浴控制温度,其可能的原因是
(2)S2Cl2遇水会生成SO2、HCl两种气体,某同学设计了如图所示实验方案来测定该混合气体中SO2的体积分数。
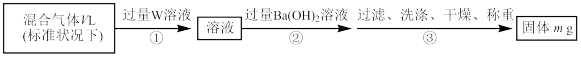
①W溶液可以是
a.H2O2溶液 b.KMnO4溶液(硫酸酸化) c.氯水
②该混合气体中二氧化硫的体积分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】硫和氮及其化合物在生产生活中应用广泛,含氮氧化物和硫氧化物的尾气需处理后才能排放。请回答下列问题:
(1)下列装置可用于实验室吸收尾气中SO2的是__________  填标号
填标号 。
。

(2)实验室有一瓶放置很久的Na2SO3固体药品,小明同学想设计一个实验验证这瓶药品是否变质?请你帮助他设计一个实验__________ 。
(3)用Cu与HNO3和H2SO4的混合酸反应制备CuSO4,则参加反应的HNO3和H2SO4物质的量之比为__________
(4)利用氨水可以将SO2和NO2吸收,原理如图所示:

NO2被吸收的离子方程式是__________ 。
(5)若32.0gCu与一定量的HNO3溶液反应,当Cu反应完时,共产生标准状况下的13.44L气体(NO和NO2),则消耗的HNO3溶液中溶质的物质的量为__________ 。
(6)在酸性NaClO溶液中,HClO氧化NO生成Cl-和 。其他条件相同,NO转化为
。其他条件相同,NO转化为 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。NaClO溶液的初始pH越小,NO转化率越高。其原因是
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。NaClO溶液的初始pH越小,NO转化率越高。其原因是__________ 。
(1)下列装置可用于实验室吸收尾气中SO2的是
 填标号
填标号 。
。
(2)实验室有一瓶放置很久的Na2SO3固体药品,小明同学想设计一个实验验证这瓶药品是否变质?请你帮助他设计一个实验
(3)用Cu与HNO3和H2SO4的混合酸反应制备CuSO4,则参加反应的HNO3和H2SO4物质的量之比为
(4)利用氨水可以将SO2和NO2吸收,原理如图所示:

NO2被吸收的离子方程式是
(5)若32.0gCu与一定量的HNO3溶液反应,当Cu反应完时,共产生标准状况下的13.44L气体(NO和NO2),则消耗的HNO3溶液中溶质的物质的量为
(6)在酸性NaClO溶液中,HClO氧化NO生成Cl-和
 。其他条件相同,NO转化为
。其他条件相同,NO转化为 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。NaClO溶液的初始pH越小,NO转化率越高。其原因是
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。NaClO溶液的初始pH越小,NO转化率越高。其原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】食盐是生活必需品,也是一种工业原料。粗盐含有 、
、 、
、 等杂质。
等杂质。
(1)“粗盐→精盐”过程:
①“除杂1”中反应的离子方程式为____ 。
②试剂X为____ (填化学式)。
③该过程中不涉及的实验操作是____ (填标号)。
A.溶解 B.过滤 C.蒸发 D.渗析
(2)用精盐配制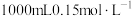 生理盐水的过程:
生理盐水的过程:
①用托盘天平称取 固体的质量为
固体的质量为____ g。
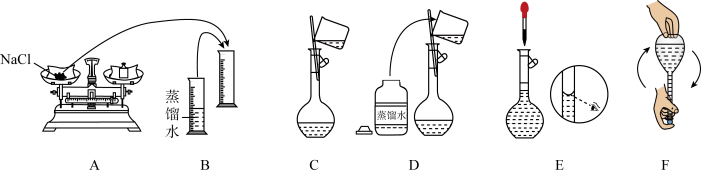
②下列关于配制溶液过程中操作不正确的是_______ (填标号)。 ”过程:
”过程:
①将电解过程发生反应的化学方程式补充完整:______ ,__ ___
___ __
__ __
__ 。
。
②在一定条件下 与盐酸反应生成消毒剂
与盐酸反应生成消毒剂 。“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克
。“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克 的氧化能力。则
的氧化能力。则 的有效氯含量为
的有效氯含量为______ g。
 、
、 、
、 等杂质。
等杂质。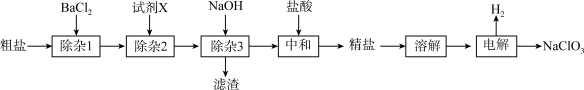
(1)“粗盐→精盐”过程:
①“除杂1”中反应的离子方程式为
②试剂X为
③该过程中不涉及的实验操作是
A.溶解 B.过滤 C.蒸发 D.渗析
(2)用精盐配制
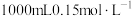 生理盐水的过程:
生理盐水的过程:①用托盘天平称取
 固体的质量为
固体的质量为②下列关于配制溶液过程中操作不正确的是
 ”过程:
”过程:①将电解过程发生反应的化学方程式补充完整:
 ___
___ __
__ __
__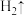 。
。②在一定条件下
 与盐酸反应生成消毒剂
与盐酸反应生成消毒剂 。“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克
。“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克 的氧化能力。则
的氧化能力。则 的有效氯含量为
的有效氯含量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】镁与钠都是活泼的金属单质,能与很多物质反应。
(1)点燃一小段已擦去氧化膜的镁条,伸入到充满二氧化碳的集气瓶中,反应剧烈,发生了置换反应。该反应的化学方程式是___________ 。
(2)为探究金属钠能否与二氧化碳反应,进行如下实验:

a.将一小块金属钠在燃烧匙中点燃,迅速伸入盛有二氧化碳的集气瓶中,如图所示,充分反应,放置冷却。
b.在集气瓶中加入适量蒸馏水,振荡,过滤。
①步骤a中观察到生成大量白烟,集气瓶底部有黑色固体产生,瓶壁有白色物质产生。甲同学取适量该白色物质溶于水得到溶液A,进行如下实验,推断出集气瓶瓶壁上白色物质主要是Na2CO3
请完成下列表格:
现象1是___________ ,溶液B可能是___________ (写出一种即可)。
②步骤b中观察到滤液为无色溶液,滤纸上留有黑色固体。乙同学从元素守恒的角度,可推测该黑色固体可能是___________ 。
(3)金属钠在700℃时与CCl4生成纳米级金刚石粉末(用C表示)。写出反应的化学方程式并表示该反应电子转移的方向和数目:___________
(1)点燃一小段已擦去氧化膜的镁条,伸入到充满二氧化碳的集气瓶中,反应剧烈,发生了置换反应。该反应的化学方程式是
(2)为探究金属钠能否与二氧化碳反应,进行如下实验:

a.将一小块金属钠在燃烧匙中点燃,迅速伸入盛有二氧化碳的集气瓶中,如图所示,充分反应,放置冷却。
b.在集气瓶中加入适量蒸馏水,振荡,过滤。
①步骤a中观察到生成大量白烟,集气瓶底部有黑色固体产生,瓶壁有白色物质产生。甲同学取适量该白色物质溶于水得到溶液A,进行如下实验,推断出集气瓶瓶壁上白色物质主要是Na2CO3
请完成下列表格:
| 实验Ⅰ | 实验Ⅱ | |
| 实验操作 |  | 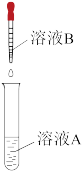 |
| 实验现象 | 现象1 | 现象2:有白色沉淀生成 |
②步骤b中观察到滤液为无色溶液,滤纸上留有黑色固体。乙同学从元素守恒的角度,可推测该黑色固体可能是
(3)金属钠在700℃时与CCl4生成纳米级金刚石粉末(用C表示)。写出反应的化学方程式并表示该反应电子转移的方向和数目:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】侯氏制碱法原理:将NH3和CO2气体通入饱和食盐水中即可获得NaHCO3和NH4Cl的混合物,然后分离出NaHCO3再加热制得纯碱。其流程如图:

参照表中数据:
回答下列问题:
(1)气体A、B依次是___________ 。
A.CO2、NH3 B. NH3、CO2 C.任何顺序都可以
(2)写出Ⅰ和Ⅱ步骤总反应的化学方程式:___________ 。由反应原理可知,a___________ 9.6(填“<”“>”或“=”)。
(3)操作Ⅲ的名称是___________ ,化学实验室进行该操作用到的主要玻璃仪器有___________ 、___________ 、玻璃棒。
(4)经步骤Ⅲ所得溶液中含有的盐为___________ 、___________ (写化学式)。经过___________ (填操作名称)后可以得到化肥。

参照表中数据:
| 物质 | CO2 | NH3 | NaHCO3 | NH4Cl | NaCl |
| 溶解度 (20 ℃) | V水∶V二氧化碳=1∶1 | V水∶V氨气=1∶700 | 9.6 g | 37.2 g | a g |
回答下列问题:
(1)气体A、B依次是
A.CO2、NH3 B. NH3、CO2 C.任何顺序都可以
(2)写出Ⅰ和Ⅱ步骤总反应的化学方程式:
(3)操作Ⅲ的名称是
(4)经步骤Ⅲ所得溶液中含有的盐为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某同学拟用50 mL NaOH溶液吸收CO2气体制备Na2CO3溶液。为了防止通入的CO2气体过量生成NaHCO3,他设计了如下实验步骤:
①用25 mL NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;
②小心煮沸溶液1~2 min;
③在得到的溶液中加入另一半(25 mL)NaOH溶液,使溶液充分混合。
(1)他能否制得较纯净的Na2CO3溶液?___________ 。理由是___________ 。
(2)按他的设计,第①步实验装置如下图。装置A中使用的试剂是石灰石和盐酸溶液。可否使用纯碱代替石灰石?___________ 。装置B使用的试剂是___________ ,作用是___________ 。

(3)有人认为实验步骤②③的顺序对调,即先混合再煮沸更合理,你认为对吗?______ 。为什么? ______ 。
①用25 mL NaOH溶液吸收过量的CO2气体,至CO2气体不再溶解;
②小心煮沸溶液1~2 min;
③在得到的溶液中加入另一半(25 mL)NaOH溶液,使溶液充分混合。
(1)他能否制得较纯净的Na2CO3溶液?
(2)按他的设计,第①步实验装置如下图。装置A中使用的试剂是石灰石和盐酸溶液。可否使用纯碱代替石灰石?

(3)有人认为实验步骤②③的顺序对调,即先混合再煮沸更合理,你认为对吗?
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】硫酸亚铁铵(NH4)2Fe(SO4)2•6H2O又称莫尔盐,是浅绿色晶体。用硫铁矿(主要含FeS2、SiO2等)制备莫尔盐的流程如下:(已知:FeS2与H2SO4不反应)
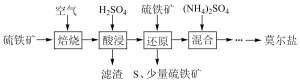
(1)莫尔盐属于____________ 。
A、酸式盐 B、碱式盐 C、复盐 D、硫酸盐
(2)硫铁矿焙烧的主反应是:4FeS2+11O2 2Fe2O3+8SO2,加快硫铁矿焙烧速率的措施有
2Fe2O3+8SO2,加快硫铁矿焙烧速率的措施有__________ ,若150kg硫铁矿(FeS2质量分数为80%)完全反应转移电子数为________________________
(3)加H2SO4酸浸,发生反应的离子方程式为________________________________ 。
(4)“还原”时,Fe3+可通过反应Ⅰ、Ⅱ被FeS2还原。
反应Ⅰ的离子方程式为:FeS2 +14Fe3+ +8H2O===15Fe2++ 2SO42—+16H+
反应Ⅱ的离子方程式为:_________________________________ 。
(5)为证明所得莫尔盐晶体中含有Fe2+和NH4+,实验方法是取其少量溶液于一支试管中, _______________ 证明含有Fe2+和NH4+。

(1)莫尔盐属于
A、酸式盐 B、碱式盐 C、复盐 D、硫酸盐
(2)硫铁矿焙烧的主反应是:4FeS2+11O2
 2Fe2O3+8SO2,加快硫铁矿焙烧速率的措施有
2Fe2O3+8SO2,加快硫铁矿焙烧速率的措施有(3)加H2SO4酸浸,发生反应的离子方程式为
(4)“还原”时,Fe3+可通过反应Ⅰ、Ⅱ被FeS2还原。
反应Ⅰ的离子方程式为:FeS2 +14Fe3+ +8H2O===15Fe2++ 2SO42—+16H+
反应Ⅱ的离子方程式为:
(5)为证明所得莫尔盐晶体中含有Fe2+和NH4+,实验方法是取其少量溶液于
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】某无色溶液X,由Na+、Ag+、Ba2+、Al3+、AlO 、MnO
、MnO 、CO
、CO 、SO
、SO 中的若干种离子组成,取溶液进行如下连续实验:
中的若干种离子组成,取溶液进行如下连续实验:

(1)白色沉淀甲是______ 。
(2)X溶液中一定存在的离子是______ 。
(3)白色沉淀乙中一定有:______ ,可能有______ 证明其是否存在的方法是______ 。
(4)若将过量的气体A与适量的气体B通入水中,写出反应的离子方程式______
 、MnO
、MnO 、CO
、CO 、SO
、SO 中的若干种离子组成,取溶液进行如下连续实验:
中的若干种离子组成,取溶液进行如下连续实验:
(1)白色沉淀甲是
(2)X溶液中一定存在的离子是
(3)白色沉淀乙中一定有:
(4)若将过量的气体A与适量的气体B通入水中,写出反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】四溴化碳是一种灰白色粉末,熔点为94~95℃,广泛用于有机化合物的溴代、农药的制备等。某合作学习小组的同学拟用丙酮和液溴制备四溴化碳,其原理为CH3COCH3+4Br2+5NaOH→CBr4+CH3COONa+4NaBr+4H2O。回答下列问题:
Ⅰ.制取Br2
(1)甲组同学拟用溴化钠、二氧化锰及浓硫酸制备液溴,其实验装置如图1所示:

①该装置不用橡皮塞及橡皮管,其原因是___________________ ;
②冰水的作用是__________________________ 。
Ⅱ.制取CBr4
(2)乙组同学拟利用甲组同学制得的液溴与CH3COCH3(沸点56.5℃)等试剂制取四溴化碳。实验步骤如下:
步骤1:向图2中三颈烧瓶中加入11.4 g NaOH和46 mL水,搅拌。
步骤2:冰水浴冷却至2℃时,开始不断滴加液溴20 g,滴加完毕后在5℃下保持20 min。
步骤3:加入少量相转移试剂,在不断搅拌下滴入1.6 g丙酮,维持温度在5~10℃,连续搅拌4 h。
步骤4:过滤、冷水洗涤、减压烘干,得产品8.3 g。
①步骤2滴入Br2之前,冷却至2℃的目的是__________________________
②步骤4洗涤时,如何证明已洗涤干净:___________________________ 。
③本次实验中产品的产率为______________ 。
Ⅰ.制取Br2
(1)甲组同学拟用溴化钠、二氧化锰及浓硫酸制备液溴,其实验装置如图1所示:

①该装置不用橡皮塞及橡皮管,其原因是
②冰水的作用是
Ⅱ.制取CBr4
(2)乙组同学拟利用甲组同学制得的液溴与CH3COCH3(沸点56.5℃)等试剂制取四溴化碳。实验步骤如下:
步骤1:向图2中三颈烧瓶中加入11.4 g NaOH和46 mL水,搅拌。
步骤2:冰水浴冷却至2℃时,开始不断滴加液溴20 g,滴加完毕后在5℃下保持20 min。
步骤3:加入少量相转移试剂,在不断搅拌下滴入1.6 g丙酮,维持温度在5~10℃,连续搅拌4 h。
步骤4:过滤、冷水洗涤、减压烘干,得产品8.3 g。
①步骤2滴入Br2之前,冷却至2℃的目的是
②步骤4洗涤时,如何证明已洗涤干净:
③本次实验中产品的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】亚硫酰氯(俗称氯化亚砜,SOCl2)是一种液态化合物,沸点77℃,在农药、制药行业、有机合成等领域用途广泛。实验室合成原理:SO2+Cl2+SCl2=2SOCl2,部分装置如图所示:

请回答下列问题:
(1)仪器c的名称是__________________ 。
(2)实验室用二氧化锰与浓盐酸共热反应的离子方程式为______________________ 。
(3)已知SOCl2遇水剧烈反应,液面上产生白雾,并常有刺激性气味的气体产生。蒸干AlCl3溶液不能得到无水AlCl3,使SOCl2与AlCl3·6H2O混合加热,可得到无水AlCl3,试解释原因:____________________________________________ 。
(4)装置e中产生的Cl2经过装置d(含两个洗气瓶)后进入三颈烧瓶,按Cl2的流向,第一个洗气瓶应放入的试剂是__________
(5)若反应中消耗Cl2的体积为896 mL(已转化为标准状况,SO2足量),最后得到纯净的SOCl2 4.76 g,则SOCl2的产率为__________ (保留三位有效数字)。
(6)分离产物后,向获得的SOCl2中加入足量NaOH溶液,振荡、静置得到无色溶液W,检验溶液W中存在Cl-的方法是______________________________ 。

请回答下列问题:
(1)仪器c的名称是
(2)实验室用二氧化锰与浓盐酸共热反应的离子方程式为
(3)已知SOCl2遇水剧烈反应,液面上产生白雾,并常有刺激性气味的气体产生。蒸干AlCl3溶液不能得到无水AlCl3,使SOCl2与AlCl3·6H2O混合加热,可得到无水AlCl3,试解释原因:
(4)装置e中产生的Cl2经过装置d(含两个洗气瓶)后进入三颈烧瓶,按Cl2的流向,第一个洗气瓶应放入的试剂是
(5)若反应中消耗Cl2的体积为896 mL(已转化为标准状况,SO2足量),最后得到纯净的SOCl2 4.76 g,则SOCl2的产率为
(6)分离产物后,向获得的SOCl2中加入足量NaOH溶液,振荡、静置得到无色溶液W,检验溶液W中存在Cl-的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某溶液可能含Cl-、SO42-、CO32-、Cu2+、Ba2+和Na+。探究小组为了确定该溶液中离子的组成,取该溶液 100mL 进行以下实验:(填写下表空格)
若 100mL 溶液中含有 0.3mol Na+,则向步骤三的滤液中加入足量 AgNO3 溶液, 过滤、洗涤、干燥,可得到______________ g 白色沉淀[保留小数点后一位]。
| 实验操作与现象 | 实验结论 | 判断理由 | |
| 步骤一 | 加入过量NaOH溶液,得到蓝色沉淀; | 肯定有 Cu2+、肯定无 | 肯定无该离子的理由 |
| 步骤二 | 将蓝色沉淀过滤、洗涤、灼烧得到24.0g 固体; | Cu2+物质的量浓度为 | Cu 元素守恒。过滤所用玻璃仪器有烧杯、 |
| 步骤三 | 向上述滤液中加足量Ba(NO3)2溶液,得到46.6g不溶于稀硝酸的沉淀。 | 肯定有Cl-、 | 相应的离子方程式: |
您最近一年使用:0次



