化学与科学、技术、社会密切相关。下列有关说法中错误的是
| A.已知中和热是57.3kJ·mol-1,则含1mol NaOH 和1mol CH3COOH 的两种稀溶液混合反应放热57.3kJ |
| B.常温下,反应C(s) +CO2(g) =2CO(g)不能自发进行,则该反应的△H>0 |
| C.氢氧燃料电池发电比氢气直接燃烧产生热量发电能量转换率高 |
| D.航海船只的船底四周嵌锌块,利用的是牺牲阳极保护法 |
更新时间:2019-02-20 12:57:30
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列有关热化学方程式的说法正确的是
A.甲烷的标准燃烧热为890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为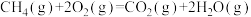  |
B.500℃、30MPa下,将0.5mol 和1.5mol 和1.5mol 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放热19.3kJ,其热化学反应方程式为: ,放热19.3kJ,其热化学反应方程式为:  |
C.已知稀溶液中 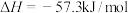 则稀醋酸与稀氢氧化钠溶液反应生成1mol水时放出57.3kJ的热量 则稀醋酸与稀氢氧化钠溶液反应生成1mol水时放出57.3kJ的热量 |
D.CO(g)的燃烧热是283.0kJ/mol,则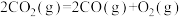 反应的 反应的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关热化学方程式书写及对应表述均正确的是
| A.已知2C(s)+O2(g)=2CO(g)△H=-221kJ/mol,则可知C的燃烧热△H=-110.5kJ/mol |
| B.稀醋酸与0.1mol/LNaOH溶液反应:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol |
| C.已知1mol氢气完全燃烧生成液态水所放出的热量为285.5kJ,则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g)△H=+285.5kJ/mol |
| D.密闭容器中,16g硫粉与足量铁粉混合加热生成硫化亚铁时,放出47.8kJ热量。则Fe(s)+S(s)=FeS(s)△H=-95.6kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】强酸和强碱的稀溶液的中和热可表示为:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol
已知:CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) ΔH=-Q1 kJ/mol
H2SO4(浓)+NaOH(aq)= Na2SO4(aq)+H2O(l) ΔH=-Q2 kJ/mol
Na2SO4(aq)+H2O(l) ΔH=-Q2 kJ/mol
HNO3(aq)+KOH(aq)=KNO3(aq)+H2O(l) ΔH=-Q3 kJ/mol
上述反应均为溶液中的反应,则Q1、Q2、Q3的绝对值大小的关系为
已知:CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) ΔH=-Q1 kJ/mol
H2SO4(浓)+NaOH(aq)=
 Na2SO4(aq)+H2O(l) ΔH=-Q2 kJ/mol
Na2SO4(aq)+H2O(l) ΔH=-Q2 kJ/molHNO3(aq)+KOH(aq)=KNO3(aq)+H2O(l) ΔH=-Q3 kJ/mol
上述反应均为溶液中的反应,则Q1、Q2、Q3的绝对值大小的关系为
| A.Q1=Q2=Q3 | B.Q2>Q1>Q3 | C.Q2>Q3>Q1 | D.Q2=Q3>Q1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】由铁及其化合物可制得FeSO4·7H2O、FeCl3、K2FeO4等化工产品,它们在生产、生活中具有 广泛应用。高炉炼铁的反应为 Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH=-23.5 kJ·mol-1。对于反应Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g),下列有关说法正确的是
| A.该反应一定能自发进行,则该反应的ΔS>0 |
| B.升高温度使反应物活化分子数增多,能提高反应速率和CO平衡转化率 |
| C.增加炼铁炉高度,延长CO和铁矿石接触时间,能降低平衡时尾气中CO的体积分数 |
| D.制备的生铁中含少量FexC,相同条件下与酸反应放出氢气的速率比纯铁慢 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述中不正确 的是
| A.可将钢铁设备与电源的负极相连以防止钢铁腐蚀 |
| B.常温下,NH3(g)+HCl(g) = NH4Cl(s)能够自发进行,则该反应的ΔH<0 |
| C.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
| D.反应H2(g)+I2(g)⇌2HI(g)到达平衡状态后,恒温恒容下充入氦气,则正反应速率增大,逆反应速率减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列叙述中不正确 的是
| A.常温下,NH3(g)+HCl(g)=NH4Cl(s) 能够自发进行,则该反应的△H<0 |
| B.需加热才能进行的反应是吸热反应,不需加热就能进行的反应是放热反应 |
| C.C(金刚石,s)=C(石墨,s) △H= -1.9kJ·mol-1,则石墨比金刚石稳定 |
D.常温下,0.1mol·L-1CH3COONa溶液加水稀释后,溶液中 的值增大 的值增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关电化学原理及应用的相关说法正确的是
| A.电池是能量高效转化装置,燃料电池放电时化学能全部转化为电能 |
| B.电热水器用牺牲阳极的阴极保护法阻止不锈钢内胆腐蚀,阳极选用铜棒 |
| C.工业上用电解法精炼铜过程中,阳极质量减少和阴极质量增加相同 |
| D.电解氧化法在铝制品表面形成氧化膜减缓腐蚀,铝件作为阳极 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示。下列说法正确的是


| A.该微生物燃料电池,负极为b |
| B.为保证该电池的供电速度,应在较高温度下工作 |
C.当电路中有0.5mol电子发生转移,则有1mol的 通过质子交换膜 通过质子交换膜 |
D.该电池正极电极反应式为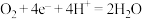 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】甲醇-空气燃料电池的反应为2CH3OH+3O2+4KOH=2K2CO3+6H2O,下列有关说法正确的是( )
| A.甲醇-空气燃料电池的负极反应为CH3OH-6e-+8OH-=CO32-+6H2O |
| B.一定温度下,反应2H2(g)+CO(g)=CH3OH(g)能自发进行,该反应的ΔH>0 |
| C.根据共价键的键能可以准确计算CO2(g)+3H2(g)=CH3OH(g)+H2O(l)的ΔH |
| D.标准状况下,甲醇-空气燃料电池放电时消耗5.6LO2,转移电子的数目约为3.01×1023 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于金属的腐蚀与防护说法正确的是
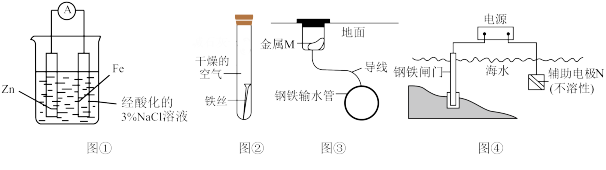

| A.图①中往Fe电极区滴入2滴K3[Fe(CN)6],产生蓝色沉淀 |
| B.图②中铁丝容易生成Fe2O3·xH2O |
| C.图③中M可用石墨代替 |
| D.图④中若电源断开,闸门易发生吸氧腐蚀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关生活生产中的叙述合理的是
| A.铜的精炼工业和电镀铜工业,均可采用CuS04溶液做电解质溶液 |
| B.铅蓄电池放电时,负极反应式为Pb02+4H++2e-=Pb2++2H20 |
| C.水库的钢闸门与电源负极相连以防止其生锈,该法即牺牲阳极的阴极保护法 |
| D.用惰性电极电解NaOH溶液,一段时间后,加入一定质量的NaOH固体,能将溶液恢复至与原来溶液完全一样 |
您最近一年使用:0次




