化学是一门非常重要的自然学科,在社会各领域中都发挥着重要的作用。
(1)黑火药是我国古代四大发明之一,其化学反应方程式为: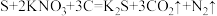
①上述反应所涉及到的物质中属于非电解质的是________ ;
②上述反应中被还原的元素是________ (填元素符号);
③收集上述反应生成的气体0.4mol,通入100mL 的氢氧化钠溶液中,最终所得溶液中的溶质是
的氢氧化钠溶液中,最终所得溶液中的溶质是________ (填化学式);
(2)我国古代常用绿矾 来制备硫酸,若将绿矾投入到稀硝酸中,发生反应的离子方程式为
来制备硫酸,若将绿矾投入到稀硝酸中,发生反应的离子方程式为________ ;
(3)在第一次世界大战期间,德军在比利时的伊普雷战役中使用了氯气制造的毒气弹。现代工业常用氯气制备漂白粉、消毒液等物质,写出制备84消毒液的离子反应方程式________ 。
(1)黑火药是我国古代四大发明之一,其化学反应方程式为:
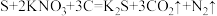
①上述反应所涉及到的物质中属于非电解质的是
②上述反应中被还原的元素是
③收集上述反应生成的气体0.4mol,通入100mL
 的氢氧化钠溶液中,最终所得溶液中的溶质是
的氢氧化钠溶液中,最终所得溶液中的溶质是(2)我国古代常用绿矾
 来制备硫酸,若将绿矾投入到稀硝酸中,发生反应的离子方程式为
来制备硫酸,若将绿矾投入到稀硝酸中,发生反应的离子方程式为(3)在第一次世界大战期间,德军在比利时的伊普雷战役中使用了氯气制造的毒气弹。现代工业常用氯气制备漂白粉、消毒液等物质,写出制备84消毒液的离子反应方程式
更新时间:2019-03-03 19:28:19
|
相似题推荐
【推荐1】短程硝化-厌氧氨氧化工艺的目的是将氨氮( )废水中的氮元素转变为
)废水中的氮元素转变为 脱除,其机理如下:
脱除,其机理如下:

资料:氧气浓度过高时, 会被氧化成
会被氧化成 。
。
(1)参与I中反应的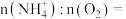
_____ 。
(2)Ⅱ中生成 的离子方程式为
的离子方程式为_____ 。
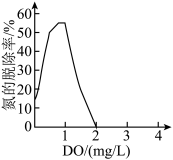
(3)废水溶解氧浓度(DO)对氮的脱除率的影响如图所示。当DO>2mg/L时,氮的脱除率为0,其原因可能是厌氧氨氧化菌被㧕制,Ⅱ中反应无法发生;还有可能是_____ 。
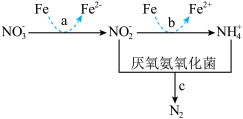
(4)经上述工艺处理后,排出的水中含有一定量的 ,加入铁粉能有效除去
,加入铁粉能有效除去 。该过程涉及的三个反应(a、b和c)如图:在整个反应过程中几乎监测不到
。该过程涉及的三个反应(a、b和c)如图:在整个反应过程中几乎监测不到 浓度的增加。请从化学反应速率的角度解释其原因:
浓度的增加。请从化学反应速率的角度解释其原因:_____ 。
 )废水中的氮元素转变为
)废水中的氮元素转变为 脱除,其机理如下:
脱除,其机理如下:
资料:氧气浓度过高时,
 会被氧化成
会被氧化成 。
。(1)参与I中反应的
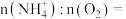
(2)Ⅱ中生成
 的离子方程式为
的离子方程式为(3)废水溶解氧浓度(DO)对氮的脱除率的影响如图所示。当DO>2mg/L时,氮的脱除率为0,其原因可能是厌氧氨氧化菌被㧕制,Ⅱ中反应无法发生;还有可能是

(4)经上述工艺处理后,排出的水中含有一定量的
 ,加入铁粉能有效除去
,加入铁粉能有效除去 。该过程涉及的三个反应(a、b和c)如图:在整个反应过程中几乎监测不到
。该过程涉及的三个反应(a、b和c)如图:在整个反应过程中几乎监测不到 浓度的增加。请从化学反应速率的角度解释其原因:
浓度的增加。请从化学反应速率的角度解释其原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)在反应式: aFeCl2+bKNO3+cHCl=dFeCl3+eKCl+fX+gH2O中,若b=1,d=3,则X 的分子式为____________ 。
(2)完成以下氧化还原反应的离子反应方程式,并标出电子转移的方向和数目:___________
___CrI3+____Cl2+______——____K2CrO4 + ____KIO4 +___KCl+______
(2)完成以下氧化还原反应的离子反应方程式,并标出电子转移的方向和数目:
___CrI3+____Cl2+______——____K2CrO4 + ____KIO4 +___KCl+______
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氧化还原反应是重要的化学反应类型,在生活、生产、科研领域都有广泛的应用,请回答以下问题。
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐会导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。以上过程中分别体现了亚硝酸盐、维生素C的什么性质:______ 、______ (填“氧化性”或“还原性”)。
(2)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体Cl2。
①将方程式补充完整:______ 。
______NaClO+______HCl(浓)=______NaCl+______Cl2↑+______H2O
②该反应中氧化剂是______ (填化学式),氧化产物与还原产物个数比为______ 。
③砒霜(As2O3)可与Zn反应:As2O3+6Zn+6H2SO4=2AsH3+6ZnSO4+3H2O。每生成1个AsH3分子转移______ 个电子。
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐会导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。以上过程中分别体现了亚硝酸盐、维生素C的什么性质:
(2)生活中若将“84”消毒液(有效成分是NaClO)和洁厕精(主要成分是HCl)混合,易产生黄绿色有毒气体Cl2。
①将方程式补充完整:
______NaClO+______HCl(浓)=______NaCl+______Cl2↑+______H2O
②该反应中氧化剂是
③砒霜(As2O3)可与Zn反应:As2O3+6Zn+6H2SO4=2AsH3+6ZnSO4+3H2O。每生成1个AsH3分子转移
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某同学对铜与硝酸的反应进行探究,请你参与并完成有关问题的解答。该同学采用如图所示装置验证铜与硝酸的反应。已知仪器A中盛有足量的一定浓度的硝酸溶液,试管B中盛有3.2g铜。
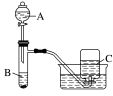
(1)请写出铜与稀硝酸反应的化学方程式:___ 。
(2)在铜与硝酸的反应中,硝酸所表现出的化学性质有___ 。
(3)仪器C中收集的气体主要是___ (填化学式)。
(4)待试管B中的铜反应完全后,如果向B中液体里加入足量氢氧化钠溶液,可生成沉淀的质量是__ g。

(1)请写出铜与稀硝酸反应的化学方程式:
(2)在铜与硝酸的反应中,硝酸所表现出的化学性质有
(3)仪器C中收集的气体主要是
(4)待试管B中的铜反应完全后,如果向B中液体里加入足量氢氧化钠溶液,可生成沉淀的质量是
您最近一年使用:0次
【推荐2】细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如图所示。
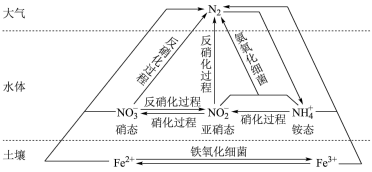
(1)图所示氮循环中,属于氮的固定的有______ (填字母序号)。
a.N2转化为氨态氮 b.硝化过程 c. 反硝化过程
(2)硝化过程中,含氮物质发生______ (填“氧化"或“还原")反应。
(3)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移的电子的物质的量为_________ mol。
(4)土壤中的铁循环可用于水体脱氨(脱氨是指将氨元素从水体中除去),结合图中的转化,土壤中的铁循环脱除水体中氨态氮和硝态氮的原理用离子方程式表示如下: 6Fe3++2NH =6Fe2+ +N2↑+8H+和
=6Fe2+ +N2↑+8H+和__________________

(1)图所示氮循环中,属于氮的固定的有
a.N2转化为氨态氮 b.硝化过程 c. 反硝化过程
(2)硝化过程中,含氮物质发生
(3)氨态氮与亚硝态氮可以在氨氧化细菌的作用下转化为氮气。该反应中,当产生0.02mol氮气时,转移的电子的物质的量为
(4)土壤中的铁循环可用于水体脱氨(脱氨是指将氨元素从水体中除去),结合图中的转化,土壤中的铁循环脱除水体中氨态氮和硝态氮的原理用离子方程式表示如下: 6Fe3++2NH
 =6Fe2+ +N2↑+8H+和
=6Fe2+ +N2↑+8H+和
您最近一年使用:0次

 )。为了防止亚硝酸钠污染环境,可以用氯化铵溶液处理废液。亚硝酸钠和氯化铵溶液在加热条件下发生反应,使亚硝酸钠转化为无毒物质。反应可看成两步,亚硝酸钠和氯化铵先反应生成氯化钠和亚硝酸铵,亚硝酸铵再受热分解生成氮气和水。
)。为了防止亚硝酸钠污染环境,可以用氯化铵溶液处理废液。亚硝酸钠和氯化铵溶液在加热条件下发生反应,使亚硝酸钠转化为无毒物质。反应可看成两步,亚硝酸钠和氯化铵先反应生成氯化钠和亚硝酸铵,亚硝酸铵再受热分解生成氮气和水。

