在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙。下图所示A--E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题。
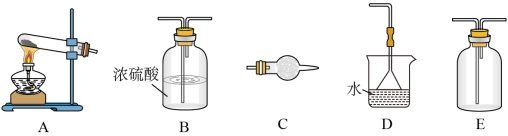
(1)实验室制取、收集干燥的NH3,需选用上述仪器装置中的______ 。
(2)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是_____ ,写出制纳米级碳酸钙的化学方程式:______ 。
(3)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级___________ 。

(1)实验室制取、收集干燥的NH3,需选用上述仪器装置中的
(2)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是
(3)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级
11-12高三上·江苏·阶段练习 查看更多[1]
(已下线)2012届江苏省淮州中学高三上学期10月份月考化学试卷
更新时间:2016-12-09 02:07:27
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】将少量FeCl3的饱和溶液分别滴加到下列物质中,得到三种分散系①、②、③
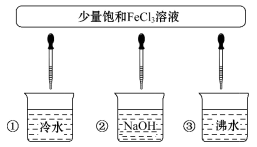
(1)将③继续加热煮沸至液体呈红褐色,反应的化学方程式为_______ 。
(2)如何用最简单的方法判断③中是否成功制备胶体?_______ 。

(1)将③继续加热煮沸至液体呈红褐色,反应的化学方程式为
(2)如何用最简单的方法判断③中是否成功制备胶体?
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】有下列词语:①渗析 ②盐析 ③聚沉 ④溶胶 ⑤凝胶 ⑥电泳 ⑦丁达尔效应 ⑧中和 ⑨水解,选出适当的词语将其序号填入下列空格中。
(1)往浓肥皂水中加入饱和食盐水(或固体食盐),肥皂凝聚,这种现象称为________ 。
(2)在肥皂水中透过强光,可看到光带,这种现象称为________ 。
(3)使热的浓肥皂水冷却并完全固化后的物质叫________ 。
(4)在肥皂水中加入酚酞变红色,说明高级脂肪酸根离子发生了________ 。
(5)在Fe(OH)3胶体中加入(NH4)2SO4产生红褐色沉淀,这种现象叫做________ 。
(6)用半透膜把制取Fe(OH)3胶体中生成的氯化钠分离出的方法叫做________ 。
(7)在水泥和冶金工厂常用高压电对气溶胶作用,除去大量烟尘,以减小对空气的污染。这种做法应用的主要原理是________ 。
(1)往浓肥皂水中加入饱和食盐水(或固体食盐),肥皂凝聚,这种现象称为
(2)在肥皂水中透过强光,可看到光带,这种现象称为
(3)使热的浓肥皂水冷却并完全固化后的物质叫
(4)在肥皂水中加入酚酞变红色,说明高级脂肪酸根离子发生了
(5)在Fe(OH)3胶体中加入(NH4)2SO4产生红褐色沉淀,这种现象叫做
(6)用半透膜把制取Fe(OH)3胶体中生成的氯化钠分离出的方法叫做
(7)在水泥和冶金工厂常用高压电对气溶胶作用,除去大量烟尘,以减小对空气的污染。这种做法应用的主要原理是
您最近一年使用:0次
【推荐3】湿法炼锌是在低温及水溶液中进行的一系列冶金作业过程。一种以锌焙砂矿(主要成分ZnO、Fe2O3,含有少量FeAs2O6、FeSb2O6等杂质)为原料冶炼锌的工艺流程如图:

回答下列问题:
(1)As和Sb是第VA族元素,As位于第四周期,则As的原子结构示意图为____ ,FeSb2O6中铁元素的化合价为____ 。
(2)酸浸时,Fe3+水解有助于ZnO溶解,该过程的离子反应方程式为____ 。
(3)pH大于5时,Fe3+全部水解生成Fe(OH)3胶体,Fe(OH)3胶体的胶粒带正电,在pH=5.2左右,小于5.2时胶粒带正电,此时As和Sb以AsO 和SbO
和SbO 存在,酸浸时控制pH=5~5.2的原因是
存在,酸浸时控制pH=5~5.2的原因是____ 。
(4)室温下,当c(Zn2+)=1 mol·L-1时,Zn2+开始沉淀的pH为____ 。{已知Ksp[Zn(OH)2]=1.2×10-17,lg2=0.3,lg3=0.5}
(5)酸浸后分离出滤渣的实验操作名称是____ ,实验室进行此操作时用到的玻璃仪器有烧杯、____ 。
(6)废电解液中的主要成分____ (填化学式)可以返回“酸浸”和“浸出”循环使用。

回答下列问题:
(1)As和Sb是第VA族元素,As位于第四周期,则As的原子结构示意图为
(2)酸浸时,Fe3+水解有助于ZnO溶解,该过程的离子反应方程式为
(3)pH大于5时,Fe3+全部水解生成Fe(OH)3胶体,Fe(OH)3胶体的胶粒带正电,在pH=5.2左右,小于5.2时胶粒带正电,此时As和Sb以AsO
 和SbO
和SbO 存在,酸浸时控制pH=5~5.2的原因是
存在,酸浸时控制pH=5~5.2的原因是(4)室温下,当c(Zn2+)=1 mol·L-1时,Zn2+开始沉淀的pH为
(5)酸浸后分离出滤渣的实验操作名称是
(6)废电解液中的主要成分
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】研究氮的循环和转化对生产、生活有重要的价值。
I.氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如下所示。

(1)设备1中发生反应的化学方程式是_______ ,实验室用消石灰和氯化铵固体制取NH3,该反应的化学方程式为_______ ;
(2)在工业上,可用浓氨水检验输送氯气的管道是否漏气,若漏气则有白烟生成,写出反应的化学方程式_______ 。设备2中通入的物质A是_______ 。
II.氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以NH 和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:
和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:

(3)过程①的目的是将NH 转化为NH3·H2O,并通过鼓入大量空气将氨气吹出,写出NH
转化为NH3·H2O,并通过鼓入大量空气将氨气吹出,写出NH 转化为NH3·H2O的离子方程式
转化为NH3·H2O的离子方程式_______ 。
(4)过程②加入NaClO溶液可将氨氮转化为无毒物质,反应后含氮元素的物质化学式为_______ 。
(5)含余氯废水的主要成分是NaClO以及HClO。X可选用以下哪种溶液以达到去除余氯的目的_______ (填序号)。
a.KOH b.Na2SO3 c.KMnO4 d.NaCl
I.氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如下所示。

(1)设备1中发生反应的化学方程式是
(2)在工业上,可用浓氨水检验输送氯气的管道是否漏气,若漏气则有白烟生成,写出反应的化学方程式
II.氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以NH
 和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:
和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:
(3)过程①的目的是将NH
 转化为NH3·H2O,并通过鼓入大量空气将氨气吹出,写出NH
转化为NH3·H2O,并通过鼓入大量空气将氨气吹出,写出NH 转化为NH3·H2O的离子方程式
转化为NH3·H2O的离子方程式(4)过程②加入NaClO溶液可将氨氮转化为无毒物质,反应后含氮元素的物质化学式为
(5)含余氯废水的主要成分是NaClO以及HClO。X可选用以下哪种溶液以达到去除余氯的目的
a.KOH b.Na2SO3 c.KMnO4 d.NaCl
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某实验小组的同学利用浓硫酸和浓硝酸进行如下实验。

请回答下列问题:
(1)现欲用15 mol/L HNO3溶液配制500 mL2 mol·L-1HNO3溶液,要用到的仪器除烧杯、胶头滴管、玻璃棒、量筒外,还必须使用的一种玻璃仪器是___________ 。
(2)甲同学用上图中所示的装置制取并收集NO2气体,选用仪器连接的顺序应是A接(填字母)___________ , A中发生反应的离子方程式为___________ 。
(3)乙同学用上图中的装置A进行铜与浓硫酸反应制取SO2气体,装置A中还缺少的仪器名称是___________ , 该反应的化学方程式为___________ ,该同学将一收集满SO2气体的小试管倒置于滴有紫色石蕊溶液的水中,可观察到的现象是___________ ,实验所产生的SO2尾气选用装置F来吸收。
(4)丙同学用上图中所示的装置制取并收集氨气,在装置B中加入的固体试剂是___________ (填化学式), 为了检验集气瓶中氨气是否集满,可将蘸有浓硝酸的玻璃棒移近集气瓶口,若___________ ,则证明已收集满。
(5)取6.4 g铜与500mL、x mol/L的硝酸恰好完全反应,生成的混合气体(假设其组成仅为NO和NO2)在标准状况的体积为2.24 L。则该硝酸中HNO3的物质的量为___________ 。

请回答下列问题:
(1)现欲用15 mol/L HNO3溶液配制500 mL2 mol·L-1HNO3溶液,要用到的仪器除烧杯、胶头滴管、玻璃棒、量筒外,还必须使用的一种玻璃仪器是
(2)甲同学用上图中所示的装置制取并收集NO2气体,选用仪器连接的顺序应是A接(填字母)
(3)乙同学用上图中的装置A进行铜与浓硫酸反应制取SO2气体,装置A中还缺少的仪器名称是
(4)丙同学用上图中所示的装置制取并收集氨气,在装置B中加入的固体试剂是
(5)取6.4 g铜与500mL、x mol/L的硝酸恰好完全反应,生成的混合气体(假设其组成仅为NO和NO2)在标准状况的体积为2.24 L。则该硝酸中HNO3的物质的量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某课外活动小组在实验室用下图所示的装置进行实验,验证氨的某些性质并收集少量纯净氮气。试回答:

(1)实验前先将仪器按图连接好,然后___________ ,再开始实验。
(2)实验进行一段时间后,可以观察到硬质试管内黑色的CuO粉末变成______ 色,盛无水CuSO4的干燥管内出现__________ 色,并在最后的出气导管处收集到纯净、干燥的N2。根据这些现象,硬质试管中的反应方程式为____________ ,这个反应说明氨气具有___________ 性。
(3)洗气瓶中浓硫酸的主要作用是_______________ 。
(4)在最后出气管口收集干燥、纯净的氮气,收集方法是__________ (填编号)
A.向上排空气法 B.向下排空气法
C.排水法 D.用塑料袋或球胆收集

(1)实验前先将仪器按图连接好,然后
(2)实验进行一段时间后,可以观察到硬质试管内黑色的CuO粉末变成
(3)洗气瓶中浓硫酸的主要作用是
(4)在最后出气管口收集干燥、纯净的氮气,收集方法是
A.向上排空气法 B.向下排空气法
C.排水法 D.用塑料袋或球胆收集
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某同学设计了如下装置用于制取SO2并验证SO2的部分性质。

请回答下列问题:
(1)写出氮气的电子式________ 。
(2)B中选用不同的试剂可验证SO2不同的性质。为验证SO2具有酸性氧化物性质,在B中可以放入的试剂是________ (填相应的编号)。
①新制氯水 ②品红溶液 ③含酚酞的NaOH试液 ④紫色石蕊试液
(3)装置C中可观察到白色沉淀现象,相关反应的离子方程式为__________________________ 。

请回答下列问题:
(1)写出氮气的电子式
(2)B中选用不同的试剂可验证SO2不同的性质。为验证SO2具有酸性氧化物性质,在B中可以放入的试剂是
①新制氯水 ②品红溶液 ③含酚酞的NaOH试液 ④紫色石蕊试液
(3)装置C中可观察到白色沉淀现象,相关反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】氧化铁可溶于稀盐酸.某同学想知道是稀盐酸中的哪种粒子(H2O、H+、Cl﹣)能使氧化铁溶解.设计如下实验:

【提出假设】
假设I:盐酸中的H2O使氧化铁溶解
假设Ⅱ:盐酸中的H+使氧化铁溶解
假设Ⅲ:盐酸中的_____________ 使氧化铁溶解
【实验探究】
(1)实验①氧化铁不溶解,可以验证假设___________ 不成立.
(2)实验②的目的是验证假设Ⅲ,则X溶液为_____________ ,滴加X溶液后氧化铁仍未溶解,欲得出结论可在加入X溶液后的试管中加入____________ ,发现氧化铁溶解.
(3)氧化铁溶于稀盐酸的离子方程式为:_________________ .
(4)将实验探究(2)得到的溶液经系列操作后可得到饱和氯化铁溶液,将其逐滴滴加到一定量的沸水中,继续加热到溶液呈红褐色可得到氢氧化铁胶体,可通过___________ 鉴别.取少量Fe(OH)3胶体置于试管中,向试管中滴加一定量稀盐酸,边滴边振荡,可以看到溶液先出现红褐色浑浊,接着红褐色浑浊逐渐变浅,最终又得到黄色的FeCl3溶液,先出现红褐色浑浊的原因:_________ ,又得到黄色的FeCl3溶液的化学方程式为:____________________ .

【提出假设】
假设I:盐酸中的H2O使氧化铁溶解
假设Ⅱ:盐酸中的H+使氧化铁溶解
假设Ⅲ:盐酸中的
【实验探究】
(1)实验①氧化铁不溶解,可以验证假设
(2)实验②的目的是验证假设Ⅲ,则X溶液为
(3)氧化铁溶于稀盐酸的离子方程式为:
(4)将实验探究(2)得到的溶液经系列操作后可得到饱和氯化铁溶液,将其逐滴滴加到一定量的沸水中,继续加热到溶液呈红褐色可得到氢氧化铁胶体,可通过
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某中学化学课外活动小组欲探究铁在氯气中燃烧产物的成分、性质和用途,设计了如下实验步骤:
Ⅰ、用下列实验装置制取纯净干燥的氯气

写出A、B中所盛放最佳化学试剂的名称_________ 、__________ ,画出虚线框内所需装置图并标明所需试剂的名称_________ 。
Ⅱ、某同学将一定量铁粉与Cl2恰好完全反应得到一固体物质a,然后通过实验确定其成分。探究过程如下:
(1)提出假设:(请把下列假设补充完整)
假设①:该固体物质是FeCl3;假设②:_________ ;假设③:_________ 。
(2)设计实验方案:
取少量固体物质a于烧杯中,加适量水溶解,然后取两份a溶液分别进行实验,实验现象与结论如下表,请在表格内的横线处填空。
由此得出结论:假设_______ 成立(填序号①②③)。
Ⅲ、为进一步探究物质a的性质,他们又利用a溶液做了如下一些实验,其中现象、结论均正确的是_________ (填写序号)
A.向氢氧化镁悬浊液中滴加a溶液出现红褐色沉淀,证明Ksp[Fe(OH)3]< Ksp[Mg(OH)2]
B.向a溶液中加入少量铁粉,铁粉溶解,溶液颜色由浅绿色变成黄色
C.向沸水中滴加a的饱和溶液,立即出现红褐色沉淀
D.将a溶液加热蒸干并灼烧,得到Fe2O3固体
IV、a溶液常作印刷电路铜板的腐蚀剂,写出发生反应的离子方程式___________ 。活动小组的同学们又设计了两种从上述废液中回收Cu的方案:
方案1:设计流程图如下:
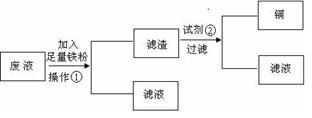
请分别写出操作①和试剂②的名称_________ ,_______ 。
方案2:在废液中加入适量的盐酸调节溶液的pH=1,用铜和石墨作电极进行电解,铜作________ 极。当观察到阴极有少量气泡产生时,停止电解,这时要回收的Cu已全部析出。
评价:方案2在电极上直接回收铜,操作上比方案1简便,但方案2也有不足之处,主要表现为:______________ 。
Ⅰ、用下列实验装置制取纯净干燥的氯气

写出A、B中所盛放最佳化学试剂的名称
Ⅱ、某同学将一定量铁粉与Cl2恰好完全反应得到一固体物质a,然后通过实验确定其成分。探究过程如下:
(1)提出假设:(请把下列假设补充完整)
假设①:该固体物质是FeCl3;假设②:
(2)设计实验方案:
取少量固体物质a于烧杯中,加适量水溶解,然后取两份a溶液分别进行实验,实验现象与结论如下表,请在表格内的横线处填空。
| 实验方法 | 实验现象 | 结论 |
| 在溶液中加KSCN溶液 | 固体物质中有FeCl3 | |
| 向a溶液中滴加酸性KMnO4溶液 | KMnO4溶液紫色不褪色 | 固体物质中不含 |
由此得出结论:假设
Ⅲ、为进一步探究物质a的性质,他们又利用a溶液做了如下一些实验,其中现象、结论均正确的是
A.向氢氧化镁悬浊液中滴加a溶液出现红褐色沉淀,证明Ksp[Fe(OH)3]< Ksp[Mg(OH)2]
B.向a溶液中加入少量铁粉,铁粉溶解,溶液颜色由浅绿色变成黄色
C.向沸水中滴加a的饱和溶液,立即出现红褐色沉淀
D.将a溶液加热蒸干并灼烧,得到Fe2O3固体
IV、a溶液常作印刷电路铜板的腐蚀剂,写出发生反应的离子方程式
方案1:设计流程图如下:

请分别写出操作①和试剂②的名称
方案2:在废液中加入适量的盐酸调节溶液的pH=1,用铜和石墨作电极进行电解,铜作
评价:方案2在电极上直接回收铜,操作上比方案1简便,但方案2也有不足之处,主要表现为:
您最近一年使用:0次



