研究物质的合成或制备是有机化学、无机化学的重要任务之一。
(1)某实验小组探究实验室制备无水氯化镁的方法,设计了如下图装置。
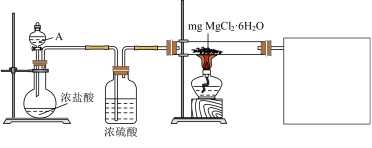
①分液漏斗中的A物质是___________ (填试剂名称)。
②利用中学常见的仪器,某同学在空白方框内补充完整实验装置,他选择的试剂有____ (填序号)
A.稀NaOH溶液 B.无水氯化钙 C.稀硫酸 D.浓硫酸
(2)实验室制备并收集纯净乙烯。
①有的同学通过乙醇制备乙烯,写出相关化学方程式:_______________ ;该实验除乙醇外,所需的试剂或用品(不包括仪器)有_______________________ 。
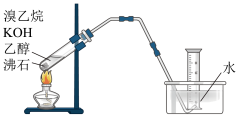
②有的同学探究其他制备乙烯的方法,他设计了下图装置制备乙烯。实验结果是量筒内壁附着较多无色油状液体,且得到很少量的气体。请分析气体产率很低的原因主要是_______ 。
(1)某实验小组探究实验室制备无水氯化镁的方法,设计了如下图装置。

①分液漏斗中的A物质是
②利用中学常见的仪器,某同学在空白方框内补充完整实验装置,他选择的试剂有
A.稀NaOH溶液 B.无水氯化钙 C.稀硫酸 D.浓硫酸
(2)实验室制备并收集纯净乙烯。
①有的同学通过乙醇制备乙烯,写出相关化学方程式:
②有的同学探究其他制备乙烯的方法,他设计了下图装置制备乙烯。实验结果是量筒内壁附着较多无色油状液体,且得到很少量的气体。请分析气体产率很低的原因主要是

更新时间:2019-03-09 12:28:19
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】水杨酸甲酯又叫冬青油,是一种重要的有机合成原料。某化学小组用水杨酸( )和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率。
)和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率。
实验步骤:
Ⅰ.如图,在三颈烧瓶中加入6.9 g (0.05 mol)水杨酸和24 g(30 mL,0.75 mol)甲醇,向混合物中加入约10 mL甲苯(甲苯与水形成的共沸物,沸点为85℃,该实验中加入甲苯,易将水蒸出),再小心地加入5 mL浓硫酸,摇动混匀,加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时;

Ⅱ.待装置冷却后,分离出甲醇,然后转移至分液漏斗,依次用少量水、5%NaHCO3 溶液和水洗涤;分出的产物加入少量无水MgSO4固体,过滤得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯4.5g。
常用物理常数:
请根据以上信息回答下列问题:
(1)仪器A的名称是___________ ,制备水杨酸甲酯时,最合适的加热方法是__________ 。
(2)实验中加入甲苯对合成水杨酸甲酯的作用是_____________________ 。
(3)反应结束后,分离甲醇的操作是_____________ 。
(4)洗涤操作中,第一次水洗的主要目的是__________ ,第二次水洗的主要目的是________ 。
(5)检验产品中是否含有水杨酸的化学方法是________________________ 。
(6)本实验的产率为___________ (保留两位有效数字)。
 )和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率。
)和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率。实验步骤:
Ⅰ.如图,在三颈烧瓶中加入6.9 g (0.05 mol)水杨酸和24 g(30 mL,0.75 mol)甲醇,向混合物中加入约10 mL甲苯(甲苯与水形成的共沸物,沸点为85℃,该实验中加入甲苯,易将水蒸出),再小心地加入5 mL浓硫酸,摇动混匀,加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时;

Ⅱ.待装置冷却后,分离出甲醇,然后转移至分液漏斗,依次用少量水、5%NaHCO3 溶液和水洗涤;分出的产物加入少量无水MgSO4固体,过滤得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯4.5g。
常用物理常数:
名称 | 分子量 | 颜色状态 | 相对密度 | 熔点(℃) | 沸点(℃) |
水杨酸甲酯 | 152 | 无色液体 | 1.18 | -8.6 | 224 |
水杨酸 | 138 | 白色晶体 | 1.44 | 158 | 210 |
甲醇 | 32 | 无色液体 | 0.792 | -97 | 64.7 |
(1)仪器A的名称是
(2)实验中加入甲苯对合成水杨酸甲酯的作用是
(3)反应结束后,分离甲醇的操作是
(4)洗涤操作中,第一次水洗的主要目的是
(5)检验产品中是否含有水杨酸的化学方法是
(6)本实验的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】学习小组进行实验研究乙醇的化学性质。
(1)将金属钠分别投入蒸馏水、无水乙醇和煤油(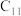 ~
~ 的烷烃)中,现象如下。
的烷烃)中,现象如下。 与
与 反应时断裂
反应时断裂_______ (填序号)。
a. 键 b.
键 b. 键 c.
键 c. 键
键
②乙中反应的化学方程式是_______ 。
③与甲相比,乙中反应较为缓慢,从结构角度解释原因:_______ 。
(2)实验室用乙醇、乙酸和浓硫酸制取乙酸乙酯,装置如图。 溶液的作用是
溶液的作用是_______ 。
②关于该实验的说法正确的是_______ (填序号)。
a.浓硫酸是该反应的催化剂
b.在试管中加入几片碎瓷片以防止暴沸
c.实验中加入过量乙醇,可使乙酸的转化率达到100%
(1)将金属钠分别投入蒸馏水、无水乙醇和煤油(
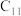 ~
~ 的烷烃)中,现象如下。
的烷烃)中,现象如下。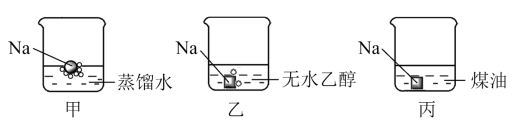
 与
与 反应时断裂
反应时断裂a.
 键 b.
键 b. 键 c.
键 c. 键
键②乙中反应的化学方程式是
③与甲相比,乙中反应较为缓慢,从结构角度解释原因:
(2)实验室用乙醇、乙酸和浓硫酸制取乙酸乙酯,装置如图。

 溶液的作用是
溶液的作用是②关于该实验的说法正确的是
a.浓硫酸是该反应的催化剂
b.在试管中加入几片碎瓷片以防止暴沸
c.实验中加入过量乙醇,可使乙酸的转化率达到100%
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯。

已知:
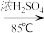
 +H2O
+H2O
(1)制备粗品
将12.5 mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是_____________ ,导管B除了导气外还具有的作用是冷凝。
②试管C置于冰水浴中的目的是_________________________ 。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_________ 层(填“上”或“下”),分液后用_______________ (填编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按下图装置蒸馏,冷却水从________ (填“f”或“g”) 口进入。蒸馏时要加入生石灰,目的是吸收水分,便于蒸馏出更纯净的产品。
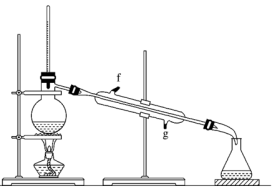
③收集产品时,控制的温度应在________ ℃左右,实验制得的环己烯精品质量低于理论产量,可能的原因是__________________ (填字母序号,下同)。
a.蒸馏时从70 ℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是______________ 。
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点

已知:

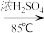
 +H2O
+H2O| 密度(g·cm-3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
将12.5 mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是
②试管C置于冰水浴中的目的是
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按下图装置蒸馏,冷却水从

③收集产品时,控制的温度应在
a.蒸馏时从70 ℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】工业上常利用含硫废水生产 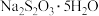 ,实验室可用如下装置(略去部分夹持仪器)模拟生产过程。
,实验室可用如下装置(略去部分夹持仪器)模拟生产过程。
烧瓶 中发生反应如下:
中发生反应如下:
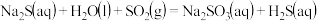

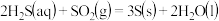

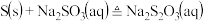

 中的长颈漏斗内注入液体至形成一段液柱,若
中的长颈漏斗内注入液体至形成一段液柱,若____ ,则整个装置气密性良好。装置  的作用是
的作用是____ 。装置  中为
中为____ 溶液。仪器  的名称是
的名称是____ 。
(2)为提高产品纯度,应使烧瓶 中
中  和
和  恰好完全反应,则烧瓶
恰好完全反应,则烧瓶  中
中  和
和  物质的量之比为
物质的量之比为____ 。
(3)装置 的作用之一是观察
的作用之一是观察  的生成速率,其中的液体最好选择
的生成速率,其中的液体最好选择____ (填字母序号)。
a.蒸馏水 b.饱和 溶液
溶液
c.饱和 溶液 d.饱和
溶液 d.饱和  溶液
溶液
实验中,为使 缓慢进入烧瓶
缓慢进入烧瓶  ,采用的操作是
,采用的操作是____ 。
已知反应 相对较慢,则烧瓶
相对较慢,则烧瓶  中反应达到终点的现象是
中反应达到终点的现象是____ 。
反应后期可用酒精灯适当加热烧瓶 ,实验室用酒精灯加热时必须使用石棉网的仪器有
,实验室用酒精灯加热时必须使用石棉网的仪器有____ (填字母序号)。
a.烧杯 b.蒸发皿 c.试管 d.锥形瓶
(4)已知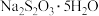 遇酸易分解,写出其与稀硫酸反应的离子方程式:
遇酸易分解,写出其与稀硫酸反应的离子方程式:____ 。
(5)反应终止后,烧瓶 中的溶液经蒸发浓缩、冷却结晶即可析出
中的溶液经蒸发浓缩、冷却结晶即可析出 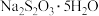 ,其中可能含有
,其中可能含有  、
、  等杂质。利用所给试剂设计实验,检测产品中是否存在
等杂质。利用所给试剂设计实验,检测产品中是否存在  ,简要说明实验操作、现象和结论:
,简要说明实验操作、现象和结论:____ 。(供选择的试剂:稀盐酸、稀硫酸、稀硝酸、  溶液、
溶液、  溶液)
溶液)
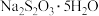 ,实验室可用如下装置(略去部分夹持仪器)模拟生产过程。
,实验室可用如下装置(略去部分夹持仪器)模拟生产过程。烧瓶
 中发生反应如下:
中发生反应如下: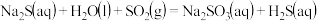

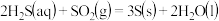

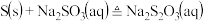

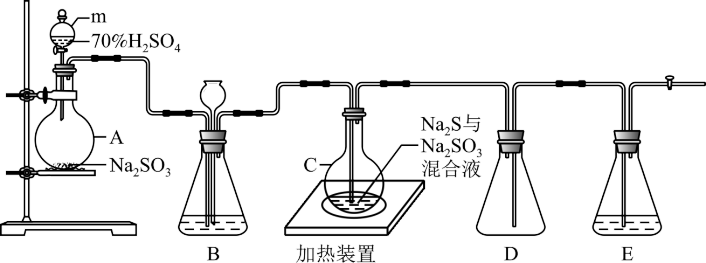
 中的长颈漏斗内注入液体至形成一段液柱,若
中的长颈漏斗内注入液体至形成一段液柱,若 的作用是
的作用是 中为
中为 的名称是
的名称是(2)为提高产品纯度,应使烧瓶
 中
中  和
和  恰好完全反应,则烧瓶
恰好完全反应,则烧瓶  中
中  和
和  物质的量之比为
物质的量之比为(3)装置
 的作用之一是观察
的作用之一是观察  的生成速率,其中的液体最好选择
的生成速率,其中的液体最好选择a.蒸馏水 b.饱和
 溶液
溶液c.饱和
 溶液 d.饱和
溶液 d.饱和  溶液
溶液实验中,为使
 缓慢进入烧瓶
缓慢进入烧瓶  ,采用的操作是
,采用的操作是已知反应
 相对较慢,则烧瓶
相对较慢,则烧瓶  中反应达到终点的现象是
中反应达到终点的现象是反应后期可用酒精灯适当加热烧瓶
 ,实验室用酒精灯加热时必须使用石棉网的仪器有
,实验室用酒精灯加热时必须使用石棉网的仪器有a.烧杯 b.蒸发皿 c.试管 d.锥形瓶
(4)已知
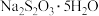 遇酸易分解,写出其与稀硫酸反应的离子方程式:
遇酸易分解,写出其与稀硫酸反应的离子方程式:(5)反应终止后,烧瓶
 中的溶液经蒸发浓缩、冷却结晶即可析出
中的溶液经蒸发浓缩、冷却结晶即可析出 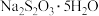 ,其中可能含有
,其中可能含有  、
、  等杂质。利用所给试剂设计实验,检测产品中是否存在
等杂质。利用所给试剂设计实验,检测产品中是否存在  ,简要说明实验操作、现象和结论:
,简要说明实验操作、现象和结论: 溶液、
溶液、  溶液)
溶液)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】实验室用镁和硝基苯制取反式偶氮苯(溶解性:不溶于水,溶于醇、醚)。实验原理如下:
2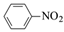 +4Mg+8CH3OH→
+4Mg+8CH3OH→ +4Mg(OCH3)2+4H2O
+4Mg(OCH3)2+4H2O
已知:①Mg(OCH3)2在水中极易水解。
②反式偶氮苯产品在紫外线照射后部分转化为顺式偶氮苯。
实验流程如下:

(1)反应中,硝基苯变为反式偶氮苯的反应属于_______________
A、取代反应 B、消去反应 C、还原反应 D、氧化反应
(2)在反应装置中,加入原料及溶剂,搅拌下加热回流。反应加入的镁屑应该_______________________________________ 。
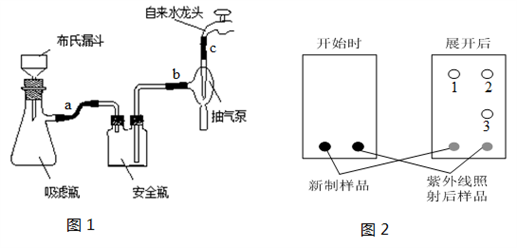
(3)反应结束后将反应液倒入冰水中,用乙酸中和至中性,即有反式偶氮苯粗产品析出,抽滤(抽滤装置如图1),滤渣用95%乙醇水溶液重结晶提纯。
①为了得到较大颗粒的晶体,加入乙酸时需要____________ (填“缓慢加入”、“快速加入”)。
②抽滤过程中要洗涤粗产品,下列液体最合适的是___________ 。
A.乙醚 B.蒸馏水 C.95%乙醇水溶液 D.饱和NaCl溶液
③抽滤完毕,应先断开橡皮管______________ (填序号),以防倒吸。
④重结晶操作包括“加热溶解、趁热过滤、冷却结晶、抽滤、洗涤、干燥”。上述重结晶过程中的________________________ 操作除去了可溶性杂质。
(4)已知薄层色谱分析中,分子极性弱的物质,在溶剂中扩散更快。某同学采用薄层色谱分析所得偶氮苯,实验开始时和展开后的斑点如图2所示。展开后的斑点中,顺式偶氮苯为______ (填斑点序号),说明顺式偶氮苯的分子极性比反式偶氮苯的分子极性__________ (填“强”或“弱”)。
2
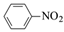 +4Mg+8CH3OH→
+4Mg+8CH3OH→ +4Mg(OCH3)2+4H2O
+4Mg(OCH3)2+4H2O已知:①Mg(OCH3)2在水中极易水解。
②反式偶氮苯产品在紫外线照射后部分转化为顺式偶氮苯。
实验流程如下:

(1)反应中,硝基苯变为反式偶氮苯的反应属于
A、取代反应 B、消去反应 C、还原反应 D、氧化反应
(2)在反应装置中,加入原料及溶剂,搅拌下加热回流。反应加入的镁屑应该

(3)反应结束后将反应液倒入冰水中,用乙酸中和至中性,即有反式偶氮苯粗产品析出,抽滤(抽滤装置如图1),滤渣用95%乙醇水溶液重结晶提纯。
①为了得到较大颗粒的晶体,加入乙酸时需要
②抽滤过程中要洗涤粗产品,下列液体最合适的是
A.乙醚 B.蒸馏水 C.95%乙醇水溶液 D.饱和NaCl溶液
③抽滤完毕,应先断开橡皮管
④重结晶操作包括“加热溶解、趁热过滤、冷却结晶、抽滤、洗涤、干燥”。上述重结晶过程中的
(4)已知薄层色谱分析中,分子极性弱的物质,在溶剂中扩散更快。某同学采用薄层色谱分析所得偶氮苯,实验开始时和展开后的斑点如图2所示。展开后的斑点中,顺式偶氮苯为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某同学设计实验探究浓硫酸与蔗糖反应所生成的产物,装置如图所示:
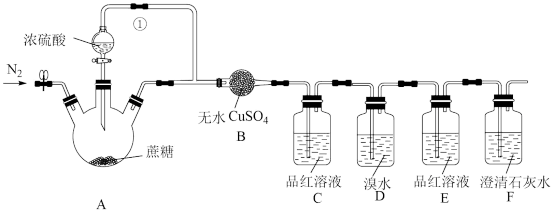
已知:实验前向蔗糖中加入几滴水,装置D、F中盛装的试剂均是足量的。
请回答下列问题:
(1)按图示连接好装置后,需检查_______ ;盛装浓硫酸的仪器的名称为_______ 。
(2)反应开始时,需要先向装置中通入N2,通入N2的作用为_______ 。;装置A中的导气管①的作用为_______ 。
(3)反应过程中,发现装置B处的无水CuSO4的颜色由白色变为_______ 。
(4)反应开始后,装置C中品红溶液褪色,这说明浓H2SO4与蔗糖反应生成了SO2气体,则装置D中应出现的现象为_______ ,该现象对应的离子方程式为_______ 。
(5)在实验过程中,装置F中出现白色浑浊现象,_______ (填“能”或“不能”)说明浓H2SO4与蔗糖反应所生成的产物中含有CO2气体;若将装置F放在装置B和C之间,澄清石灰水中出现白色浑浊现象,_______ (填“能”或“不能”)说明浓H2SO4与蔗糖反应所生成的产物中含有CO2气体,分析原因:_______ (用文字说明)。

已知:实验前向蔗糖中加入几滴水,装置D、F中盛装的试剂均是足量的。
请回答下列问题:
(1)按图示连接好装置后,需检查
(2)反应开始时,需要先向装置中通入N2,通入N2的作用为
(3)反应过程中,发现装置B处的无水CuSO4的颜色由白色变为
(4)反应开始后,装置C中品红溶液褪色,这说明浓H2SO4与蔗糖反应生成了SO2气体,则装置D中应出现的现象为
(5)在实验过程中,装置F中出现白色浑浊现象,
您最近一年使用:0次



