现有200 mL MgCl2和AlCl3混合溶液,其中Mg2+浓度0.2mol/L、Cl-浓度为1.3 mol/L。要使Mg2+转化成Mg(OH)2并使Mg2+、Al3+分离开来,至少需要4 mol/L NaOH溶液( )
| A.80mL | B.100mL | C.120mL | D.140mL |
12-13高一·全国·课时练习 查看更多[8]
更新时间:2019-03-17 20:57:25
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】右图表示在某溶液中滴加Ba(OH)2 溶液时,沉淀的物质的量随Ba(OH)2 的物质的量的变化关系。该溶液的成分可能是
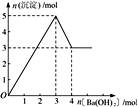

| A.MgSO4 | B.Al2 (SO4 )3 | C.Fe2 (SO4 )3 | D.NaAlO2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】加热蒸干氯化镁溶液因水解不完全会得到一种灰白色沉淀-碱式氯化镁,化学式可表示为Mgx(OH)yClz•nH2O。设计如图装置验证其化学式。下列有关实验说法不正确的是


| A.碱式氯化镁受热分解产生氧化镁、氯化氢和水 |
| B.①②中依次盛装浓硫酸、氢氧化钠溶液 |
| C.称取样品质量、反应后硬质玻璃管中剩余固体质量以及装置①的增重即可推出化学式 |
| D.碱石灰的作用是尾气处理,防止空气污染 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列反应的离子方程式正确的是
| A.少量CO2通入CaCl2溶液中:CO2+Ca2++H2O=CaCO3↓+2H+ |
| B.向含FeBr2和FeI2且物质的量各为0.5mol的溶液中通入1molCl2:4I−+2Fe2++3Cl2=2Fe3++2I2+6Cl− |
C.向明矾溶液中滴加Ba(OH)2溶液至沉淀的质量最大:2Al3++3 +6OH−+3Ba2+=3BaSO4↓+2Al(OH)3↓ +6OH−+3Ba2+=3BaSO4↓+2Al(OH)3↓ |
| D.向漂白粉溶液中通入少量二氧化硫:Ca2++3ClO−+SO2+H2O=CaSO4↓+Cl−+2HClO |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】铝土矿的主要成分是Al2O3,还有部分SiO2、Fe2O3以及少量不溶于酸碱溶液的其他杂质。工业上从铝土矿中提取铝可采取如下工艺:
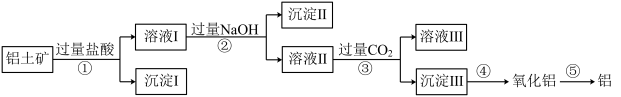
下列说法正确的是

下列说法正确的是
| A.步骤②过量氢氧化钠可用过量氨水代替 |
B.步骤③发生的反应为[Al(OH)4]-+CO2=Al(OH)3↓+ |
| C.溶液Ⅲ中溶质主要为Na2CO3 |
| D.步骤④需用蒸发皿和酒精灯 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】溶液中可能含有H+、 、Mg2+、Al3+、Fe3+、
、Mg2+、Al3+、Fe3+、 、
、 、
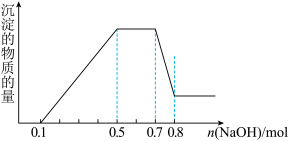
、 中的几种。①加入铝片,产生无色无味的气体;②加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是( )
中的几种。①加入铝片,产生无色无味的气体;②加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是( )
 、Mg2+、Al3+、Fe3+、
、Mg2+、Al3+、Fe3+、 、
、 、
、 中的几种。①加入铝片,产生无色无味的气体;②加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是( )
中的几种。①加入铝片,产生无色无味的气体;②加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法正确的是( )
A.溶液中一定不含 ,可能含有 ,可能含有 和 和 |
B.在滴加NaOH溶液物质的量为0.5~0.7mol时,发生离子反应为Al3++4OH-=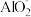 +2H2O +2H2O |
| C.溶液中的阳离子只有H+、Mg2+、Al3+ |
D.n(H+)∶n( )∶n(Mg2+)=2∶4∶1 )∶n(Mg2+)=2∶4∶1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列各组物质的稀溶液相互反应,无论是前者滴入后者,还是后者滴入前者,反应现象相同的是
| A.Na2CO3和HCl | B.AlCl3和NaOH |
| C.NaAlO2和H2SO4 | D.Ba(OH)2和Ba(HCO3)2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】将一定质量的镁和铝混合物投入200 mL稀硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入的NaOH溶液体积的变化关系如图所示。则下列说法不正确的是
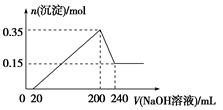

| A.镁和铝的总质量为9 g |
| B.合金与稀硫酸反应生成的氢气体积为10.08 L |
| C.稀硫酸的物质的量浓度为2.5 mol/L |
| D.氢氧化钠溶液的物质的量浓度为5 mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】研究发现,硝酸越稀,还原产物中氮元素的化合价越低。某同学取适量的铁粉和铝粉的混合物与足量很稀的硝酸充分反应,无气体放出。在反应结束后的溶液中,逐滴加入4mol/LNaOH溶液,所加NaOH溶液的体积(ml)与产生的沉淀的物质的量(mol)的关系如图所示。下列说法不正确的是( )


| A.溶液中n(NH4+)=0.012mol |
| B.混合物中铝粉与铁粉物质的量的比为1:2 |
| C.测定F点沉淀的质量,步骤是:过滤、洗涤、低温烘干、称量 |
| D.铝与该浓度硝酸反应的离子方程式为:8Al+30H++3NO3-=8Al3++3NH4++9H2O |
您最近一年使用:0次



