在研究化学反应中的能量变化时,我们通常做下面的实验:在一个小烧杯里,加入20克已研磨成粉末的八水合氢氧化钡,将小烧杯放在事先已滴有3-4滴水的玻璃片(或三合板)上,然后向烧杯内加入约10克氯化铵晶体,根据实验步骤,填写下表,并回答问题
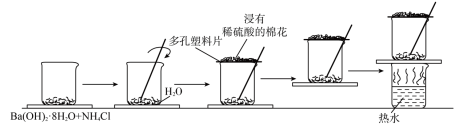
(4)写出实验过程中发生反应的化学方程式__________ 。
(5)实验中要立即用玻璃棒迅速搅拌的原因是:_________________ 。
(6)该反应在常温下就可进行,说明_________ 。

实验步骤 | 实验现象及结论 |
| 将晶体混合,立即快速搅拌 | 有刺激性气味能使湿润的紫色石蕊试纸变蓝的 |
| 用手摸烧杯下部 | 感觉烧杯变凉说明此反应是 |
| 用手拿起烧杯 | 烧杯下面的带有几滴水的玻璃片粘到了烧杯底部 |
| 将粘有玻璃片的烧杯放在盛有热水的烧杯上 | 玻璃片脱离上面烧杯底部 |
| 反应后移走多孔塑料片观察反应物 | 混合物成糊状,证明有 |
(5)实验中要立即用玻璃棒迅速搅拌的原因是:
(6)该反应在常温下就可进行,说明
更新时间:2019-04-19 11:04:45
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)根据图示能量关系
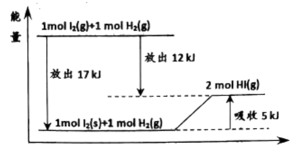
①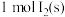 变为
变为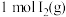 时需要
时需要___________ (填“放出”或“吸收”)___________  的能量。
的能量。
②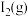 与
与 生成
生成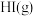 的反应是
的反应是___________ (填“放热”或“吸热”)反应。
(2)一定温度下,在容积为2L的密闭容器中进行反应: ,M、N、P的物质的量随时间变化的曲线如图所示:
,M、N、P的物质的量随时间变化的曲线如图所示:
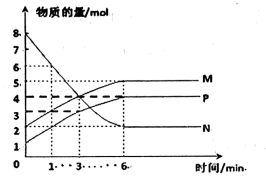
①下列措施不能提高反应速率的是___________ 。
A.升高温度 B.加入适量N C.加压压缩 D.及时分离出P
②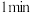 到
到 这段时刻,以M的浓度变化表示的平均反应速率为:
这段时刻,以M的浓度变化表示的平均反应速率为:___________ ,反应达平衡状态时,N的转化率为:___________ 。
(1)根据图示能量关系

①
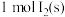 变为
变为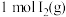 时需要
时需要 的能量。
的能量。②
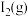 与
与 生成
生成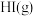 的反应是
的反应是(2)一定温度下,在容积为2L的密闭容器中进行反应:
 ,M、N、P的物质的量随时间变化的曲线如图所示:
,M、N、P的物质的量随时间变化的曲线如图所示:
①下列措施不能提高反应速率的是
A.升高温度 B.加入适量N C.加压压缩 D.及时分离出P
②
 到
到 这段时刻,以M的浓度变化表示的平均反应速率为:
这段时刻,以M的浓度变化表示的平均反应速率为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A为醇,A、C互为同系物,反应②的原子利用率为100%,F的化学式为C3H6O2。有关物质的转化关系如图所示:
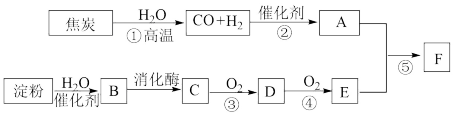
(1)A的结构简式为_______ ,E中官能团的名称是_______ 。
(2)反应①是_______ (填“放热反应”或“吸热反应”),反应③的反应类型为_______ 。
(3)淀粉的化学式为_______ ,向新制Cu(OH)2中加入适量B溶液,加热,可观察到的实验现象为_______ 。
(4)写出反应⑤的化学方程式:_______ 。

(1)A的结构简式为
(2)反应①是
(3)淀粉的化学式为
(4)写出反应⑤的化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ下图为H2和Cl2生成HCl过程中的能量变化:
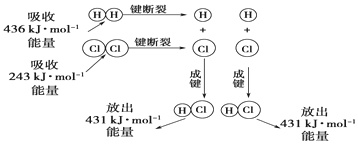
请回答下列有关问题:
(1)H2+Cl2═2HCl是_______ (填“吸热”或“放热”)反应,反应物的总能量_______ (填“>”,“=”或“<”)生成物的总能量;
(2)当有1molHCl生成时,反应_________ (填“吸收”或“放出”)的能量为________ KJ。
Ⅱ 一个完整的氧化还原反应方程式可拆写成两个半反应式,一个为氧化反应式,一个为还原反应式。
(1)已知某一反应的半反应式分别为CH4+10OH-—8e-=CO32-+7H2O和O2+2H2O+4e-=4OH-请写出该反应的总反应式:________________________ 。
(2)下图为氢氧燃料电池的构造示意图:
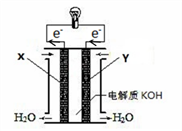
X极为电池的______________ (填“正”或“负”)极,X极的电极反应式为_____________________ ;若电池工作过程中有5.6LO2(标准状况下)参与反应,则转移电子的物质的量为_______________ 。

请回答下列有关问题:
(1)H2+Cl2═2HCl是
(2)当有1molHCl生成时,反应
Ⅱ 一个完整的氧化还原反应方程式可拆写成两个半反应式,一个为氧化反应式,一个为还原反应式。
(1)已知某一反应的半反应式分别为CH4+10OH-—8e-=CO32-+7H2O和O2+2H2O+4e-=4OH-请写出该反应的总反应式:
(2)下图为氢氧燃料电池的构造示意图:

X极为电池的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】氯乙烯(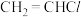 )是一种应用于高分子化工的重要单体,为无色、易液化气体,沸点为
)是一种应用于高分子化工的重要单体,为无色、易液化气体,沸点为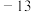 ℃。实验室可利用
℃。实验室可利用 、HCl、
、HCl、 的混合气体在催化剂作用下加热制备氯乙烯。回答下列问题:
的混合气体在催化剂作用下加热制备氯乙烯。回答下列问题:
Ⅰ.HCl的制备
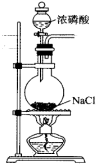
(1)盛装浓磷酸的仪器名称为______ ,已知该反应中参与反应的NaCl与 的物质的量之比为2∶1,写出该反应的化学方程式:
的物质的量之比为2∶1,写出该反应的化学方程式:______ 。
(2)磷酸浓度过低或过高均不利于HCl的逸出,写出磷酸浓度过低不利于HCl逸出的原因:______ 。
Ⅱ.氯乙烯的制备
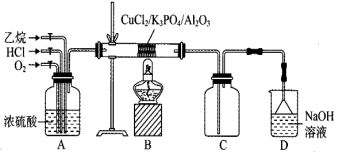
(3)①氯乙烯的电子式为______ 。
②A装置的作用为______ 。
③B中反应的化学方程式为______ 。
(4)该制备过程中会有副反应发生,生成副产物乙烯。 为该反应的催化剂,其中
为该反应的催化剂,其中 为主催化剂,为了提高反应物的转化率和产物氯乙烯的选择性,常需加入助催化剂如KCl、
为主催化剂,为了提高反应物的转化率和产物氯乙烯的选择性,常需加入助催化剂如KCl、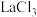 等,图1为K、Cu物质的量之比对催化剂活性的影响,图2为La的百分含量对催化剂活性的影响:
等,图1为K、Cu物质的量之比对催化剂活性的影响,图2为La的百分含量对催化剂活性的影响:

则实际生产过程中应选择的K、Cu的物质的量之比为______ ,La的百分含量为______ 。
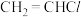 )是一种应用于高分子化工的重要单体,为无色、易液化气体,沸点为
)是一种应用于高分子化工的重要单体,为无色、易液化气体,沸点为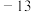 ℃。实验室可利用
℃。实验室可利用 、HCl、
、HCl、 的混合气体在催化剂作用下加热制备氯乙烯。回答下列问题:
的混合气体在催化剂作用下加热制备氯乙烯。回答下列问题:Ⅰ.HCl的制备

(1)盛装浓磷酸的仪器名称为
 的物质的量之比为2∶1,写出该反应的化学方程式:
的物质的量之比为2∶1,写出该反应的化学方程式:(2)磷酸浓度过低或过高均不利于HCl的逸出,写出磷酸浓度过低不利于HCl逸出的原因:
Ⅱ.氯乙烯的制备

(3)①氯乙烯的电子式为
②A装置的作用为
③B中反应的化学方程式为
(4)该制备过程中会有副反应发生,生成副产物乙烯。
 为该反应的催化剂,其中
为该反应的催化剂,其中 为主催化剂,为了提高反应物的转化率和产物氯乙烯的选择性,常需加入助催化剂如KCl、
为主催化剂,为了提高反应物的转化率和产物氯乙烯的选择性,常需加入助催化剂如KCl、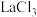 等,图1为K、Cu物质的量之比对催化剂活性的影响,图2为La的百分含量对催化剂活性的影响:
等,图1为K、Cu物质的量之比对催化剂活性的影响,图2为La的百分含量对催化剂活性的影响:
则实际生产过程中应选择的K、Cu的物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
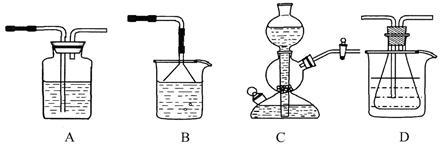
【推荐2】我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他利用NaHCO3、NaCl、NH4C1等物质溶解度的差异,以食盐、氨气、二氧化碳等为原料制得NaHCO3,进而生产出纯碱。以下A、B、C、D四个装置可组装成实验室模拟 “侯氏制碱法”制取NaHCO3的实验装置。装置中分别盛有以下试剂:B:稀硫酸;C:盐酸、碳酸钙;D:含氨的饱和食盐水、水
四种盐在不同温度下的溶解度(g/100g水)表
(说明:①>35℃NH4HCO3会有分解)
请回答以下问题:
(1)装置的连接顺序应是_________ (填字母)。
(2)A装置中盛放的试剂是_________ ,其作用是______________ 。
(3)在实验过程中,需要控制D温度在30℃~35℃,原因是__________________ 。
(4)反应结束后,将锥形瓶浸在冷水中,析出NaHCO3晶体。用蒸馏水洗涤NaHCO3晶体的目的是除去____________ 杂质(以化学式表示)
(5)将锥形瓶中的产物过滤后,所得的母液中含有________ (以化学式表示),加入氯化氢,并进行___________ 操作,使NaCl溶液循环使用,同时可回收NH4C1。

四种盐在不同温度下的溶解度(g/100g水)表
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ | |
| NaCl | 35.7 | 35.8 | 36.0 | 36_3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | —① | — | — | — |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
(说明:①>35℃NH4HCO3会有分解)
请回答以下问题:
(1)装置的连接顺序应是
(2)A装置中盛放的试剂是
(3)在实验过程中,需要控制D温度在30℃~35℃,原因是
(4)反应结束后,将锥形瓶浸在冷水中,析出NaHCO3晶体。用蒸馏水洗涤NaHCO3晶体的目的是除去
(5)将锥形瓶中的产物过滤后,所得的母液中含有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】葡萄糖酸锌作为补锌药,具有见效快、吸收率高、副作用小、使用方便等优点。某学习小组在实验室以葡萄糖和氧化锌为主要原料合成该物质。
反应原理:CH2OH(CHOH)4CHO + H2O2 CH2OH(CHOH)4COOH + H2O
CH2OH(CHOH)4COOH + H2O
2CH2OH(CHOH)4COOH + ZnO Zn[CH2OH(CHOH)4COO] 2 + H2O
Zn[CH2OH(CHOH)4COO] 2 + H2O
设计的合成路线为:
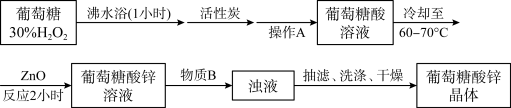
相关信息如下:
葡萄糖酸锌易溶于水,在乙醇与水的混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图如图1
实验中所涉及的部分装置如图所示(图2装置先制备葡萄糖酸,再与ZnO反应制备
葡萄糖酸锌),图3为抽滤装置
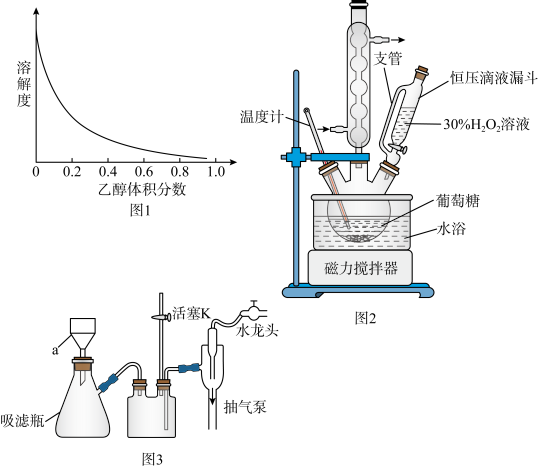
请根据以上信息,回答下列问题:
(1)图2中恒压滴液漏斗的支管的作用是___________ ,图3中a装置的名称____________ 。
(2)30%H2O2所用的物质的量大概是葡萄糖的3倍,而且并未一次性与葡萄糖混合,而是利用恒压滴液漏斗缓慢滴加的理由_________________________________ 。
(3)操作A是______________ ,物质B是________________ 。
(4)抽滤完毕或中途停止抽滤时,应先___________________ ,然后____________________ 。
(5)三颈烧瓶中的葡萄糖酸锌晶体转入到抽滤装置中时,瓶壁上往往还粘有少量晶体,需选用液体将瓶壁上的晶体冲洗下来后转入到抽滤装置中,下列液体最合适的是_______ 。
A 无水乙醇 B 饱和NaCl溶液 C 70%乙醇水溶液 D 滤液
(6)下列说法正确的是________ 。
A 用银氨溶液来替代30%H2O2将葡萄糖转变成葡萄糖酸,既经济又方便
B ZnO粉末与葡萄糖酸反应时,利用磁力搅拌可以增大ZnO粉末与葡萄糖酸的接触面积,加快反应速率
C 在抽滤过程中,如果吸滤瓶中的液体快接近支管口时,则拔掉吸滤瓶上的橡皮管,并从吸滤瓶的支管口倒出溶液
D 将葡萄糖酸锌晶体放在干燥器中可以防潮,在干燥器中放有干燥剂,并添加了无水CoCl2来指示是否得更换干燥剂,如果CoCl2为蓝色,说明干燥剂已经失效
反应原理:CH2OH(CHOH)4CHO + H2O2
 CH2OH(CHOH)4COOH + H2O
CH2OH(CHOH)4COOH + H2O2CH2OH(CHOH)4COOH + ZnO
 Zn[CH2OH(CHOH)4COO] 2 + H2O
Zn[CH2OH(CHOH)4COO] 2 + H2O设计的合成路线为:

相关信息如下:
葡萄糖酸锌易溶于水,在乙醇与水的混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图如图1
实验中所涉及的部分装置如图所示(图2装置先制备葡萄糖酸,再与ZnO反应制备
葡萄糖酸锌),图3为抽滤装置

请根据以上信息,回答下列问题:
(1)图2中恒压滴液漏斗的支管的作用是
(2)30%H2O2所用的物质的量大概是葡萄糖的3倍,而且并未一次性与葡萄糖混合,而是利用恒压滴液漏斗缓慢滴加的理由
(3)操作A是
(4)抽滤完毕或中途停止抽滤时,应先
(5)三颈烧瓶中的葡萄糖酸锌晶体转入到抽滤装置中时,瓶壁上往往还粘有少量晶体,需选用液体将瓶壁上的晶体冲洗下来后转入到抽滤装置中,下列液体最合适的是
A 无水乙醇 B 饱和NaCl溶液 C 70%乙醇水溶液 D 滤液
(6)下列说法正确的是
A 用银氨溶液来替代30%H2O2将葡萄糖转变成葡萄糖酸,既经济又方便
B ZnO粉末与葡萄糖酸反应时,利用磁力搅拌可以增大ZnO粉末与葡萄糖酸的接触面积,加快反应速率
C 在抽滤过程中,如果吸滤瓶中的液体快接近支管口时,则拔掉吸滤瓶上的橡皮管,并从吸滤瓶的支管口倒出溶液
D 将葡萄糖酸锌晶体放在干燥器中可以防潮,在干燥器中放有干燥剂,并添加了无水CoCl2来指示是否得更换干燥剂,如果CoCl2为蓝色,说明干燥剂已经失效
您最近一年使用:0次



