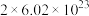硫酸亚铁铵受热分解的反应方程式为2(NH4)2Fe(SO4)2 Fe2O3+2NH3↑+N2↑+4SO2↑+5H2O,用NA表示阿伏伽德罗常数的值。下列说法正确的是
Fe2O3+2NH3↑+N2↑+4SO2↑+5H2O,用NA表示阿伏伽德罗常数的值。下列说法正确的是
 Fe2O3+2NH3↑+N2↑+4SO2↑+5H2O,用NA表示阿伏伽德罗常数的值。下列说法正确的是
Fe2O3+2NH3↑+N2↑+4SO2↑+5H2O,用NA表示阿伏伽德罗常数的值。下列说法正确的是| A.1 L 0.1 mol·L−1 (NH4)2Fe(SO4)2溶液中Fe2+的数目为0.1NA |
| B.将1 mol SO2和1 mol O2充分反应后,其分子总数为1.5NA |
| C.常温常压下,3.0 g 15N2中含有的中子总数为1.4NA |
| D.标准状况下,每生成15.68 L气体转移电子数目为0.8NA |
2019高三下·全国·专题练习 查看更多[5]
(已下线)2019年3月2019届高三第一次全国大联考(新课标Ⅰ卷)-化学【市级联考】广东省肇庆市2019届高中毕业班第三次统一检测理综化学试题福建省2020届高三化学总复习专题训练——硫酸亚铁铵山西省忻州市第一中学2020-2021学年高二上学期开学考试化学试题(已下线)模块三 化学计量在实验中的应用(模块检测)-2022年高考化学一轮复习小题多维练(全国通用)
更新时间:2019-04-28 21:30:24
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.0.5 乙醇中含有3 乙醇中含有3 个 个 键 键 |
B.22.4L(标准状况)乙烯气体完全燃烧后生成的水分子总数为2 |
C.常温下,1  溶液含有的氯原子数目为 溶液含有的氯原子数目为 |
D.32g硫在足量的氧气中充分燃烧,转移电子数为6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知 是阿伏加 德罗常数的值,下列说法错误的是
是阿伏加 德罗常数的值,下列说法错误的是

 是阿伏加 德罗常数的值,下列说法错误的是
是阿伏加 德罗常数的值,下列说法错误的是

A.常温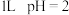 的 的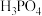 溶液中含 溶液中含 数目 数目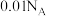 |
B.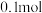 苯被氧化为 苯被氧化为 转移电子数为 转移电子数为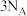 |
C. 甘油 甘油 丙三醇 丙三醇 中共价键数目为 中共价键数目为 |
D.18g重水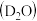 中含有的中子数为 中含有的中子数为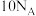 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】NA表示阿伏加 德罗常数,下列叙述正确的是( )
| A.等物质的量的N2和CO所含分子数均为NA |
| B.1.7gH2O2中含有的电子数为0.9NA |
| C.标准状况下,22.4L空气含有NA个单质分子 |
| D.1mol·L-1NaCl溶液含有NA个Na+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA代表阿伏加罗常数的值,下列叙述正确的是
| A.标准状况下,22.4LCCl4中含有共价键的数目为4NA |
| B.常温常压下,6.4 g氧气和臭氧中含有的原子总数为0.4NA |
| C.室温时,0.1mol/L的NH4Cl溶液中, 含Cl-的数目为0.1NA |
| D.一定条件下6.4gSO2与足量氧气反应生成SO3,转移电子数为0.2 NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】设NA为阿伏加德罗常数的值。下列说法正确的是
| A.一定条件下,将1 mol N2和3 mol H2混合发生反应,转移的电子总数为6 NA |
| B.1 L 0.1 mol·L-1的Na2CO3溶液中阴离子的总数大于0.1 NA |
| C.向FeI2溶液中通入适量Cl2,当有2 mol Fe2+被氧化时,消耗Cl2的分子数为NA |
| D.1 mol-CH3中所含的电子总数为10 NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知NA为阿伏加德罗常数,下列说法正确的是
| A.25℃时,1.0 L pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA |
| B.0.1 mol H2C2O4被氧化为CO2,转移的电子数为0.1NA |
| C.32 g乙醇和14 g二甲醚(H3C-O-CH3)组成的混合物中共价键数目为8NA |
| D.1 mol Na2O2晶体所含离子总数为4NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.28g 氮气含有的原子数是NA |
| B.标准状况下,22.4L水的分子数是NA |
| C.2L0.5mol·L-1的稀硫酸中含有H2SO4分子数是NA |
D.20g 含有的中子数是10NA 含有的中子数是10NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.标准状况下,2.24 L  中含有的氢原子数为 中含有的氢原子数为 |
B.2 mol NO与1 mol  在密闭容器中充分反应后的分子数小于 在密闭容器中充分反应后的分子数小于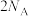 |
C.500 mL 0.1 mol/L的 溶液中,所含的 溶液中,所含的 总数为 总数为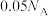 |
D.1 mol  中,π键的数目为 中,π键的数目为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】设 代表阿伏加德罗常数的值,下列叙述错误的是
代表阿伏加德罗常数的值,下列叙述错误的是
 代表阿伏加德罗常数的值,下列叙述错误的是
代表阿伏加德罗常数的值,下列叙述错误的是A.1.8g  含的质子数为 含的质子数为 |
B.质量相等的 和 和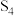 ,所含的S原子数均为 ,所含的S原子数均为 |
C.56g Fe与足量 加热完全反应,电子转移数为3 加热完全反应,电子转移数为3 |
D. 和 和 的混合物10g,与足量盐酸反应生成 的混合物10g,与足量盐酸反应生成 分子数为0.1 分子数为0.1 |
您最近一年使用:0次

 个
个 混合气体的物质的量一定为0.15mol
混合气体的物质的量一定为0.15mol 的
的 和
和 混合气体的物质的量为0.5mol
混合气体的物质的量为0.5mol