(1)下列装置属于原电池的是___________ ;
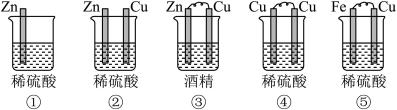
(2)在选出的原电池中,______ 是负极,发生______ (氧化、还原) 反应 ,______ 是正极 ,该极的现象___________________________ ;
(3)在该原电池的内电路中,硫酸根离子移向_________ (正、负)极。
(4)此原电池反应的化学方程式为___________________________ 。

(2)在选出的原电池中,
(3)在该原电池的内电路中,硫酸根离子移向
(4)此原电池反应的化学方程式为
18-19高一下·山东德州·期中 查看更多[2]
更新时间:2019-05-13 16:00:11
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】在原电池中,若两电极是活泼性不同的金属,一般负极金属的活泼性比正极金属的的活泼性___________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】填空
(1)理论上,任何自发的___________ 反应都可以设计成原电池。
(2)外电路:___________ 性较强的物质在负极上失去电子,___________ 性较强的物质在正极上得到电子。
(3)内电路:将两电极浸入电解质溶液中,阴、阳离子作___________ 移动。
(1)理论上,任何自发的
(2)外电路:
(3)内电路:将两电极浸入电解质溶液中,阴、阳离子作
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气。对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
Ⅰ.脱硝:
已知:H2的燃烧热为285.8kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔH=+133kJ·mol-1
H2O(g)=H2O(l) ΔH=-44kJ·mol-1
催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为:____________ 。
Ⅱ.脱碳:
(1)向2L密闭容器中加入2molCO2和6molH2,在适当的催化剂作用下,发生反应:
CO2(g)+3H2(g) CH3OH(l)+H2O(l)
CH3OH(l)+H2O(l)
①该反应自发进行的条件是_____________ (填“低温”、“高温”或“任意温度”)
②下列叙述能说明此反应达到平衡状态的是____________ 。(填字母)
a.混合气体的平均式量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1molCO2生成的同时有3mol H—H键断裂
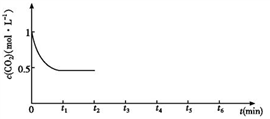
③CO2的浓度随时间(0~t2)变化如下图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出t2~t6 CO2浓度随时间的变化。_____________
⑵改变温度,使反应CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH﹤0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
CH3OH(g)+H2O(g) ΔH﹤0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
①达到平衡时,反应Ⅰ、Ⅱ对比:平衡常数K(I)______ K(II)(填“﹥”“﹤”或“=”下同);平衡时CH3OH的浓度c(I)____ c(II)。
②对反应Ⅰ,前10min内的平均反应速率v(CH3OH)=_______ 。在其他条件不变的情况下,若30min时只改变温度T2℃,此时H2的物质的量为3.2mol,则T1___ T2(填“>”、“<”或“=”)。若30min时只向容器中再充入1molCO2(g)和1molH2O(g),则平衡_____ 移动(填“正向”“逆向”或“不”)。
⑶利用人工光合作用可将CO2转化为甲酸,反应原理为2CO2+2H2O=2HCOOH+O2,
装置如图所示:
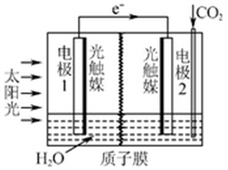
①电极2的电极反应式是____________ ;
②在标准状况下,当电极2室有11.2L CO2反应。 理论上电极1室液体质量_____ (填“增加”或“减少”______ g。
Ⅰ.脱硝:
已知:H2的燃烧热为285.8kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔH=+133kJ·mol-1
H2O(g)=H2O(l) ΔH=-44kJ·mol-1
催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为:
Ⅱ.脱碳:
(1)向2L密闭容器中加入2molCO2和6molH2,在适当的催化剂作用下,发生反应:
CO2(g)+3H2(g)
 CH3OH(l)+H2O(l)
CH3OH(l)+H2O(l)①该反应自发进行的条件是
②下列叙述能说明此反应达到平衡状态的是
a.混合气体的平均式量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1molCO2生成的同时有3mol H—H键断裂
③CO2的浓度随时间(0~t2)变化如下图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出t2~t6 CO2浓度随时间的变化。

⑵改变温度,使反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH﹤0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
CH3OH(g)+H2O(g) ΔH﹤0中的所有物质都为气态。起始温度、体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应Ⅰ:恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 | ||||
| 反应Ⅱ:绝热恒容 | 0min | 0 | 0 | 2 | 2 |
①达到平衡时,反应Ⅰ、Ⅱ对比:平衡常数K(I)
②对反应Ⅰ,前10min内的平均反应速率v(CH3OH)=
⑶利用人工光合作用可将CO2转化为甲酸,反应原理为2CO2+2H2O=2HCOOH+O2,
装置如图所示:

①电极2的电极反应式是
②在标准状况下,当电极2室有11.2L CO2反应。 理论上电极1室液体质量
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】某化学兴趣小组为了探究原电池产生电流的过程,设计了如图所示实验:
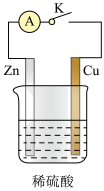
(1)下列叙述中正确的是___ 。
A.打开开关K时铜片作负极,关闭开关K时铜片作正极
B.打开开关K,锌片和铜片上均有气泡产生
C.关闭开关K后,溶液中的H+浓度减小
D.关闭开关K产生气泡的速率比打开开关K时慢
(2)打开开关K后,装置中发生反应的离子方程式为___ 。
(3)关闭开关K后,则该装置为___ (填“原电池”或“电解池”),锌极为___ 极(填“正”、“负”、“阳”或“阴”),铜极上的电极反应式为__ 。若反应过程中有0.3mol的电子发生转移,则产生的气体在标准状况下的体积为___ L。

(1)下列叙述中正确的是
A.打开开关K时铜片作负极,关闭开关K时铜片作正极
B.打开开关K,锌片和铜片上均有气泡产生
C.关闭开关K后,溶液中的H+浓度减小
D.关闭开关K产生气泡的速率比打开开关K时慢
(2)打开开关K后,装置中发生反应的离子方程式为
(3)关闭开关K后,则该装置为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】化学反应中的能量和速率变化对生产生活有着重要意义。某研究学习小组进行下列探究。
(1)甲同学探究反应Fe+H2SO4(稀)=FeSO4+H2↑中的能量变化。向装有铁片的试管中加入1mol/L的H2SO4,观察到试管内有气泡产生,触摸试管外壁,温度升高。
①该反应为___________ (填“放热”或“吸热”)反应。
②该反应反应物的总能量___________ (填“>”或“<”)生成物的总能量
(2)乙同学认为原电池原理也可加快化学反应速率,他设计如图所示实验装置。铁片上的电极反应式为___________ 。

(3)下列反应通过原电池实现化学能直接转化为电能的___________ (填序号)。
①2H2+O2=2H2O ②Fe+Cu2+=Fe2++Cu ③CaO+H2O=Ca(OH)2
(1)甲同学探究反应Fe+H2SO4(稀)=FeSO4+H2↑中的能量变化。向装有铁片的试管中加入1mol/L的H2SO4,观察到试管内有气泡产生,触摸试管外壁,温度升高。
①该反应为
②该反应反应物的总能量
(2)乙同学认为原电池原理也可加快化学反应速率,他设计如图所示实验装置。铁片上的电极反应式为

(3)下列反应通过原电池实现化学能直接转化为电能的
①2H2+O2=2H2O ②Fe+Cu2+=Fe2++Cu ③CaO+H2O=Ca(OH)2
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】电能是现代社会应用最广泛的能源之一。
(1)某原电池装置如图所示。
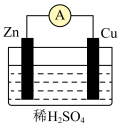
① 电极为原电池的
电极为原电池的___________ 极(填“正”或“负”),电极反应式是___________ 。
② 电极上发生的反应属于
电极上发生的反应属于___________ (填“氧化”或“还原”)反应,当铜表面析出 氢气(标准状况)时,导线中通过了
氢气(标准状况)时,导线中通过了___________  电子。
电子。
③能证明化学能转化为电能的实验现象是:铜片上有气泡产生、___________ 。
(2)下列反应通过原电池装置,可实现化学能直接转化为电能的是___________ (填序号)。
A.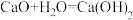 B.
B. C.
C.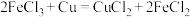
(1)某原电池装置如图所示。

①
 电极为原电池的
电极为原电池的②
 电极上发生的反应属于
电极上发生的反应属于 氢气(标准状况)时,导线中通过了
氢气(标准状况)时,导线中通过了 电子。
电子。③能证明化学能转化为电能的实验现象是:铜片上有气泡产生、
(2)下列反应通过原电池装置,可实现化学能直接转化为电能的是
A.
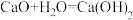 B.
B. C.
C.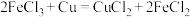
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】原电池是把____ 转化成_____ 的装置,其反应的实质是________ 。写出铜锌原电池(稀硫酸为介质)的电极反应:正极________ ,负极____ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】氢气是一种高效清洁的可再生能源,请回答:
(1)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式:_____________ 。
(2)氢氧燃料电池一般是以惰性金属铂(Pt)或石墨做电极材料,若电解质溶液为KOH,则负极上的电极反应式为__________________________________ 。
(1)由氢气和氧气反应生成1mol水蒸气放热241.8kJ,写出该反应的热化学方程式:
(2)氢氧燃料电池一般是以惰性金属铂(Pt)或石墨做电极材料,若电解质溶液为KOH,则负极上的电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】利用电化学装置原理可以设计出许多应用于环境保护、化学品提取的装置。
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。图1是通过人工光合作用,以 和
和 为原料制备HCOOH和
为原料制备HCOOH和 的原理示意图。
的原理示意图。______ 极,表面发生的电极反应为______ 。
(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图2所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。______
②Y极生成1 mol 时,
时,______ mol 移向
移向______ (填“X”或“Y”)极。
(3)NO也可以利用电化学手段将其转化为 脱除,装置如图3所示,电极为多孔惰性材料。则负极的电极反应式是
脱除,装置如图3所示,电极为多孔惰性材料。则负极的电极反应式是____________ 。
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。图1是通过人工光合作用,以
 和
和 为原料制备HCOOH和
为原料制备HCOOH和 的原理示意图。
的原理示意图。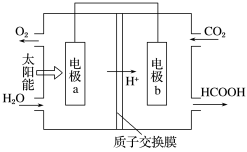
(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如图2所示,该电池从浓缩海水中提取LiCl的同时又获得了电能。
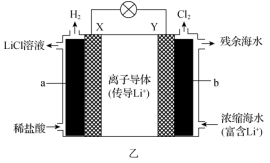
②Y极生成1 mol
 时,
时, 移向
移向(3)NO也可以利用电化学手段将其转化为
 脱除,装置如图3所示,电极为多孔惰性材料。则负极的电极反应式是
脱除,装置如图3所示,电极为多孔惰性材料。则负极的电极反应式是
您最近一年使用:0次



