电能是现代社会应用最广泛的能源之一。
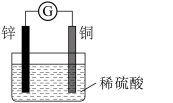
(1)某原电池装置如图所示。
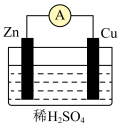
① 电极为原电池的
电极为原电池的___________ 极(填“正”或“负”),电极反应式是___________ 。
② 电极上发生的反应属于
电极上发生的反应属于___________ (填“氧化”或“还原”)反应,当铜表面析出 氢气(标准状况)时,导线中通过了
氢气(标准状况)时,导线中通过了___________  电子。
电子。
③能证明化学能转化为电能的实验现象是:铜片上有气泡产生、___________ 。
(2)下列反应通过原电池装置,可实现化学能直接转化为电能的是___________ (填序号)。
A.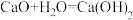 B.
B. C.
C.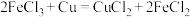
(1)某原电池装置如图所示。

①
 电极为原电池的
电极为原电池的②
 电极上发生的反应属于
电极上发生的反应属于 氢气(标准状况)时,导线中通过了
氢气(标准状况)时,导线中通过了 电子。
电子。③能证明化学能转化为电能的实验现象是:铜片上有气泡产生、
(2)下列反应通过原电池装置,可实现化学能直接转化为电能的是
A.
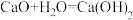 B.
B. C.
C.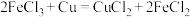
更新时间:2023-08-11 16:06:35
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】观察如图,回答问题:
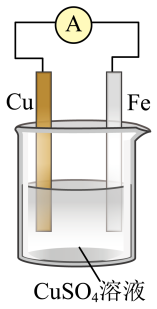
(1)该装置叫__ 装置,可以将__ 能转化为__ 能。
(2)负极是__ ,电极反应式为__ 。
(3)正极是__ ,电极反应式为__ 。
(4)电池总反应的离子方程式为__ 。

(1)该装置叫
(2)负极是
(3)正极是
(4)电池总反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.Zn+CuSO4=ZnSO4+Cu B.2NaOH+H2SO4=Na2SO4+2H2O,判断能否设计成原电池A._______ ,B. _______ 。(填“能”或“不能”)
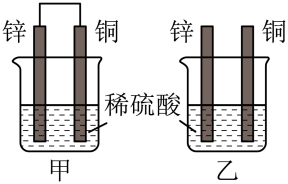
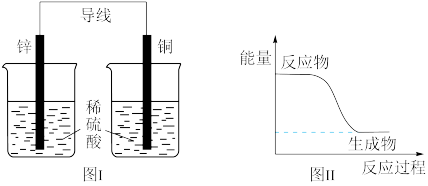
(2)将纯锌片和纯铜片按图方式插入100mL相同浓度的稀硫酸中一段时间。
下列说法正确的是_______。
(3)请写出图中构成原电池的正极电极反应式_______ 。
(4)电池工作时,溶液中SO 向
向_______ 极移动(填“锌”或“铜”);电池工作完成后,溶液中SO 浓度
浓度_______ (填“增大”“减小”或“不变”)。
(5)化学能可与热能、电能等相互转化。下列表述错误的是_______。
(1)现有如下两个反应:A.Zn+CuSO4=ZnSO4+Cu B.2NaOH+H2SO4=Na2SO4+2H2O,判断能否设计成原电池A.
(2)将纯锌片和纯铜片按图方式插入100mL相同浓度的稀硫酸中一段时间。

下列说法正确的是_______。
| A.甲、乙装置均实现了化学能转变为电能 |
| B.甲中铜片上有气体产生,铜片发生了氧化反应 |
| C.两烧杯中反应原理相同,稀硫酸起始浓度相同,因而反应速率相同 |
| D.两烧杯溶液中的H+均被消耗,因而H+浓度减小 |
(4)电池工作时,溶液中SO
 向
向 浓度
浓度(5)化学能可与热能、电能等相互转化。下列表述错误的是_______。

| A.化学反应中能量变化的主要原因是化学键的断裂与形成 |
| B.酸碱中和反应中,反应物的总能量比生成物的总能量高 |
| C.图I所示的装置能将化学能转变为电能 |
| D.图II所示的反应为放热反应 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。将锌片和铜片插入相同浓度的稀硫酸中,如图所示。按要求回答下列问题:

(1)下列说法正确的是_______ (填字母)。
a.甲、乙均为化学能转变为电能的装置
b.甲中锌片是负极,乙中铜片是正极
c.甲、乙溶液中的pH均增大
d.若将稀硫酸换为硫酸铜溶液,则甲、乙中铜片的质量均增加
(2)甲、乙中构成原电池的正极电极反应式为_______ ,原电池工作过程中,电流由_______ (填“铜片”或“锌片”)经导线流向_______ (填“铜片”或“锌片”)。溶液中的 向
向_______ (填“正极”或“负极”)移动。
(3)原电池工作一段时间后,若溶液质量增加3.15g,则放出气体_______ mol。
(4)对甲、乙装置做如下变化后,可形成原电池的是_______ (填字母)。
a.甲中铜片换成锌片
b.乙中锌片和铜片相互倾斜至上端接触
c.甲中稀硫酸用乙醇代替

(1)下列说法正确的是
a.甲、乙均为化学能转变为电能的装置
b.甲中锌片是负极,乙中铜片是正极
c.甲、乙溶液中的pH均增大
d.若将稀硫酸换为硫酸铜溶液,则甲、乙中铜片的质量均增加
(2)甲、乙中构成原电池的正极电极反应式为
 向
向(3)原电池工作一段时间后,若溶液质量增加3.15g,则放出气体
(4)对甲、乙装置做如下变化后,可形成原电池的是
a.甲中铜片换成锌片
b.乙中锌片和铜片相互倾斜至上端接触
c.甲中稀硫酸用乙醇代替
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】2020年第七十五届联合国大会上,中国向世界郑重承诺在2030年前实现碳达峰,在2060年前实现碳中和。大力发展绿色能源、清洁能源是实现碳中和的最有效方法。
(1)原电池反应能够提供电能而不产生CO2气体,下图是某原电池装置图。_______ 极,发生_______ (填“氧化”或“还原”)反应。
②Cu棒,上发生的电极反应是_______ 。
③溶液中H+向_______ (填“Zn”或“Cu”)电极定向移动。
(2)将上述装置中电解质稀H2SO4换为足量AgNO3溶液,灯泡也变亮,电流表指针偏转,无色溶液颜色没有变化。
①原电池的负极是_______ (填“Zn”或“Cu”),正极的电极反应是_______ 。
②若更换电解质时称量两个电极,质量恰好相等,放电一段时间后再称量两个电极,发现质量相差2.81g,则导线上通过的n(e-)=_______ mol。
(3)碱性锌锰电池是日常生活中常用电池,原电池反应是:Zn(①)+ 2MnO2 (②) +2H2O =Zn(OH)2(③)+2MnOOH(④)。
①该原电池的正极材料是_______ (填序号,下同),负极材料是_______ 。
②该原电池电解质是KOH溶液,写出正极的电极反应_______ 。
(1)原电池反应能够提供电能而不产生CO2气体,下图是某原电池装置图。

②Cu棒,上发生的电极反应是
③溶液中H+向
(2)将上述装置中电解质稀H2SO4换为足量AgNO3溶液,灯泡也变亮,电流表指针偏转,无色溶液颜色没有变化。
①原电池的负极是
②若更换电解质时称量两个电极,质量恰好相等,放电一段时间后再称量两个电极,发现质量相差2.81g,则导线上通过的n(e-)=
(3)碱性锌锰电池是日常生活中常用电池,原电池反应是:Zn(①)+ 2MnO2 (②) +2H2O =Zn(OH)2(③)+2MnOOH(④)。
①该原电池的正极材料是
②该原电池电解质是KOH溶液,写出正极的电极反应
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】写出下列原电池的电极反应和总反应(属于离子反应的,用离子方程式表示)。
(1)负极:___________ ;正极:___________ ;总反应式:___________ 。
(2)负极:___________ ;正极:___________ ;总反应式:___________ 。
| 负极 | 正极 | 电解质溶液 | |
| (1) | 铁 | 铜 | 稀硫酸 |
| (2) | 铜 | 银 | AgNO3溶液 |
(1)负极:
(2)负极:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】氢氧燃料电池是最常见的燃料电池,该电池在正极通入氧气,在负极通入氢气,而电解质溶液通常是KOH溶液。
(1)请写出氢氧燃料电池负极的电极反应方程式___ 。
(2)氢氧燃料电池有何优点:___ 。
(1)请写出氢氧燃料电池负极的电极反应方程式
(2)氢氧燃料电池有何优点:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】根据原电池原理,结合装置图,按要求解答问题:

(1)若X为Zn,Y为硫酸铜溶液,溶液中的Cu2+移向___________ (填“Cu”或“X”)电极。
(2)若X为银,Y为硝酸银溶液,则X的电极方程式___________
(3)若X为Fe,Y为浓硝酸,则Cu电极电极方程式是___________ 。

(1)若X为Zn,Y为硫酸铜溶液,溶液中的Cu2+移向
(2)若X为银,Y为硝酸银溶液,则X的电极方程式
(3)若X为Fe,Y为浓硝酸,则Cu电极电极方程式是
您最近一年使用:0次