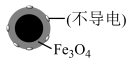
观察如图,回答问题:
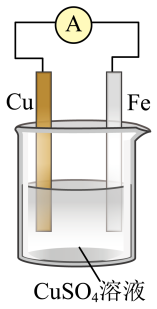
(1)该装置叫__ 装置,可以将__ 能转化为__ 能。
(2)负极是__ ,电极反应式为__ 。
(3)正极是__ ,电极反应式为__ 。
(4)电池总反应的离子方程式为__ 。

(1)该装置叫
(2)负极是
(3)正极是
(4)电池总反应的离子方程式为
更新时间:2020-01-29 20:19:14
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】电池的种类繁多,应用广泛,根据电化学原理回答下列问题。
(1)下图中,若溶液 为稀
为稀 ,电流表指针发生偏转,
,电流表指针发生偏转, 电极材料为
电极材料为 且作负极,则
且作负极,则 电极上发生的电极反应式为
电极上发生的电极反应式为___________ ;反应进行一段时间后溶液酸性将___________ (填“增强”“减弱”或“基本不变”)。
(2) 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如图,电池总反应为
组合形成的质子交换膜燃料电池的结构示意图如图,电池总反应为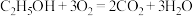 ,则
,则 电极是
电极是___________ (填“正极”或“负极”), 电极的电极反应式为
电极的电极反应式为___________ 。若线路中转移 电子,则上述
电子,则上述 燃料电池消耗的
燃料电池消耗的 在标准状况下的体积为
在标准状况下的体积为___________ L。
(3)一种熔融碳酸盐燃料电池的原理示意图如下。请回答下列问题:
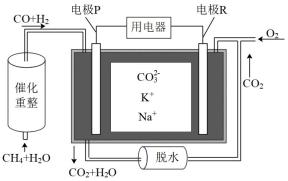
①反应 ,每消耗
,每消耗 理论上转移的电子数目为
理论上转移的电子数目为___________
②电池工作时, 向电极
向电极___________ (填“A”或“B”)移动。
③电极 上发生的电极反应为
上发生的电极反应为___________ 。
(4)科学家研发出一种新系统,通过“溶解”水中的二氧化碳,以触发电化学反应,有效减少碳的排放,其工作原理如图所示。

①系统工作时,a极为___________ 极,b极区的电极反应式为___________ 。
②系统工作时b极区有少量固体析出,可能的原因是___________ 。
(1)下图中,若溶液
 为稀
为稀 ,电流表指针发生偏转,
,电流表指针发生偏转, 电极材料为
电极材料为 且作负极,则
且作负极,则 电极上发生的电极反应式为
电极上发生的电极反应式为
(2)
 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如图,电池总反应为
组合形成的质子交换膜燃料电池的结构示意图如图,电池总反应为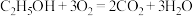 ,则
,则 电极是
电极是 电极的电极反应式为
电极的电极反应式为 电子,则上述
电子,则上述 燃料电池消耗的
燃料电池消耗的 在标准状况下的体积为
在标准状况下的体积为
(3)一种熔融碳酸盐燃料电池的原理示意图如下。请回答下列问题:

①反应
 ,每消耗
,每消耗 理论上转移的电子数目为
理论上转移的电子数目为②电池工作时,
 向电极
向电极③电极
 上发生的电极反应为
上发生的电极反应为(4)科学家研发出一种新系统,通过“溶解”水中的二氧化碳,以触发电化学反应,有效减少碳的排放,其工作原理如图所示。

①系统工作时,a极为
②系统工作时b极区有少量固体析出,可能的原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】电化学原理在探究物质性质和实际生产中应用广泛,据此回答下列问题。
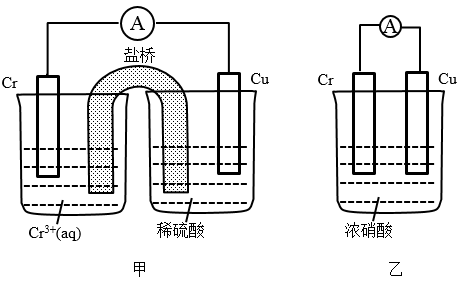
(1)在如图装置中,观察到装置甲铜电极上产生大量的无色气体;而装置乙中铜电极上无气体产生,铬电极上产生大量红棕色气体。由装置甲知铬的金属活动性比铜__ (填“强”或“弱”);由装置乙知常温下铬在浓硝酸中出现__ 现象。
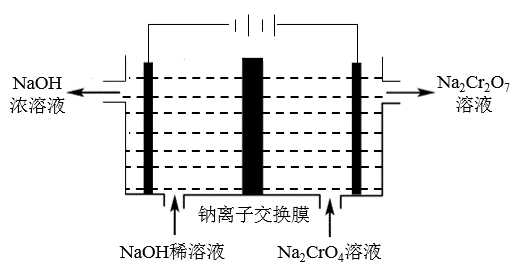
(2)工业上使用如图装置,以石墨作电极电解Na2CrO4溶液,使Na2CrO4转化为Na2Cr2O7,其转化原理为__ 。
(3)CrO3和K2Cr2O7均易溶于水,它们是工业废水造成铬污染的主要原因。要将Cr(Ⅵ)转化为Cr(Ⅲ)常见的处理方法是电解法和铁氧磁体法。
①电解法:将含Cr2O 的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和Cr2O
的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和Cr2O 发生反应,则阳极的电极反应式为
发生反应,则阳极的电极反应式为__ 。阴极上Cr2O 、H+、Fe3+都可能放电。若Cr2O
、H+、Fe3+都可能放电。若Cr2O 放电,则阴极的电极反应式为
放电,则阴极的电极反应式为__ ;若H+放电,则阴极区形成Fe(OH)3和Cr(OH)3沉淀。
②铁氧磁体法:在含Cr(Ⅵ)的废水中加入绿矾,在pH<4时发生反应使Cr(Ⅵ)转化为Cr(Ⅲ),调节溶液pH为6~8,使溶液中的Fe(Ⅱ)、Fe(Ⅲ)、Cr(Ⅲ)析出组成相当于Fe(Ⅱ)[Fe(Ⅲ)x•Cr(Ⅲ)2-x]O4(铁氧磁体)的沉淀,则铁氧磁体中x=___ 。
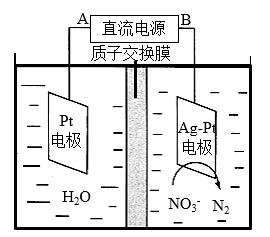
(4)电解法还可用于处理酸性硝酸盐污水,设计如图电解池。若电解过程中转移了0.1mol电子,则质子交换膜两侧电解液的质量变化差(△m左−△m右)为___ g。

(1)在如图装置中,观察到装置甲铜电极上产生大量的无色气体;而装置乙中铜电极上无气体产生,铬电极上产生大量红棕色气体。由装置甲知铬的金属活动性比铜
(2)工业上使用如图装置,以石墨作电极电解Na2CrO4溶液,使Na2CrO4转化为Na2Cr2O7,其转化原理为

(3)CrO3和K2Cr2O7均易溶于水,它们是工业废水造成铬污染的主要原因。要将Cr(Ⅵ)转化为Cr(Ⅲ)常见的处理方法是电解法和铁氧磁体法。
①电解法:将含Cr2O
 的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和Cr2O
的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和Cr2O 发生反应,则阳极的电极反应式为
发生反应,则阳极的电极反应式为 、H+、Fe3+都可能放电。若Cr2O
、H+、Fe3+都可能放电。若Cr2O 放电,则阴极的电极反应式为
放电,则阴极的电极反应式为②铁氧磁体法:在含Cr(Ⅵ)的废水中加入绿矾,在pH<4时发生反应使Cr(Ⅵ)转化为Cr(Ⅲ),调节溶液pH为6~8,使溶液中的Fe(Ⅱ)、Fe(Ⅲ)、Cr(Ⅲ)析出组成相当于Fe(Ⅱ)[Fe(Ⅲ)x•Cr(Ⅲ)2-x]O4(铁氧磁体)的沉淀,则铁氧磁体中x=
(4)电解法还可用于处理酸性硝酸盐污水,设计如图电解池。若电解过程中转移了0.1mol电子,则质子交换膜两侧电解液的质量变化差(△m左−△m右)为

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】能源是现代文明的动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。
(1)从能量的变化和反应的快慢等角度研究反应:2H2(g)+O2(g)=2H2O(g)。已知该反应为放热反应,下图能正确表示该反应中能量变化的是_______ (填“a”或“b”)。

从断键和成键的角度分析上述反应中能量的变化,化学键的键能如下表所示:
则生成1molH2O(g)可以放出热量_______ kJ。
(2)下列属于吸热反应的是_______ (填序号)。
a.稀释浓硫酸
b.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.CO2和单质碳的反应
d.高温煅烧石灰石使其分解
e.铁在氯气中燃烧
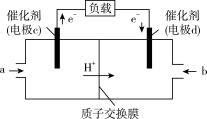
(3)氢燃料电池车是北京冬奥会期间的交通服务用车,酸性氢氧燃料电池的构造如图所示。

①若该电池中的电解质溶液是稀硫酸溶液,则a电极上发生反应的电极反应式为_______
②b电极是该电池的_______ 极(填“正”或“负”),从氧化还原反应的角度分析,该电极发生的反应属于_______ 反应。
③当转移0.2mol电子时,需要消耗标况下的氢气体积是_______ L。
(1)从能量的变化和反应的快慢等角度研究反应:2H2(g)+O2(g)=2H2O(g)。已知该反应为放热反应,下图能正确表示该反应中能量变化的是

从断键和成键的角度分析上述反应中能量的变化,化学键的键能如下表所示:
| 化学键 | H—H | O=O | H—O |
| 键能(kJ∙mol−1) | 436 | 496 | 463 |
(2)下列属于吸热反应的是
a.稀释浓硫酸
b.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.CO2和单质碳的反应
d.高温煅烧石灰石使其分解
e.铁在氯气中燃烧
(3)氢燃料电池车是北京冬奥会期间的交通服务用车,酸性氢氧燃料电池的构造如图所示。

①若该电池中的电解质溶液是稀硫酸溶液,则a电极上发生反应的电极反应式为
②b电极是该电池的
③当转移0.2mol电子时,需要消耗标况下的氢气体积是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】(1)氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接K1或K2,可交替得到H2和O2。
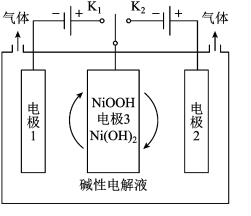
①制H2时,连接_____ 。产生H2的电极反应式是_____ 。
②改变开关连接方式,可得 O2。
③结合①和②中电极3的电极反应式,说明电极3的作用:_____ 。
(2)用零价铁(Fe)去除水体中的硝酸盐( )已成为环境修复研究的热点之一。
)已成为环境修复研究的热点之一。
①Fe 还原水体中 的反应原理如图所示。作负极的物质是
的反应原理如图所示。作负极的物质是_____ 。

正极的电极反应式是_____ 。
②将足量铁粉投入水体中,经 24 小时测定 的去除率和 pH,结果如下:
的去除率和 pH,结果如下:
pH=4.5 时, 的去除率低。其原因是
的去除率低。其原因是_____ 。

①制H2时,连接
②改变开关连接方式,可得 O2。
③结合①和②中电极3的电极反应式,说明电极3的作用:
(2)用零价铁(Fe)去除水体中的硝酸盐(
 )已成为环境修复研究的热点之一。
)已成为环境修复研究的热点之一。①Fe 还原水体中
 的反应原理如图所示。作负极的物质是
的反应原理如图所示。作负极的物质是
正极的电极反应式是
②将足量铁粉投入水体中,经 24 小时测定
 的去除率和 pH,结果如下:
的去除率和 pH,结果如下:| 初始 pH | pH=2.5 | pH=4.5 |
 的去除率3 的去除率3 | 接近100 % | <50 % |
| 24 小时 pH | 接近中性 | 接近中性 |
铁的最终物质形态 | FeO(OH)
| FeO(OH) |
 的去除率低。其原因是
的去除率低。其原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为:Zn+2OH--2e-=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-根据上述反应式,做下列题目。

(1)判断下列叙述中正确的是________ (填字母)。
(2)写出电池的总反应式:_______ 。
(3)使用时,负极区的pH________ (填“增大”“减小”或“不变”,下同),正极区的pH______ ,电解质溶液的pH_______ 。

(1)判断下列叙述中正确的是
| A.在使用过程中,电解质KOH被不断消耗 |
| B.使用过程中,电子由Ag2O极经外电路流向Zn极 |
| C.Zn是负极,Ag2O是正极 |
| D.Zn电极发生还原反应,Ag2O电极发生氧化反应 |
(3)使用时,负极区的pH
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】图为某同学设计的原电池装置

(1)当电解质溶液为稀硫酸时:①Fe电极是__ (填“正”或“负”)极,其电极反应为__
②Cu电极的电极反应为_____ ,该电极发生______ 反应(填“氧化”或“还原”)反应。原电池工作一段时间后,铁片的质量减少了2.8克,铜片表面产生气体____ L(标准状况下),导线中通过_____ mol电子。
(2)当电解质溶液为浓硫酸时:①Fe电极是______ 极,其电极反应为____ ,
②Cu电极是_____ 极,其电极反应为_______

(1)当电解质溶液为稀硫酸时:①Fe电极是
②Cu电极的电极反应为
(2)当电解质溶液为浓硫酸时:①Fe电极是
②Cu电极是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】按要求回答下列问题:
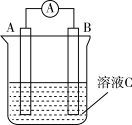
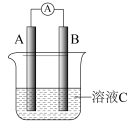
(1)如图所示是原电池的装置图。若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(负极)极材料为___________ ,B(正极)极材料为___________ ,溶液C为___________ 。
(2)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中O2-可以在固体介质NASICON(固溶体)内自由移动,工作时O2-的移动方向___________ (填“从a到b”或“从b到a”),负极发生的电极反应式为:___________ 。

(3)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示。
(1)如图所示是原电池的装置图。若需将反应:Cu+2Fe3+=Cu2++2Fe2+设计成如图所示的原电池装置,则A(负极)极材料为

(2)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中O2-可以在固体介质NASICON(固溶体)内自由移动,工作时O2-的移动方向

(3)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示。
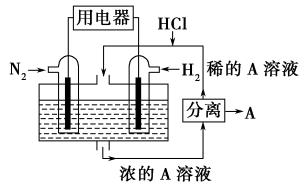
①电池正极发生的反应式是
②A是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】根据原电池原理,人们研制出了性能各异的化学电池。

(1)利用H2与O2的反应设计氢氧燃料电池,装置如图所示。
①通入H2的一极是电池的______ (填“正极”或“负极”)。
②电子从通入______ 的一极经导线流向通入______ 的一极(填“H2”或“O2”)。
③通入O2一极的电极反应式为______ 。
(2)一种新型Mg-海水电池的工作原理如图所示,下列说法正确的是______ (填字母)。

a.该电池工作时,金属镁作正极
b.H2O2在石墨电极上得到电子,发生还原反应

(1)利用H2与O2的反应设计氢氧燃料电池,装置如图所示。
①通入H2的一极是电池的
②电子从通入
③通入O2一极的电极反应式为
(2)一种新型Mg-海水电池的工作原理如图所示,下列说法正确的是

a.该电池工作时,金属镁作正极
b.H2O2在石墨电极上得到电子,发生还原反应
您最近一年使用:0次