微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为:Zn+2OH--2e-=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-根据上述反应式,做下列题目。

(1)判断下列叙述中正确的是________ (填字母)。
(2)写出电池的总反应式:_______ 。
(3)使用时,负极区的pH________ (填“增大”“减小”或“不变”,下同),正极区的pH______ ,电解质溶液的pH_______ 。

(1)判断下列叙述中正确的是
| A.在使用过程中,电解质KOH被不断消耗 |
| B.使用过程中,电子由Ag2O极经外电路流向Zn极 |
| C.Zn是负极,Ag2O是正极 |
| D.Zn电极发生还原反应,Ag2O电极发生氧化反应 |
(3)使用时,负极区的pH
23-24高二上·全国·课时练习 查看更多[1]
更新时间:2023-09-20 15:15:23
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】某原电池装置如图所示。
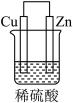
(1)其负极是_________ (填“Zn”或“Cu”),发生的是__________ (填“氧化”或“还原”)反应。
(2)正极上的现象是________________________________________ 。
(3)电子由_______________ (填“锌片”或“铜片”)沿导线流出。
(4)电池的总反应是_______________________________________ 。

(1)其负极是
(2)正极上的现象是
(3)电子由
(4)电池的总反应是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献。
(1)现有如下两个反应:A.Zn+CuSO4=ZnSO4+Cu B.2NaOH+H2SO4=Na2SO4+2H2O,判断能否设计成原电池A._______ ,B. _______ 。(填“能”或“不能”)
(2)将纯锌片和纯铜片按图方式插入100mL相同浓度的稀硫酸中一段时间。
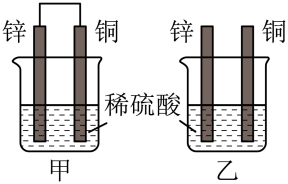
下列说法正确的是_______。
(3)请写出图中构成原电池的正极电极反应式_______ 。
(4)电池工作时,溶液中SO 向
向_______ 极移动(填“锌”或“铜”);电池工作完成后,溶液中SO 浓度
浓度_______ (填“增大”“减小”或“不变”)。
(5)化学能可与热能、电能等相互转化。下列表述错误的是_______。
(1)现有如下两个反应:A.Zn+CuSO4=ZnSO4+Cu B.2NaOH+H2SO4=Na2SO4+2H2O,判断能否设计成原电池A.
(2)将纯锌片和纯铜片按图方式插入100mL相同浓度的稀硫酸中一段时间。

下列说法正确的是_______。
| A.甲、乙装置均实现了化学能转变为电能 |
| B.甲中铜片上有气体产生,铜片发生了氧化反应 |
| C.两烧杯中反应原理相同,稀硫酸起始浓度相同,因而反应速率相同 |
| D.两烧杯溶液中的H+均被消耗,因而H+浓度减小 |
(4)电池工作时,溶液中SO
 向
向 浓度
浓度(5)化学能可与热能、电能等相互转化。下列表述错误的是_______。

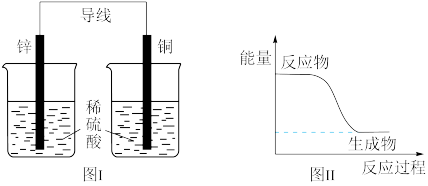
| A.化学反应中能量变化的主要原因是化学键的断裂与形成 |
| B.酸碱中和反应中,反应物的总能量比生成物的总能量高 |
| C.图I所示的装置能将化学能转变为电能 |
| D.图II所示的反应为放热反应 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】回答下列问题
(1)电子表和电子计算器中所用的是纽扣式微型银锌电池,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为Ag2O + Zn + H2O = 2Ag + Zn(OH)2
①工作时电子从___________ 极流向___________ 极(填“Ag2O”或“Zn”)。
②工作时电池正极区的pH___________ (填“增大”、“减小”或“不变”)。
③请写出负极的电极反应式:___________ 。
(2)家用液化气中主要成分之一是丁烷。 当1g丁烷完全燃烧并生成CO2和液态水时,放出热量50 kJ。试写出丁烷燃烧的热化学方程式:___________ 。
(1)电子表和电子计算器中所用的是纽扣式微型银锌电池,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为Ag2O + Zn + H2O = 2Ag + Zn(OH)2
①工作时电子从
②工作时电池正极区的pH
③请写出负极的电极反应式:
(2)家用液化气中主要成分之一是丁烷。 当1g丁烷完全燃烧并生成CO2和液态水时,放出热量50 kJ。试写出丁烷燃烧的热化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】能量转化是化学变化的主要特征之一,按要求回答下列问题。
(1)页岩气是从页岩层中开采出来的天然气,成分以甲烷为主,页岩气的资源潜力可能大于常规天然气。下列有关页岩气的叙述错误的是_______(填序号)。
(2)有关的电池装置如下:
①上述四种电池中,属于二次电池的是_______ (填序号,下同),属于干电池的是_______ 。
②a装置中,外电路中电子的流向是_______ (填“从Zn流向Cu”或“从Cu流向Zn”)。
③c装置中,若电解质改为碱性介质,则负极的电极反应式为_______ 。
(3)氧化还原反应一般可以设计成原电池。若将反应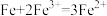 设计成原电池,则:
设计成原电池,则:
①该电池的电解质溶液可以是_______ 。
②当外电路中转移1mol e-时,电解质溶液增加的质量是_______ g。
(1)页岩气是从页岩层中开采出来的天然气,成分以甲烷为主,页岩气的资源潜力可能大于常规天然气。下列有关页岩气的叙述错误的是_______(填序号)。
| A.页岩气属于新能源 |
| B.页岩气和氧气的反应是放热反应 |
| C.甲烷中每个原子的最外层电子排布都达到8电子稳定结构 |
| D.页岩气可以作燃料电池的负极燃料 |
| 电池装置 | 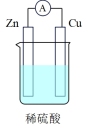 | 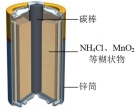 | 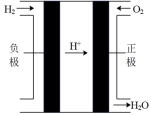 | 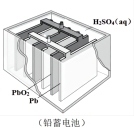 |
| 编号 | a | b | c | d |
①上述四种电池中,属于二次电池的是
②a装置中,外电路中电子的流向是
③c装置中,若电解质改为碱性介质,则负极的电极反应式为
(3)氧化还原反应一般可以设计成原电池。若将反应
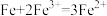 设计成原电池,则:
设计成原电池,则:①该电池的电解质溶液可以是
②当外电路中转移1mol e-时,电解质溶液增加的质量是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】某学习小组用如图所示A、B装置分别探究金属锌与稀硫酸的反应,实验过程中A装置烧杯内的溶液温度升高,B装置的电流计指针发生偏转。
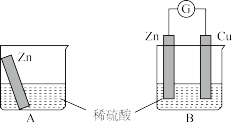
(1)装置B烧杯中发生反应的离子方程式为_______ 。
(2)B装置中锌做_______ 极, 铜做_______ 极 (填“正”或“负”)。电子由_______ 极流向_______ 极 (填“Zn”或“Cu”)
(3)Cu板上的现象是_______ ,发生的电极反应是_______ 。
(4)该小组同学反思原电池的原理,其中观点正确的是_______(填字母)。

(1)装置B烧杯中发生反应的离子方程式为
(2)B装置中锌做
(3)Cu板上的现象是
(4)该小组同学反思原电池的原理,其中观点正确的是_______(填字母)。
| A.原电池反应的过程中可能没有电子发生转移 |
| B.原电池装置需要2个电极 |
| C.电极一定不能参加反应 |
| D.氧化反应和还原反应可以拆开在两极发生 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】研究化学反应中能量的转化,对于社会发展、科技进步具有重要意义。
(1)一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,如Zn+2H+=Zn2++H2↑,可拆写为氧化反应式:Zn-2e-=Zn2+,还原反应式:2H++2e-=H2。并由此实现了化学能与电能的相互转化。甲图所示原电池中:
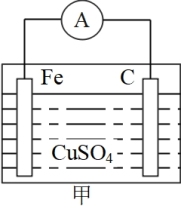
①C电极为____ 极(填“正”或“负”)。
②发生还原反应的半反应式为____ 。
③证明化学能转化为电能的实验现象是____ 。
(2)某同学根据化学反应:Cu+2FeCl3=CuCl2+2FeCl2设计的原电池实验装置如乙图,若电子从b流向a,则:
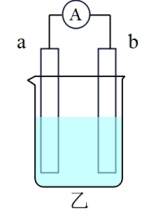
①b的电极材料为____ 。
②电解质溶液是____ 。
③a电极反应式为____ 。
(1)一个完整的氧化还原反应方程式可以拆写成两个“半反应式”,如Zn+2H+=Zn2++H2↑,可拆写为氧化反应式:Zn-2e-=Zn2+,还原反应式:2H++2e-=H2。并由此实现了化学能与电能的相互转化。甲图所示原电池中:

①C电极为
②发生还原反应的半反应式为
③证明化学能转化为电能的实验现象是
(2)某同学根据化学反应:Cu+2FeCl3=CuCl2+2FeCl2设计的原电池实验装置如乙图,若电子从b流向a,则:

①b的电极材料为
②电解质溶液是
③a电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】燃料电池在日常生活和科学研究中越来越得到广泛使用。镁-空气燃料电池是一种新型的燃料电池,可应用于电动汽车,其工作原理如图所示:
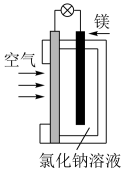
回答下列问题:
(1)通入空气的电极是______ (填“正”或“负”)极。
(2)镁电极发生______ (填“氧化”或“还原”)反应。
(3)电池总反应方程式为______ 。

回答下列问题:
(1)通入空气的电极是
(2)镁电极发生
(3)电池总反应方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】能源与材料、信息一起被称为现代社会发展的三大支柱。面对能源枯竭的危机,提高能源利用率和开辟新能源是解决这一问题的两个主要方向。
(1)化学反应速率和限度与生产、生活密切相关,这是化学学科关注的方面之一。某同学为了探究锌与盐酸反应过程中的速率变化,在 400mL 稀盐酸中加入足量 的锌粉,用排水法收集反应放出的氢气,实验记录如下(累计值):
①哪一段时间内反应速率最大:____ min(填“0~1”或“1~2”或“2~3”或“3~4” 或“4~5”)。
②另一学生为控制反应速率防止反应过快难以测量氢气体积。他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量。你认为可行的是____ (填字母序号)。
A.KCl 溶液 B.浓盐酸 C.蒸馏水 D.CuSO4 溶液
(2)如图为原电池装置示意图:
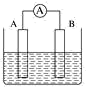
①若 A 为铝,B 为镁,电解质为稀硫酸溶液,则负极材料是_______ (填“铝片”或“镁片”)。
②若A为Cu,B 为石墨,电解质为 FeCl3 溶液,工作时的总反应为 2FeCl3+Cu=2FeCl2+CuCl2。写出铜电极的电极反应式:____ ;若该电池反应消耗了 0.1mol FeCl3, 则转移电子的数目为 _____ 。
(1)化学反应速率和限度与生产、生活密切相关,这是化学学科关注的方面之一。某同学为了探究锌与盐酸反应过程中的速率变化,在 400mL 稀盐酸中加入
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL(标况) | 100 | 240 | 464 | 576 | 620 |
①哪一段时间内反应速率最大:
②另一学生为控制反应速率防止反应过快难以测量氢气体积。他事先在盐酸中加入等体积的下列溶液以减慢反应速率但不影响生成氢气的量。你认为可行的是
A.KCl 溶液 B.浓盐酸 C.蒸馏水 D.CuSO4 溶液
(2)如图为原电池装置示意图:

①若 A 为铝,B 为镁,电解质为稀硫酸溶液,则负极材料是
②若A为Cu,B 为石墨,电解质为 FeCl3 溶液,工作时的总反应为 2FeCl3+Cu=2FeCl2+CuCl2。写出铜电极的电极反应式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】课外小组的同学对下图所示的实验装置进行了研究。
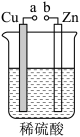
(1)a和b不连接时,烧杯中发生反应的离子方程式是_______ ,反应中的氧化剂是_______ 。
(2)将a和b用导线连接。
①Cu电极上的现象是________ 。
②Zn电极为原电池的_______ 极(填“正”或“负”),该电极反应式是________ 。

(1)a和b不连接时,烧杯中发生反应的离子方程式是
(2)将a和b用导线连接。
①Cu电极上的现象是
②Zn电极为原电池的
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】I.原电池是化学电源的雏形。
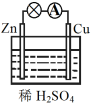
(1)如图连接好装置后,负极材料是_______ (填“Zn”或“Cu”)。
(2)相应原电池的总反应方程式为_______ 。
(3)下列化学反应可通过原电池装置,实现化学能直接转化为电能的是_______ (填序号)。
①2NaOH+H2SO4=Na2SO4 +2H2O ②Cu+2Fe 3+=Cu2++2Fe2+ ③C2H5OH+3O2 2CO2 +3H2O
2CO2 +3H2O
II.根据原电池原理,结合装置图,按要求解答问题:

(4)若X为Zn,Y为硫酸铜溶液,溶液中的Cu2+移向_______ (填“Cu”或“X”)电极。
(5)若X为银,Y为硝酸银溶液,则X的电极方程式_______
(6)若X为Fe,Y为浓硝酸,则Cu电极电极方程式是_______ 。

(1)如图连接好装置后,负极材料是
(2)相应原电池的总反应方程式为
(3)下列化学反应可通过原电池装置,实现化学能直接转化为电能的是
①2NaOH+H2SO4=Na2SO4 +2H2O ②Cu+2Fe 3+=Cu2++2Fe2+ ③C2H5OH+3O2
 2CO2 +3H2O
2CO2 +3H2OII.根据原电池原理,结合装置图,按要求解答问题:

(4)若X为Zn,Y为硫酸铜溶液,溶液中的Cu2+移向
(5)若X为银,Y为硝酸银溶液,则X的电极方程式
(6)若X为Fe,Y为浓硝酸,则Cu电极电极方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】电子表和电子计算器的电池常用微型银—锌原电池,其电极分别为Zn和Ag2O,电解质溶液为KOH溶液,负极反应和总反应分别为:Zn+2OH - -2e==ZnO+H2O和Ag2O+Zn==ZnO+2Ag
(1)该原电池工作时负极区溶液的PH值_________ (上升、下降或不变)
(2)该原电池工作时电子由____ (Zn或Ag2O)极经外电路流向_______ (正或负)极。正极上发生的电极反应为__________________________________________________
(1)该原电池工作时负极区溶液的PH值
(2)该原电池工作时电子由
您最近一年使用:0次



