科研人员设想用如图所示装置生产硫酸,下列说法不正确的是
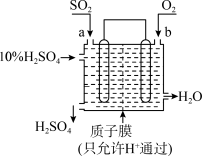

| A.a为负极,b为正极 |
| B.生产过程中氢离子由左移向右 |
| C.从左下口流出的硫酸的质量分数一定大于10% |
| D.正极反应式为O2+2H2O+4e-===4OH- |
更新时间:2019-06-01 23:11:57
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
| A.用含有少量硫酸铜的稀硫酸跟锌粒反应,能加快产生氢气,说明Cu2+具有催化能力 |
| B.增大浓度会加快化学反应速率,是因为增加了反应物单位体积内活化分子的百分数 |
| C.等体积、pH都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性:HA<HB |
| D.碱性锌锰电池是一种常见的二次电池 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关电化学的说法正确的是
| A.铜的金属活泼性比铁弱,可在海轮外壳上镶入若干铜块以减缓铁腐蚀 |
| B.原电池中,一定由活泼性强的金属作负极,发生氧化反应 |
| C.原电池放电时的负极和电解池充电时的阴极均发生氧化反应 |
| D.可充电电池充电时,负极与电源负极相连,正极与电源正极相连 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列对有关实验现象的描述或解释不正确的是
| 编号 | 事实 | 解释 |
| ① | 锌与稀盐酸反应,加入氯化钠固体,速率加快 | 增大了氯离子浓度,反应速率加快 |
| ② | 锌与稀硫酸反应,滴入几滴硫酸铜溶液,生成氢气的速率减慢 | 锌置换铜的反应干扰了锌置换氢的反应,致使生成氢气的速率变慢 |
| ③ | 大小、形状相同的镁片、铁片,与等浓度的盐酸反应产生H2的速率前者比后者大 | 镁比铁活泼,化学反应速率的决定性因素是反应物本身的性质 |
| ④ | 等浓度等体积的FeCl3和KI溶液混合反应: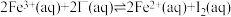 ,达到平衡后滴加KSCN溶液,出现血红色 ,达到平衡后滴加KSCN溶液,出现血红色 | 该反应为可逆反应,体系中始终存在Fe3+ |
| ⑤ | 铜与稀硫酸反应较慢,加热后,立即产生气泡 | 升高温度,反应速率加快 |
| ⑥ | 面粉生产车间容易发生爆炸 | 固体表面积大,反应速率加快 |
| A.①②④ | B.①④⑤ | C.①②⑤ | D.②④⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】有学者提出可利用铝-空气电池装置来净化水体(净水原理与明矾类似),其基本工作原理如图所示,正负极区的电解质溶液为酸化的NaCl溶液。下列说法正确的是
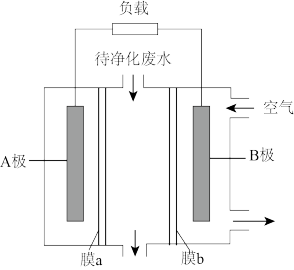

| A.膜a为阳离子交换膜 |
| B.电子流向:A电极→电解质溶液→B电极 |
| C.正极区溶液的pH降低、负极区溶液的pH升高 |
| D.将电解质溶液换成碱性的NaCl溶液可提升净水效果 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】肼(N2H4)和氧气以及KOH溶液可组成碱性燃料电池,产物为氮气和水,它是一种高效低污染的新型电池。下列关于肼燃料电池的说法不正确的是( )
| A.负极反应式为:N2H4+4OH--4e-=N2+4H2O |
| B.O2在正极发生还原反应 |
| C.电解质溶液中的OH-向正极移动 |
| D.随着放电的进行,溶液的pH减小 |
您最近一年使用:0次




