下表为元素周期表的一部分,列出10种元素在周期表中的位置。用化学符号回答下列问题:
(1)10种元素中,化学性质最活泼的金属是(填元素符号)________ 。
(2)④、⑤、⑥两种元素最高价氧化物对应的水化物中,碱性最强的是(填化学式)________ 。
(3)③、④两种元素形成的离子,离子半径由大到小的顺序是(用离子符号表示)________ 。
(4)④和⑨两种元素形成化合物与元素⑧的单质反应的离子方程式为________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑩ | ⑨ |
(2)④、⑤、⑥两种元素最高价氧化物对应的水化物中,碱性最强的是(填化学式)
(3)③、④两种元素形成的离子,离子半径由大到小的顺序是(用离子符号表示)
(4)④和⑨两种元素形成化合物与元素⑧的单质反应的离子方程式为
更新时间:2019-06-11 14:58:37
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】元素周期表前四周期W、X、Y、Z、E五种元素,W元素的原子最外层电子排布式为 ;X元素的原子价电子排布式为
;X元素的原子价电子排布式为 ;Y元素位于第二周期且原子中p能级与s能级电子总数相等;Z元素原子的M能层的p能级中有3个未成对电子;
;Y元素位于第二周期且原子中p能级与s能级电子总数相等;Z元素原子的M能层的p能级中有3个未成对电子; 中有5个未成对电子。
中有5个未成对电子。
(1)写出元素名称:Z___________ ;E___________ 。
(2)Y基态原子的电子排布图为___________ 。
(3)当 时,
时, 分子中,两共价键的键角为
分子中,两共价键的键角为___________ 度;当 时,X与Y形成的化合物与氢氧化钠溶液反应的离子方程式是
时,X与Y形成的化合物与氢氧化钠溶液反应的离子方程式是___________ 。
(4)E元素原子的价电子排布式是___________ ,在元素周期表中的位置是___________ ,按照核外电子排布,可以把元素周期表分为5个区,E元素位于周期表的___________ 区。
 ;X元素的原子价电子排布式为
;X元素的原子价电子排布式为 ;Y元素位于第二周期且原子中p能级与s能级电子总数相等;Z元素原子的M能层的p能级中有3个未成对电子;
;Y元素位于第二周期且原子中p能级与s能级电子总数相等;Z元素原子的M能层的p能级中有3个未成对电子; 中有5个未成对电子。
中有5个未成对电子。(1)写出元素名称:Z
(2)Y基态原子的电子排布图为
(3)当
 时,
时, 分子中,两共价键的键角为
分子中,两共价键的键角为 时,X与Y形成的化合物与氢氧化钠溶液反应的离子方程式是
时,X与Y形成的化合物与氢氧化钠溶液反应的离子方程式是(4)E元素原子的价电子排布式是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】某研究小组为了探究一种无机矿物盐X(仅含四种元素)的组成和性质,设计并完成如下实验:
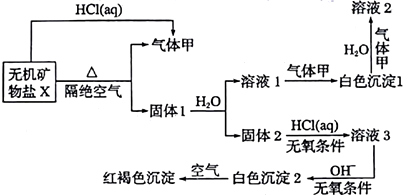
另取21.6gX在惰性气流中加热至完全分解,得到12.8g固体1和0.2mol气体甲。
(1)画出白色沉淀1中金属元素的原子结构示意图_____________ ,写出气体甲的电子式_______ 。
(2)X的化学式是______________ ,在惰性气流中加热X至完全分解的化学反应方程式为______________________________________ 。
(3)白色沉淀2在空气中变成红褐色沉淀的原因是_______ (用化学反应方程式表示)。
(4)一定条件下,气体甲鱼固体1中的某种成分可能发生氧化还原反应,写出一个有气体生成的可能的化学反应方程式______________________________ ,并设计实验方案验证该反应的产物___________________________________________ 。

另取21.6gX在惰性气流中加热至完全分解,得到12.8g固体1和0.2mol气体甲。
(1)画出白色沉淀1中金属元素的原子结构示意图
(2)X的化学式是
(3)白色沉淀2在空气中变成红褐色沉淀的原因是
(4)一定条件下,气体甲鱼固体1中的某种成分可能发生氧化还原反应,写出一个有气体生成的可能的化学反应方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐3】已知五种元素的原子序数的大小顺序为 C> A> B >D >E,A、C同周期,B、C同主族。A与B形成的离子化合物A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10电子的分子。试回答下列问题:
(1)写出以下元素的名称 A_________ C_________
(2)B元素在元素周期表中的位置是_______________ ;D2分子的结构式是______________ 。
(3)实验室制取D的氢化物的化学反应方程式为_________________________ 。
(4)用电子式表示化合物A2B的形成过程______________________ 。
(5)M、N均由A、B、C、E四种元素组成,写出此两种化合物在水溶液中发生反应的离子方程式____________________________ 。
(1)写出以下元素的名称 A
(2)B元素在元素周期表中的位置是
(3)实验室制取D的氢化物的化学反应方程式为
(4)用电子式表示化合物A2B的形成过程
(5)M、N均由A、B、C、E四种元素组成,写出此两种化合物在水溶液中发生反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐1】下图是部分短周期元素的常见化合价与原子序数的关系:
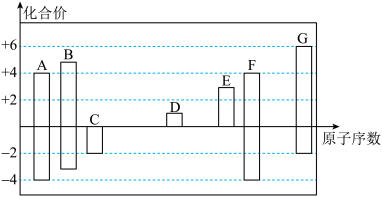
(1)元素A在周期表中的位置____________ 。C2﹣、D+、G2﹣离子半径大小顺序是____________ (填离子符号)。
(2)用电子式表示D2G的形成过程________________________ 。
(3)C、G的氢化物中沸点较低的是____________ (填化学式)。
(4)C与D形成的具有强氧化性的化合物的电子式为____________ 。

(1)元素A在周期表中的位置
(2)用电子式表示D2G的形成过程
(3)C、G的氢化物中沸点较低的是
(4)C与D形成的具有强氧化性的化合物的电子式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】如表所示为元素周期表的一部分,参照元素①~⑨在表中的位置,请回答下列问题:
(1)周期表中元素最高正价与最低价代数和为零的是______________ 族(用族序号表示)。
(2)⑥和⑦的最高价含氧酸的酸性强弱为_______________ (用酸的化学式表示)。
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式______________________ ;
(4)已知周期表中存在对角相似规则,如铍(Be)与铝化学性质相似,⑧的氧化物、氢氧化物也有两性,写出⑧的氢氧化物与④的最高价氧化物的水化物反应的化学方程式__________________ 。
(5)已知W+X=Y+Z(反应需要加热,),W、X、Y、Z分别是由①②⑨三种元素形成的四种十电子粒子(W、X为离子,Y、Z为分子),写出该化学方程式_______________________ 。
(6)由表中元素形成的物质可发生如图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。
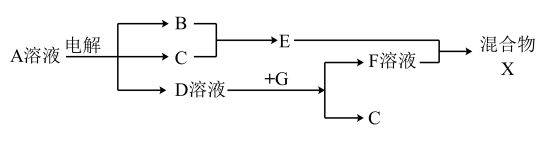
①写出D溶液与G反应的化学方程式_______________________ 。
②写出检验A溶液中溶质的阴离子的方法___________________________ 。
(1)周期表中元素最高正价与最低价代数和为零的是
(2)⑥和⑦的最高价含氧酸的酸性强弱为
(3)①、②两种元素按原子个数之比为1:1组成的常见液态化合物,在酸性溶液中能将Fe2+氧化,写出该反应的离子方程式
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ⑧ | ⑨ | ② | ③ | ||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ||||
(5)已知W+X=Y+Z(反应需要加热,),W、X、Y、Z分别是由①②⑨三种元素形成的四种十电子粒子(W、X为离子,Y、Z为分子),写出该化学方程式
(6)由表中元素形成的物质可发生如图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。

①写出D溶液与G反应的化学方程式
②写出检验A溶液中溶质的阴离子的方法
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的离子不含电子;B元素的最高价氧化物对应水化物与其氢化物能反应生成盐F;D与A同主族,且与 E同周期;E元素原子的最外层电子数是其次外层电子数的 3/4,A、B、D、E这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物。请回答下列问题:
(1)E元素在元素周期表中的位置是_______________ 。
(2)由A、B、C三种元素形成的离子化合物的化学式为_________________ 。
(3)A可分别与C、E形成甲、乙两种三原子分子,且甲有18个电子、乙有10个电子,甲与乙比较,沸点较高的是(填化学式)_______________ 。
(4)F含有的化学键类型是___________ 和_____________ ,其水溶液呈酸性,请用相关的离子方程式解释其原因___________ 。
(5)D和C形成的一种化合物能与A和C形成的一种化合物反应产生C单质,该过程的化学方程式为______ 。
(1)E元素在元素周期表中的位置是
(2)由A、B、C三种元素形成的离子化合物的化学式为
(3)A可分别与C、E形成甲、乙两种三原子分子,且甲有18个电子、乙有10个电子,甲与乙比较,沸点较高的是(填化学式)
(4)F含有的化学键类型是
(5)D和C形成的一种化合物能与A和C形成的一种化合物反应产生C单质,该过程的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】表中所列字母分别代表一种元素。
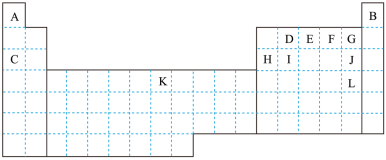
(1)G的气态氢化物比J的气态氢化物_______ (填“稳定”或“不稳定”)。
(2)在一定条件下,A与E可形成一种极易溶于水的气态化合物,其电子式为_______ ;该物质溶于水后的溶液呈_______ 性(填“酸”、“碱”或“中”)。
(3)元素C和H的最高价氧化物对应的水化物相互反应的离子方程式为:_______ 。
(4)元素G和L的原子序数相差:_______ ,它们的氢化物的水溶液酸性相对强的是:_______ (填化学式)
(5)表中A和F两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为:_______
(6)K为生产、生活中应用最广泛的金属,通常采用的冶炼方法为:_______

(1)G的气态氢化物比J的气态氢化物
(2)在一定条件下,A与E可形成一种极易溶于水的气态化合物,其电子式为
(3)元素C和H的最高价氧化物对应的水化物相互反应的离子方程式为:
(4)元素G和L的原子序数相差:
(5)表中A和F两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为:_______
| A.MnO2 | B.Na2SO4 | C.FeCl3 | D.KMnO4 |
| A.电解法 | B.热分解法 | C.热还原法 |
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】A、B、C、D、E是位于短周期的主族元素.已知:①热稳定性:HmD>HmC;
②Cm﹣、E(m﹣1)﹣具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍.依据上述信息用相应的化学用语回答下列问题:
(1)HmDm的电子式_____ .
(2)能证明Cm﹣、E(m﹣1)﹣的还原性强弱的离子方程式为____________ .
(3)将E的单质通入A与D形成的化合物的水溶液中,其离子方程式为:___________ .常温下,将等物质的量浓度的HmC溶液和A的最高价氧化物对应的水化物溶液等体积混合,写出该反应的离子方程式________________________ .
②Cm﹣、E(m﹣1)﹣具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍.依据上述信息用相应的化学用语回答下列问题:
(1)HmDm的电子式
(2)能证明Cm﹣、E(m﹣1)﹣的还原性强弱的离子方程式为
(3)将E的单质通入A与D形成的化合物的水溶液中,其离子方程式为:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E三种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出元素的名称:C__________ ,D___________ 。
(2)写出元素的原子结构示意图:A______________ ,B______________ ,
二者离子半径:_______ >_________ (填化学式,下同)。
(3)A、B的最高价氧化物的水化物的碱性:______________ >______________ 。
(4)D、E的气态氢化物的稳定性:______________ >______________ 。
(1)写出元素的名称:C
(2)写出元素的原子结构示意图:A
二者离子半径:
(3)A、B的最高价氧化物的水化物的碱性:
(4)D、E的气态氢化物的稳定性:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】现有10种元素的性质、数据如下表所列,它们均为短周期元素.
回答下列问题:
(1)D的元素名称是_______ ,H的元素符号是_______ ,B在元素周期表中的位置是(周期、族)_______ 。
(2)在以上元素形成的最高价氧化物的水化物中,酸性最强的化合物的分子式是_______ .化合物F2A2的电子式是:_______ ,构成该物质的化学键类型为_______ 。
(3)用电子式表示A的简单氢化物的形成过程如下:_______ ;G的氢化物的结构式为_______ 。
(4)一定条件下,IA2气体与足量的A单质充分反应生成20 g气态化合物,放出24.6 kJ热量,写出其热化学方程式_______ 。
(5)用J元素的单质与A元素的单质可以制成电池,电池中装有KOH浓溶液,用多孔的惰性电极甲和乙浸入KOH溶液,在甲极通入J的单质,乙极通入A的单质,则甲极的电极反应式为:_______ 。
| A | B | C | D | E | F | G | H | I | J | |
| 原子半径(10﹣10m) | 0.74 | 1.60 | 1.52 | 1.10[ | 0.99 | 1.86 | 0.75 | 0.82 | 0.102 | 0.037 |
| 最高或最低 化合价 | +2 | +1 | +5[ | +7 | +1 | +5 | +3 | +6 | +1 | |
| ﹣2 | ﹣3 | ﹣1 | ﹣3 | ﹣2 |
(1)D的元素名称是
(2)在以上元素形成的最高价氧化物的水化物中,酸性最强的化合物的分子式是
(3)用电子式表示A的简单氢化物的形成过程如下:
(4)一定条件下,IA2气体与足量的A单质充分反应生成20 g气态化合物,放出24.6 kJ热量,写出其热化学方程式
(5)用J元素的单质与A元素的单质可以制成电池,电池中装有KOH浓溶液,用多孔的惰性电极甲和乙浸入KOH溶液,在甲极通入J的单质,乙极通入A的单质,则甲极的电极反应式为:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】下表是元素剧期表的一部分,请根据要求填空

(1) 元素②最外层有_____ 个电子,在化合物中的最低负化合价为________ ;
(2) 元素⑤形成的离子的结构示意图为_________ ;
(3) 用电子式表示元素①和⑦组成的化合物的形成过程:_______________ ;
(4) 元素④、⑤的最高价氧化物的水化物之间发生反应的离子方程式_______ 。
(5) 下列选项中能证明元素⑦的非金属性强于元素⑥的是________ (双选)。
A.H2S的酸性弱于HCl B.S2-的还原性强于C1-
C.H2SO3的酸性强于HClO D.H2S不如HCl稳定

(1) 元素②最外层有
(2) 元素⑤形成的离子的结构示意图为
(3) 用电子式表示元素①和⑦组成的化合物的形成过程:
(4) 元素④、⑤的最高价氧化物的水化物之间发生反应的离子方程式
(5) 下列选项中能证明元素⑦的非金属性强于元素⑥的是
A.H2S的酸性弱于HCl B.S2-的还原性强于C1-
C.H2SO3的酸性强于HClO D.H2S不如HCl稳定
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐3】完成下列小题
(1)现有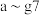 种短周期元素,它们在周期表中的位置如图,请据此回答下列问题:
种短周期元素,它们在周期表中的位置如图,请据此回答下列问题:
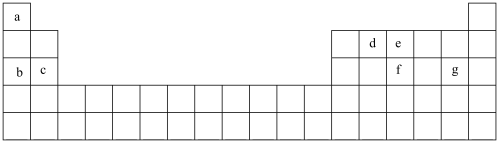
①元素 和f在周期表中的位置
和f在周期表中的位置_____ ,_____ 。
②用电子式表示由 与
与 元素组成化合物的形成过程:
元素组成化合物的形成过程:_____ 。
③元素的原子间反应最容易形成离子键的是_____ 。
A.c和f B.b和g C.d和g D.b和
④ 与
与 元素形成的分子中所有原子
元素形成的分子中所有原子_____ (填“是”或“不是”)都满足最外层为8电子结构
(2) 和
和 代表原子序数依次增大的四种短周期元素,它们满足以下条件:
代表原子序数依次增大的四种短周期元素,它们满足以下条件:
①元素周期表中, 与
与 相邻,
相邻, 与
与 也相邻;②
也相邻;② 、
、 和
和 三种元素的原子最外层电子数之和为17.请填空:
三种元素的原子最外层电子数之和为17.请填空:
①下列元素的符号:
_____ 、
_____ 、
_____ 。
② 和
和 可组成一化合物,其原子个数之比为
可组成一化合物,其原子个数之比为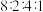 。写出该化合物的化学式
。写出该化合物的化学式_____ 。
(1)现有
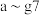 种短周期元素,它们在周期表中的位置如图,请据此回答下列问题:
种短周期元素,它们在周期表中的位置如图,请据此回答下列问题:
①元素
 和f在周期表中的位置
和f在周期表中的位置②用电子式表示由
 与
与 元素组成化合物的形成过程:
元素组成化合物的形成过程:③元素的原子间反应最容易形成离子键的是
A.c和f B.b和g C.d和g D.b和

④
 与
与 元素形成的分子中所有原子
元素形成的分子中所有原子(2)
 和
和 代表原子序数依次增大的四种短周期元素,它们满足以下条件:
代表原子序数依次增大的四种短周期元素,它们满足以下条件:①元素周期表中,
 与
与 相邻,
相邻, 与
与 也相邻;②
也相邻;② 、
、 和
和 三种元素的原子最外层电子数之和为17.请填空:
三种元素的原子最外层电子数之和为17.请填空:①下列元素的符号:



②
 和
和 可组成一化合物,其原子个数之比为
可组成一化合物,其原子个数之比为 。写出该化合物的化学式
。写出该化合物的化学式
您最近一年使用:0次



