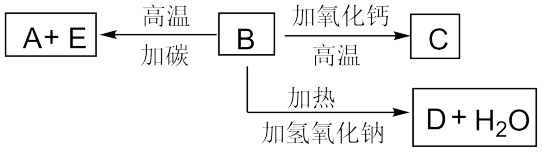
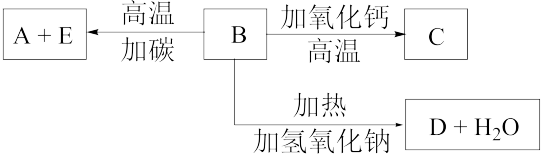
已知A,B,C,D均含有同一种元素,A为单质,根据下图所示的物质之间的转化关系,回答下列有关问题。
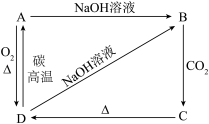
①写出A、B、C、D各物质的名称:A________ ,B________ ,C________ ,D_______ ;
②写出A→D的化学方程式:_______________ 。
③写出下列变化的离子方程式:
B→C______________________________ ;
D→B______________________________ 。

①写出A、B、C、D各物质的名称:A
②写出A→D的化学方程式:
③写出下列变化的离子方程式:
B→C
D→B
18-19高一·福建·单元测试 查看更多[2]
更新时间:2019/06/13 16:08:38
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】物质之间的变化体现了化学之美。
(1)一定条件下,含氮元素的物质可发生如图所示的循环转化。
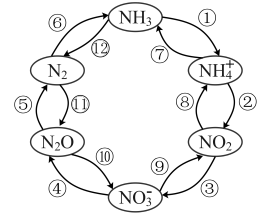
Ⅰ.图中属于“氮的固定”的是_______ (填序号,下同);转化过程中发生非氧化还原反应的是_______________ 。
Ⅱ.反应④是在酸性条件下由NO3-与镁作用实现,则该反应的离子方程式为_______ 。
(2)H2S气体与CuCl2、FeCl3溶液发生一系列反应如图所示:
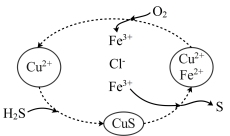
①转化图中化合价不变的元素是__________ (写名称)。
②转化图中生成S单质的离子方程式为____________ 。
(3)A、B、C、D、E、F、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。
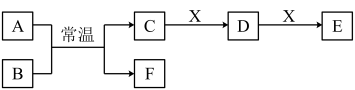
①若A为常见的金属单质,焰色反应呈黄色,B常温下为液态,X能使品红溶液褪色,则C和E反应的离子方程式为________ 。
②若D为两性氢氧化物,F为非金属单质,则X成分可能为____ (写化学式,下同)。
③若A为红棕色气体,X为金属单质,溶液D中加入KSCN溶液变红。则E为______ ,F为______ 。
(1)一定条件下,含氮元素的物质可发生如图所示的循环转化。

Ⅰ.图中属于“氮的固定”的是
Ⅱ.反应④是在酸性条件下由NO3-与镁作用实现,则该反应的离子方程式为
(2)H2S气体与CuCl2、FeCl3溶液发生一系列反应如图所示:

①转化图中化合价不变的元素是
②转化图中生成S单质的离子方程式为
(3)A、B、C、D、E、F、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去)。

①若A为常见的金属单质,焰色反应呈黄色,B常温下为液态,X能使品红溶液褪色,则C和E反应的离子方程式为
②若D为两性氢氧化物,F为非金属单质,则X成分可能为
③若A为红棕色气体,X为金属单质,溶液D中加入KSCN溶液变红。则E为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】有关物质的转化关系如下图所示。常温下,B、E 为气态,分别呈黄绿色、无色,且 E 常 用作制冷剂。D 是最常见的无色液体,F 是一种不溶于水的碱,G 是厨房中的常见调味品,H 为硝酸盐, 其摩尔质量为 80 g·mol-1。

(1)F、H 的化学式分别为___ 、___ 。
(2)请设计检验 A 中阳离子的实验方案:___ 。
(3)写出反应①的离子方程式:___ 。
(4)写出反应②的化学方程式,并标出电子转移的数目和方向:___ 。

(1)F、H 的化学式分别为
(2)请设计检验 A 中阳离子的实验方案:
(3)写出反应①的离子方程式:
(4)写出反应②的化学方程式,并标出电子转移的数目和方向:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如图所示(反应条件及其他物质已经略去):

(1)若A是一种金属,C是淡黄色固体,写出C的一种用途____ ;
(2)若常温下A为淡黄色固体单质,D为强酸,则B为___ ,D的浓溶液能使胆矾晶体由蓝变白,体现了D的___ 性。
(3)若A是化合物,C是红棕色气体,则
①A的电子式为___ ,实验室制备A气体的化学方程式为___ 。
②实验室检验A气体的方法为___ 。
③C转化为D的过程中,氧化剂与还原剂的质量比为___ 。
④将盛满B气体的试管倒扣在水槽中,并通入一定量O2,最终气体全部被吸收,所得溶液充满整个试管。若不考虑溶液扩散,计算所得溶液物质的量浓度为___ mol·L-1。(标况下计算,保留两位有效数字)

(1)若A是一种金属,C是淡黄色固体,写出C的一种用途
(2)若常温下A为淡黄色固体单质,D为强酸,则B为
(3)若A是化合物,C是红棕色气体,则
①A的电子式为
②实验室检验A气体的方法为
③C转化为D的过程中,氧化剂与还原剂的质量比为
④将盛满B气体的试管倒扣在水槽中,并通入一定量O2,最终气体全部被吸收,所得溶液充满整个试管。若不考虑溶液扩散,计算所得溶液物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:①高温下用过量的碳还原二氧化硅制得粗硅;②粗硅与干燥的HCl气体反应制得SiHCl3(Si+3HCl=SiHCl3+H2)③SiHCl3与过量的H2在1000℃~1100℃反应制得纯硅,已知SiHCl3能与水强烈反应,在空气中易自燃。
请回答:
(1)第一步制取硅的化学方程式___ 。
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl3(沸点33.0℃)中含有少量SiCl4(沸点57.6℃),提纯SiHCl3可采用___ 的方法。
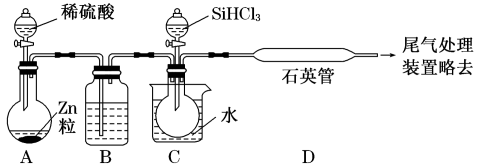
(3)实验室用SiHCl3与过量的H2反应制取纯硅装置如图所示(加热和夹持装置略去):
①装置B中的试剂是____ ,装置C需水浴加热,目的是___ 。
②反应一段时间后,装置D中可观察到有晶体硅生成,装置D不能采用普通玻璃管的原因是___ ,D中发生的反应的化学方程式是___ 。
③为保证实验的成功,操作的关键除题中已告知的之外,你认为最重要的还有:___ ,___ 。(答出两点)。
④为鉴定产品硅中是否含微量铁单质,将试样用稀盐酸溶解,取上层清液后需再加入的试剂(填写字母代号)是__ 。
a.碘水b.氯水c.NaOH溶液d.KSCN溶液e.Na2SO3溶液.

请回答:
(1)第一步制取硅的化学方程式
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl3(沸点33.0℃)中含有少量SiCl4(沸点57.6℃),提纯SiHCl3可采用
(3)实验室用SiHCl3与过量的H2反应制取纯硅装置如图所示(加热和夹持装置略去):
①装置B中的试剂是
②反应一段时间后,装置D中可观察到有晶体硅生成,装置D不能采用普通玻璃管的原因是
③为保证实验的成功,操作的关键除题中已告知的之外,你认为最重要的还有:
④为鉴定产品硅中是否含微量铁单质,将试样用稀盐酸溶解,取上层清液后需再加入的试剂(填写字母代号)是
a.碘水b.氯水c.NaOH溶液d.KSCN溶液e.Na2SO3溶液.
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】太阳能光伏产业蓬勃发展,推动了高纯硅的生产和应用。工业上以硅石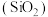 为原料制备高纯硅的工业流程如图所示。
为原料制备高纯硅的工业流程如图所示。
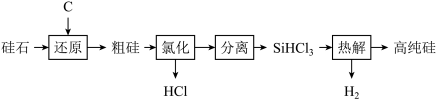
已知: 是常温下易挥发、遇水迅速生成其他物质的无色液体。
是常温下易挥发、遇水迅速生成其他物质的无色液体。
(1)Si在元素周期表中的位置是_______ 。
(2)“还原”需在高温条件下进行,该反应的化学方程式是_______ 。
(3)“氯化”时的还原产物是_______ (填化学式)。
(4)“氯化”、“分离”和“热解”的过程必须在无水、无氧条件下进行,理由是_______ 。
(5)该流程中能循环利用的物质是_______ (填两种)。
(6)高纯硅中常含有微量杂质,比如铁,对其进行测定的方法如下。
准确称取0.300g高纯硅样品用氢氟酸和稀硝酸溶解处理,配成100mL溶液,用羟胺 ,难电离)将
,难电离)将 还原为
还原为 后,加入邻菲啰啉形成橘红色络合物,再利用吸光度法测得吸光度为0.5(吸光度与
后,加入邻菲啰啉形成橘红色络合物,再利用吸光度法测得吸光度为0.5(吸光度与 浓度的对应关系如图)。
浓度的对应关系如图)。

①氢氟酸不能用玻璃试剂瓶保存的原因是_______ 。
②酸性条件下,羟胺与 反应生成无污染气体的反应的离子方程式为
反应生成无污染气体的反应的离子方程式为_______ 。
③高纯硅样品中铁的质量为_______ 。
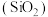 为原料制备高纯硅的工业流程如图所示。
为原料制备高纯硅的工业流程如图所示。
已知:
 是常温下易挥发、遇水迅速生成其他物质的无色液体。
是常温下易挥发、遇水迅速生成其他物质的无色液体。(1)Si在元素周期表中的位置是
(2)“还原”需在高温条件下进行,该反应的化学方程式是
(3)“氯化”时的还原产物是
(4)“氯化”、“分离”和“热解”的过程必须在无水、无氧条件下进行,理由是
(5)该流程中能循环利用的物质是
(6)高纯硅中常含有微量杂质,比如铁,对其进行测定的方法如下。
准确称取0.300g高纯硅样品用氢氟酸和稀硝酸溶解处理,配成100mL溶液,用羟胺
 ,难电离)将
,难电离)将 还原为
还原为 后,加入邻菲啰啉形成橘红色络合物,再利用吸光度法测得吸光度为0.5(吸光度与
后,加入邻菲啰啉形成橘红色络合物,再利用吸光度法测得吸光度为0.5(吸光度与 浓度的对应关系如图)。
浓度的对应关系如图)。
①氢氟酸不能用玻璃试剂瓶保存的原因是
②酸性条件下,羟胺与
 反应生成无污染气体的反应的离子方程式为
反应生成无污染气体的反应的离子方程式为③高纯硅样品中铁的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】晶体硅是一种重要的非金属材料,有科学家认为硅是“21世纪的能源”、“未来的石油”。
(1)工业上生产纯硅的工艺流程如下:

石英砂的主要成分是 ,在制备粗硅时反应的氧化产物为
,在制备粗硅时反应的氧化产物为___________ (填化学式);在该反应中,若消耗了3.6 g  ,则转移电子的总数为
,则转移电子的总数为___________ (用 表示阿伏伽德罗常数的值)。
表示阿伏伽德罗常数的值)。
(2)某实验室利用 (沸点33.0℃)与过量
(沸点33.0℃)与过量 在1000℃~1100℃反应制得纯硅(灰黑色固体)。已知
在1000℃~1100℃反应制得纯硅(灰黑色固体)。已知 能与
能与 强烈反应,在空气中易自燃。装置如图所示(热源及夹持装置略去)。
强烈反应,在空气中易自燃。装置如图所示(热源及夹持装置略去)。
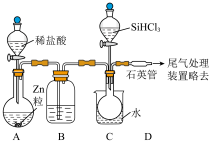
①装置B中的试剂是___________ 。装置C中水的作用是___________ 。
②反应一段时间后,装置D中观察到的现象是___________ ;装置D中发生反应的化学方程式为___________ 。
③为检验产品硅中是否含微量铁单质,将试样用稀盐酸溶解,取上层清液后需要加入的试剂有___________ (填字母)。
a. b.氯水 c.
b.氯水 c. 溶液 d.KSCN溶液
溶液 d.KSCN溶液
(1)工业上生产纯硅的工艺流程如下:

石英砂的主要成分是
 ,在制备粗硅时反应的氧化产物为
,在制备粗硅时反应的氧化产物为 ,则转移电子的总数为
,则转移电子的总数为 表示阿伏伽德罗常数的值)。
表示阿伏伽德罗常数的值)。(2)某实验室利用
 (沸点33.0℃)与过量
(沸点33.0℃)与过量 在1000℃~1100℃反应制得纯硅(灰黑色固体)。已知
在1000℃~1100℃反应制得纯硅(灰黑色固体)。已知 能与
能与 强烈反应,在空气中易自燃。装置如图所示(热源及夹持装置略去)。
强烈反应,在空气中易自燃。装置如图所示(热源及夹持装置略去)。
①装置B中的试剂是
②反应一段时间后,装置D中观察到的现象是
③为检验产品硅中是否含微量铁单质,将试样用稀盐酸溶解,取上层清液后需要加入的试剂有
a.
 b.氯水 c.
b.氯水 c. 溶液 d.KSCN溶液
溶液 d.KSCN溶液
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:_______ 。当有1molC参与反应时,该反应转移的电子数是________ 。
(2)还原炉中发生的化学反应方程式为:_______ 。
(3)上述工艺生产中循环使用的物质除Si、 外,还有
外,还有_______ 。
(4)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式:_______ 。
(5)关于硅及其相关化合物的叙述正确的是_____ 。
A.自然界中存在天然游离的硅单质
B.已知C与Si的最高正价都是正四价,由于 ,用类比法得知,
,用类比法得知,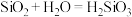
C.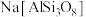 用氧化物形式表示为
用氧化物形式表示为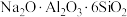
D. 既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
E.玻璃、水泥、陶瓷都是传统的硅酸盐产品
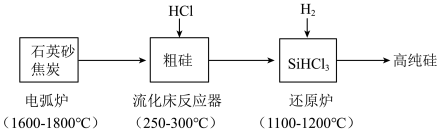
(2)还原炉中发生的化学反应方程式为:
(3)上述工艺生产中循环使用的物质除Si、
 外,还有
外,还有(4)工业上可利用水玻璃和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式:
(5)关于硅及其相关化合物的叙述正确的是
A.自然界中存在天然游离的硅单质
B.已知C与Si的最高正价都是正四价,由于
 ,用类比法得知,
,用类比法得知,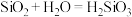
C.
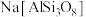 用氧化物形式表示为
用氧化物形式表示为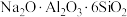
D.
 既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物
既能和NaOH溶液反应,又能和氢氟酸反应,所以是两性氧化物E.玻璃、水泥、陶瓷都是传统的硅酸盐产品
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的通常有两种工艺。因向铝土矿中加入NaOH时形成的赤泥(残渣)中常含有铝硅酸钠,故流程乙常处理SiO2含量小于8%的铝土矿,若SiO2含量较高则可采用流程甲来处理。

请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为_______ 。
(2)流程乙加入烧碱后生成SiO 的离子方程式为
的离子方程式为_______ 。
(3)流程甲滤液D中通入过量CO2的化学方程式为_______ 。
(4)“通入过量CO2”能否改用盐酸_______ ,原因是_______ 。
(5)滤液E、K中溶质的主要成分是_______ (填化学式),写出该溶质的一种用途_______ 。

请回答下列问题:
(1)流程甲加入盐酸后生成Al3+的离子方程式为
(2)流程乙加入烧碱后生成SiO
 的离子方程式为
的离子方程式为(3)流程甲滤液D中通入过量CO2的化学方程式为
(4)“通入过量CO2”能否改用盐酸
(5)滤液E、K中溶质的主要成分是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组利用下图装置探究 的性质,下图中a、b为弹簧夹,加热及固定装置略去。回答下列问题:
的性质,下图中a、b为弹簧夹,加热及固定装置略去。回答下列问题: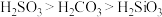 。
。
①仪器X名称_____________ ,写出Cu与浓硫酸反应的化学方程式__________________ 。
②装置A中试剂是_________ 。打开a,关闭b,滴入浓硫酸并加热。能说明酸性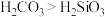 的实验现象是
的实验现象是___________________ 。
(2)验证 的相关性质。
的相关性质。
①打开b,关闭a,一段时间后,盛装 溶液装置中的现象是
溶液装置中的现象是___________ ,说明 具有
具有_______ 性。
②通入 的
的 溶液中无明显现象,现将其取出并分成两份。其中一份滴加氯水后出现了沉淀,说明
溶液中无明显现象,现将其取出并分成两份。其中一份滴加氯水后出现了沉淀,说明 具有
具有________ 性;另一份滴加氨水后也出现了沉淀,该沉淀的化学式为____________ 。
 的性质,下图中a、b为弹簧夹,加热及固定装置略去。回答下列问题:
的性质,下图中a、b为弹簧夹,加热及固定装置略去。回答下列问题:
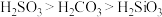 。
。①仪器X名称
②装置A中试剂是
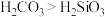 的实验现象是
的实验现象是(2)验证
 的相关性质。
的相关性质。①打开b,关闭a,一段时间后,盛装
 溶液装置中的现象是
溶液装置中的现象是 具有
具有②通入
 的
的 溶液中无明显现象,现将其取出并分成两份。其中一份滴加氯水后出现了沉淀,说明
溶液中无明显现象,现将其取出并分成两份。其中一份滴加氯水后出现了沉淀,说明 具有
具有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】 可用于制备铬颜料及铬盐,由铬铝矿渣(含57%的
可用于制备铬颜料及铬盐,由铬铝矿渣(含57%的 ,其余为
,其余为 和
和 )制备
)制备 的工艺流程如图所示。回答下列问题:
的工艺流程如图所示。回答下列问题:
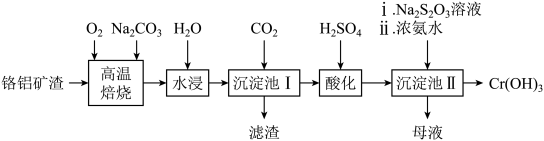
已知:①“高温焙烧”可以使矿渣转化为可溶性盐。
②酸性条件下, 能稳定存在。
能稳定存在。
(1)“高温焙烧”前需将铬铝矿渣进行球磨粉碎,目的是___________ 。“高温焙烧”时 最终生成
最终生成 ,当有7.6kg
,当有7.6kg 参与反应时,消耗
参与反应时,消耗 的体积为
的体积为___________  (标准状况),反应中
(标准状况),反应中 作
作___________ (填“还原剂”或“氧化剂”)。
(2)“滤渣”的主要成分为___________ (填化学式)。
(3)“酸化”时,含铬微粒发生反应的离子方程式为___________ 。
(4)“沉淀池Ⅱ”中加入 溶液的目的是
溶液的目的是___________ 。
(5)“母液”中溶质的主要成分除 外,还有
外,还有___________ (填化学式)。
(6)某工厂用10t该铬铝矿渣制备 ,若铬的损耗率为20%,最终可以得到
,若铬的损耗率为20%,最终可以得到 的质量为
的质量为___________ t。
 可用于制备铬颜料及铬盐,由铬铝矿渣(含57%的
可用于制备铬颜料及铬盐,由铬铝矿渣(含57%的 ,其余为
,其余为 和
和 )制备
)制备 的工艺流程如图所示。回答下列问题:
的工艺流程如图所示。回答下列问题:
已知:①“高温焙烧”可以使矿渣转化为可溶性盐。
②酸性条件下,
 能稳定存在。
能稳定存在。(1)“高温焙烧”前需将铬铝矿渣进行球磨粉碎,目的是
 最终生成
最终生成 ,当有7.6kg
,当有7.6kg 参与反应时,消耗
参与反应时,消耗 的体积为
的体积为 (标准状况),反应中
(标准状况),反应中 作
作(2)“滤渣”的主要成分为
(3)“酸化”时,含铬微粒发生反应的离子方程式为
(4)“沉淀池Ⅱ”中加入
 溶液的目的是
溶液的目的是(5)“母液”中溶质的主要成分除
 外,还有
外,还有(6)某工厂用10t该铬铝矿渣制备
 ,若铬的损耗率为20%,最终可以得到
,若铬的损耗率为20%,最终可以得到 的质量为
的质量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】Ⅰ.高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”。它可以按下列方法制备:

(1)写出步骤①的化学方程式:_________ 。
(2)步骤②经过冷凝得到的SiHCl3(沸点33.0 ℃)中含有少量的SiCl4(沸点57.6 ℃)和HCl(沸点-84.7 ℃),提纯SiHCl3的主要化学操作的名称是______ ;SiHCl3和SiCl4一样,遇水可发生剧烈水解,已知SiHCl3水解会生成两种气态产物,试写出其水解的化学方程式:________ 。
Ⅱ.白炭黑(SiO2·H2O)广泛应用于橡胶、涂料、印刷等行业,可用蛇纹石[主要成分为Mg6(Si4O10)(OH)8]来制取,其主要工艺流程如图所示:

(3)蛇纹石用氧化物形式可表示为_________________ 。
(4)碱浸时,为提高其中硅酸盐的浸取率,除采用合适的液固比和循环浸取外,还可采用的方法:①___________ ;②____________ (任举两种)。
(5)过滤1得到的滤液的主要成分是___________________ 。
(6)滤液与盐酸反应的主要离子方程式为________________ 。
(7)洗涤时,如何证明产品已洗涤干净?______________ 。

(1)写出步骤①的化学方程式:
(2)步骤②经过冷凝得到的SiHCl3(沸点33.0 ℃)中含有少量的SiCl4(沸点57.6 ℃)和HCl(沸点-84.7 ℃),提纯SiHCl3的主要化学操作的名称是
Ⅱ.白炭黑(SiO2·H2O)广泛应用于橡胶、涂料、印刷等行业,可用蛇纹石[主要成分为Mg6(Si4O10)(OH)8]来制取,其主要工艺流程如图所示:

(3)蛇纹石用氧化物形式可表示为
(4)碱浸时,为提高其中硅酸盐的浸取率,除采用合适的液固比和循环浸取外,还可采用的方法:①
(5)过滤1得到的滤液的主要成分是
(6)滤液与盐酸反应的主要离子方程式为
(7)洗涤时,如何证明产品已洗涤干净?
您最近一年使用:0次