下表列出了KNO3与NaCl在不同温度时的溶解度:
(1)现有含123 g KNO3与17.9 g NaCl的混合物,某同学设计了以下实验除去KNO3中的NaCl(不考虑水的额外损失)。
①向混合物中加入适量水,加热溶解;
②继续加热溶液至100 ℃并恒温蒸发浓缩;
③将溶液降温至10 ℃,仅得到KNO3晶体,过滤,将所得KNO3晶体洗涤并干燥。
A.在步骤②中,为确保没有晶体析出,溶液中至少要保留________ g水;
B.在步骤③中,最多可得到KNO3晶体________ g;
C.除去KNO3中少量NaCl的主要实验流程可用下图表示:
 ;
;____________
D.洗涤时,应选用少量________ (选填“热水”或“冷水”),其目的是____________ ,证明已经洗涤干净的方法是________ 。
(2)除去NaCl中少量KNO3的方法是:先将NaCl和KNO3混合物置于适量水中,加热搅拌保证固体能全部溶解,后蒸发溶液至有大量晶体析出时停止,再趁热过滤,并对过滤所得NaCl晶体进行洗涤和干燥。上述方法中,趁热过滤的目的是____________
(3)取23.4 g NaCl和40.4 g KNO3,加70 g水,加热溶解。在100 ℃时蒸发掉50 g水,维持该温度过滤,得到的晶体质量为________ g;将滤液冷却至10 ℃,充分结晶,写出析出晶体的化学式______________ 。
| 温度(℃) | 0 | 10 | 20 | 40 | 60 | 80 | 100 |
| KNO3的溶解度(g) | 13.3 | 20.9 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCl的溶解度(g) | 35.7 | 35.8 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
(1)现有含123 g KNO3与17.9 g NaCl的混合物,某同学设计了以下实验除去KNO3中的NaCl(不考虑水的额外损失)。
①向混合物中加入适量水,加热溶解;
②继续加热溶液至100 ℃并恒温蒸发浓缩;
③将溶液降温至10 ℃,仅得到KNO3晶体,过滤,将所得KNO3晶体洗涤并干燥。
A.在步骤②中,为确保没有晶体析出,溶液中至少要保留
B.在步骤③中,最多可得到KNO3晶体
C.除去KNO3中少量NaCl的主要实验流程可用下图表示:
 ;
;D.洗涤时,应选用少量
(2)除去NaCl中少量KNO3的方法是:先将NaCl和KNO3混合物置于适量水中,加热搅拌保证固体能全部溶解,后蒸发溶液至有大量晶体析出时停止,再趁热过滤,并对过滤所得NaCl晶体进行洗涤和干燥。上述方法中,趁热过滤的目的是
(3)取23.4 g NaCl和40.4 g KNO3,加70 g水,加热溶解。在100 ℃时蒸发掉50 g水,维持该温度过滤,得到的晶体质量为
更新时间:2019-05-21 10:14:35
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】I.选取下列实验方法分离物质,将最佳分离方法的序号填在横线上。
A 萃取分液法 B 升华法 C 分液法 D 蒸馏法 E 过滤法
(1)_________ 分离饱和食盐水与沙子的混合物。
(2)_________ 分离水和汽油的混合物。
(3)_________ 分离四氯化碳(沸点为76.75 ℃)和甲苯(沸点为110.6 ℃)的混合物。
(4)_________ 分离碘水中的碘。
(5)_________ 分离氯化钠固体和碘固体的混合物。
II.图是甲、乙两种固体物质的溶解度曲线。

(1)t2℃时,将等质量的甲、乙两种物质加水溶解配制成饱和溶液,所得溶液质量的大小关系为:甲____________ 乙(填“>”、“<” 或 “=”)。
(2)除去甲物质中少量乙物质可采取____________ 结晶的方法(填“蒸发”或“降温”)。
III.如图装置,按要求填空

(1)排空气法收集气体,若收集CO2气体,进气口为__________ (填“a”或“b”)
(2)若瓶中装满水,可用于收集下列气体中的__________ (选填编号)
①NO ②NO2 ③NH3 ④HCl
(3)如果广口瓶中盛放浓硫酸,可以用作气体干燥装置,则该装置不可以干燥的气体有___________ (选填编号)
①HCl ②H2 ③NH3 ④CO ⑤HI
A 萃取分液法 B 升华法 C 分液法 D 蒸馏法 E 过滤法
(1)
(2)
(3)
(4)
(5)
II.图是甲、乙两种固体物质的溶解度曲线。

(1)t2℃时,将等质量的甲、乙两种物质加水溶解配制成饱和溶液,所得溶液质量的大小关系为:甲
(2)除去甲物质中少量乙物质可采取
III.如图装置,按要求填空

(1)排空气法收集气体,若收集CO2气体,进气口为
(2)若瓶中装满水,可用于收集下列气体中的
①NO ②NO2 ③NH3 ④HCl
(3)如果广口瓶中盛放浓硫酸,可以用作气体干燥装置,则该装置不可以干燥的气体有
①HCl ②H2 ③NH3 ④CO ⑤HI
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】结合水和溶液的相关知识,回答下列问题:
(1)对于沉淀、过滤、吸附、蒸馏等净化水的操作,相对净化程度较高的是____ 。
(2)水是化学实验中常用的试剂,下列各组物质能用水鉴别的是____ 。(填字母)
A.氢氧化钠和硝酸铵
B.食盐和蔗糖
C.高锰酸钾和碘
(3)欲配制100g溶质质量分数为10%的氯化钠溶液,完成此实验的正确操作顺序是____ 。
①溶解 ②把配好的溶液装入细口瓶 ③称量 ④计算 ⑤量取
(4)如图是a、b、c三种固体物质的溶解度曲线,回答下列问题:

①P点的含义是____ 。
②在t2℃时,向30克a物质中加入50克水,充分溶解后所得溶液的质量是____ 克。
③将t1℃时a、b、c三种物质的饱和溶液升温至t2℃,所得溶液中溶质的质量分数大小关系是____ 。
④a物质中含有少量c物质,可用____ 方法提纯a物质。(填“降温结晶”或“蒸发结晶”)
(1)对于沉淀、过滤、吸附、蒸馏等净化水的操作,相对净化程度较高的是
(2)水是化学实验中常用的试剂,下列各组物质能用水鉴别的是
A.氢氧化钠和硝酸铵
B.食盐和蔗糖
C.高锰酸钾和碘
(3)欲配制100g溶质质量分数为10%的氯化钠溶液,完成此实验的正确操作顺序是
①溶解 ②把配好的溶液装入细口瓶 ③称量 ④计算 ⑤量取
(4)如图是a、b、c三种固体物质的溶解度曲线,回答下列问题:

①P点的含义是
②在t2℃时,向30克a物质中加入50克水,充分溶解后所得溶液的质量是
③将t1℃时a、b、c三种物质的饱和溶液升温至t2℃,所得溶液中溶质的质量分数大小关系是
④a物质中含有少量c物质,可用
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】实验室有一瓶由氯化钾和硝酸钾组成的化肥,但标注的质量分数已模糊不清,小明想通过实验重新标注,以下是他进行的实验步骤:
①取10克样品于烧杯中,加入蒸馏水充分溶解,配制成60克溶液;
②在配制的溶液中,加入一定量的硝酸银溶液,恰好完全反应;
③将上述混合液过滤,沉淀经洗涤、干燥后,称得质量为14.35克。
请根据上述实验回答: (相关反应的化学方程式为:KCl+AgNO3=AgCl↓+KNO3)
(1)在过滤操作中使用的玻璃仪器有:烧杯、________ 和玻璃棒。
(2)样品中氯化钾的质量分数为__________ ?(要求列式计算)
(3)完全反应后,混合液中的硝酸钾质量是_______________ 克?
(4)为了回收硝酸钾,小明对滤液进行蒸发、结晶、称量,发现所得的晶体质量小于计算得出的理论值。造成这种结果的原因可能是_______ 。(选填编号)
A、晶体没有干燥
B、蒸发时液体飞溅
C、硝酸钾残留在玻璃棒上
①取10克样品于烧杯中,加入蒸馏水充分溶解,配制成60克溶液;
②在配制的溶液中,加入一定量的硝酸银溶液,恰好完全反应;
③将上述混合液过滤,沉淀经洗涤、干燥后,称得质量为14.35克。
请根据上述实验回答: (相关反应的化学方程式为:KCl+AgNO3=AgCl↓+KNO3)
(1)在过滤操作中使用的玻璃仪器有:烧杯、
(2)样品中氯化钾的质量分数为
(3)完全反应后,混合液中的硝酸钾质量是
(4)为了回收硝酸钾,小明对滤液进行蒸发、结晶、称量,发现所得的晶体质量小于计算得出的理论值。造成这种结果的原因可能是
A、晶体没有干燥
B、蒸发时液体飞溅
C、硝酸钾残留在玻璃棒上
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】去除粗盐中的Ca2+、Mg2+和 等杂质离子,过程如下:
等杂质离子,过程如下:

(1)上述精制过程中,加入的试剂①、②、③依次为过量的___________ 溶液、过量的___________ 溶液和过量的NaOH溶液。试剂①、②能否颠倒?___________ 。
(2)检验 沉淀完全的方法:取适量滤液,
沉淀完全的方法:取适量滤液,___________ 。
(3)向滤液中加入盐酸至溶液呈微酸性。写出加入盐酸后溶液中发生反应的离子方程式:___________ 和___________ 。
(4)加入盐酸至溶液呈微酸性后,经___________ (填操作名称)可得氯化钠固体,需要用到的仪器有___________ (填字母)。
a.蒸发皿 b.漏斗 c.玻璃棒 d.酒精灯
 等杂质离子,过程如下:
等杂质离子,过程如下:
(1)上述精制过程中,加入的试剂①、②、③依次为过量的
(2)检验
 沉淀完全的方法:取适量滤液,
沉淀完全的方法:取适量滤液,(3)向滤液中加入盐酸至溶液呈微酸性。写出加入盐酸后溶液中发生反应的离子方程式:
(4)加入盐酸至溶液呈微酸性后,经
a.蒸发皿 b.漏斗 c.玻璃棒 d.酒精灯
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】粗盐中常含有少量的泥沙及氯化钙、氯化镁、硫酸盐等一些可溶性的杂质。粗盐的提纯实验操作步骤如图所示:

(1)请写出图中各步实验操作的名称②_____ ,③______ 。
(2)实验操作②的主要目的是______ 。
(3)实验操作①②③中都使用的仪器是_____ ,它在③中其作用是_____ 。
(4)通过上述实验操作,得到的精盐中可能含有的杂质是____ 。

(1)请写出图中各步实验操作的名称②
(2)实验操作②的主要目的是
(3)实验操作①②③中都使用的仪器是
(4)通过上述实验操作,得到的精盐中可能含有的杂质是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.阅读、分析下列两个材料:
材料一
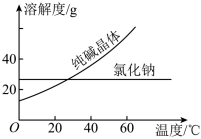
材料二
回答下列问题(填字母):
A.蒸馏法 B.萃取法C.“溶解、结晶、过滤”的方法 D.分液法
(1)将纯碱从氯化钠和纯碱的混合物中分离出来,最好选用________ 。
(2)将乙二醇和丙三醇相互分离的最佳方法是________ 。
Ⅱ.阅读下列材料,按要求回答问题。
酒精、苯、CCl4、煤油都是有机溶剂,有机溶剂之间大都能互溶;碘(I2)难溶于水,易溶于有机溶剂,其溶液呈紫色;溴(液溴)的性质与碘相似,其溶液呈橙色。
(1)下列能用分液漏斗进行分离的是________ (填字母)。
A.液溴和CCl4B.酒精和煤油
C.CaCl2和Na2SO4D.苯和蒸馏水
(2)在酒精、苯、CCl4、NaCl、蒸馏水五种试剂中:
①能把碘单质从碘水中萃取出来的是________ ,进行分液之后________ (填“能”或“不能”)得到纯净的碘单质。
②能把溴从溴水中萃取出来,并在分液时溴从分液漏斗下端流出的是________ ,若观察发现提取Br2以后的水还有颜色,解决该问题的方法是_________________________ 。
③CCl4能把碘酒中的碘萃取出来吗?________ ,为什么? ________________ 。
材料一

材料二
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 溶解性 |
| 乙二醇( C2H6O2) | -11.5 | 198 | 111 | 易溶于水和乙醇 |
| 丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互 |
回答下列问题(填字母):
A.蒸馏法 B.萃取法C.“溶解、结晶、过滤”的方法 D.分液法
(1)将纯碱从氯化钠和纯碱的混合物中分离出来,最好选用
(2)将乙二醇和丙三醇相互分离的最佳方法是
Ⅱ.阅读下列材料,按要求回答问题。
酒精、苯、CCl4、煤油都是有机溶剂,有机溶剂之间大都能互溶;碘(I2)难溶于水,易溶于有机溶剂,其溶液呈紫色;溴(液溴)的性质与碘相似,其溶液呈橙色。
(1)下列能用分液漏斗进行分离的是
A.液溴和CCl4B.酒精和煤油
C.CaCl2和Na2SO4D.苯和蒸馏水
(2)在酒精、苯、CCl4、NaCl、蒸馏水五种试剂中:
①能把碘单质从碘水中萃取出来的是
②能把溴从溴水中萃取出来,并在分液时溴从分液漏斗下端流出的是
③CCl4能把碘酒中的碘萃取出来吗?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】选择下列实验方法分离物质,将分离方法的字母代号填在表格内.
A.萃取分液 B.分液 C.蒸馏 D.过滤
A.萃取分液 B.分液 C.蒸馏 D.过滤
①分离饱和食盐水与沙子的混合物 | ②分离水和汽油的混合物 | ③分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物,CCl4和甲苯互溶 | ④提取出碘水中的碘单质 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】选择装置,完成实验。

(1)用饱和食盐水除去氯气中的氯化氢,应选用______ (填序号,下同)。
(2)除去食盐水中的泥沙,应选用______ 。
(3)用自来水制取蒸馏水,应选用______ 。
(4)用四氯化碳提取碘水中的碘,应选用______ 。

(1)用饱和食盐水除去氯气中的氯化氢,应选用
(2)除去食盐水中的泥沙,应选用
(3)用自来水制取蒸馏水,应选用
(4)用四氯化碳提取碘水中的碘,应选用
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】通过海水晾晒可得粗盐,粗盐中除NaCl外,还含有 、
、 、
、 以及泥沙等杂质,需要提纯后才能综合利用。某同学利用给定试剂NaOH溶液、
以及泥沙等杂质,需要提纯后才能综合利用。某同学利用给定试剂NaOH溶液、 溶液、
溶液、 溶液和盐酸,设计了如图粗盐精制的实验流程。(提示:根据实验目的,请思考试剂的用量)
溶液和盐酸,设计了如图粗盐精制的实验流程。(提示:根据实验目的,请思考试剂的用量)
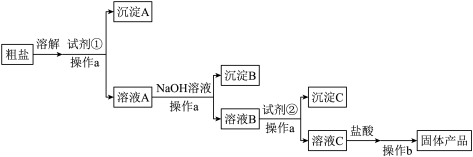
请回答:
(1)操作a名称是_______ 。
(2)试剂①是_______ 溶液(填化学式)。
(3)加入NaOH后,得到的主要沉淀B是_______ 。
(4)加入试剂②后,发生反应的离子方程式有_______ 。
(5)如果加入试剂②后直接加盐酸,产生的后果是_______ (用离子方程式表示)。
 、
、 、
、 以及泥沙等杂质,需要提纯后才能综合利用。某同学利用给定试剂NaOH溶液、
以及泥沙等杂质,需要提纯后才能综合利用。某同学利用给定试剂NaOH溶液、 溶液、
溶液、 溶液和盐酸,设计了如图粗盐精制的实验流程。(提示:根据实验目的,请思考试剂的用量)
溶液和盐酸,设计了如图粗盐精制的实验流程。(提示:根据实验目的,请思考试剂的用量)
请回答:
(1)操作a名称是
(2)试剂①是
(3)加入NaOH后,得到的主要沉淀B是
(4)加入试剂②后,发生反应的离子方程式有
(5)如果加入试剂②后直接加盐酸,产生的后果是
您最近一年使用:0次



