Ⅰ.阅读、分析下列两个材料:
材料一
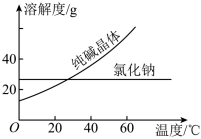
材料二
回答下列问题(填字母):
A.蒸馏法 B.萃取法C.“溶解、结晶、过滤”的方法 D.分液法
(1)将纯碱从氯化钠和纯碱的混合物中分离出来,最好选用________ 。
(2)将乙二醇和丙三醇相互分离的最佳方法是________ 。
Ⅱ.阅读下列材料,按要求回答问题。
酒精、苯、CCl4、煤油都是有机溶剂,有机溶剂之间大都能互溶;碘(I2)难溶于水,易溶于有机溶剂,其溶液呈紫色;溴(液溴)的性质与碘相似,其溶液呈橙色。
(1)下列能用分液漏斗进行分离的是________ (填字母)。
A.液溴和CCl4B.酒精和煤油
C.CaCl2和Na2SO4D.苯和蒸馏水
(2)在酒精、苯、CCl4、NaCl、蒸馏水五种试剂中:
①能把碘单质从碘水中萃取出来的是________ ,进行分液之后________ (填“能”或“不能”)得到纯净的碘单质。
②能把溴从溴水中萃取出来,并在分液时溴从分液漏斗下端流出的是________ ,若观察发现提取Br2以后的水还有颜色,解决该问题的方法是_________________________ 。
③CCl4能把碘酒中的碘萃取出来吗?________ ,为什么? ________________ 。
材料一

材料二
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 溶解性 |
| 乙二醇( C2H6O2) | -11.5 | 198 | 111 | 易溶于水和乙醇 |
| 丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互 |
回答下列问题(填字母):
A.蒸馏法 B.萃取法C.“溶解、结晶、过滤”的方法 D.分液法
(1)将纯碱从氯化钠和纯碱的混合物中分离出来,最好选用
(2)将乙二醇和丙三醇相互分离的最佳方法是
Ⅱ.阅读下列材料,按要求回答问题。
酒精、苯、CCl4、煤油都是有机溶剂,有机溶剂之间大都能互溶;碘(I2)难溶于水,易溶于有机溶剂,其溶液呈紫色;溴(液溴)的性质与碘相似,其溶液呈橙色。
(1)下列能用分液漏斗进行分离的是
A.液溴和CCl4B.酒精和煤油
C.CaCl2和Na2SO4D.苯和蒸馏水
(2)在酒精、苯、CCl4、NaCl、蒸馏水五种试剂中:
①能把碘单质从碘水中萃取出来的是
②能把溴从溴水中萃取出来,并在分液时溴从分液漏斗下端流出的是
③CCl4能把碘酒中的碘萃取出来吗?
更新时间:2020-02-23 11:54:11
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室制备乙酸乙酯的实验装置示意图和有关实验步骤如下:在A中加入4.6 g的乙醇,9.0 g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50min,反应液冷至室温后倒入分液漏斗中,分别用少量水,饱和碳酸钠溶液和水洗涤,分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集馏分,得乙酸乙酯5.28 g。
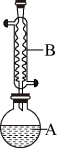
回答下列问题:
(1)仪器B的名称是:_____________
(2)A 中浓硫酸的作用是__________ 和____________ 。
(3)写出实验室用乙醇和乙酸制取乙酸乙酯的化学反应方程式:______________________________ 。
(4)在洗涤、分液操作中,应充分振荡,然后静置,待分层后________ (填标号)。
a.直接将乙酸乙酯从分液漏斗上口倒出
b.直接将乙酸乙酯从分液漏斗下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸乙酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸乙酯从上口放出
(5)实验中加入少量无水MgSO4的目的是:_________________ 。
(6)在蒸馏操作中,仪器选择及安装都正确的是:___________ (填标号)。

(7)本实验的产率是:__________ (填标号)。(产率指的是某种生成物的实际产量与理论产量的比值。已知乙醇、乙酸、乙酸乙酯的相对分子质量分别为:46、60、88。)
a.30% b.40% c.50% d.60%
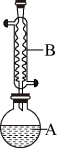
回答下列问题:
(1)仪器B的名称是:
(2)A 中浓硫酸的作用是
(3)写出实验室用乙醇和乙酸制取乙酸乙酯的化学反应方程式:
(4)在洗涤、分液操作中,应充分振荡,然后静置,待分层后
a.直接将乙酸乙酯从分液漏斗上口倒出
b.直接将乙酸乙酯从分液漏斗下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸乙酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸乙酯从上口放出
(5)实验中加入少量无水MgSO4的目的是:
(6)在蒸馏操作中,仪器选择及安装都正确的是:

(7)本实验的产率是:
a.30% b.40% c.50% d.60%
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】碳酸锂是制备各种锂化合物的关键原料。一种以磷酸锂渣(主要成分Li3PO4)为原料制备碳酸锂的工艺流程示意图如下。
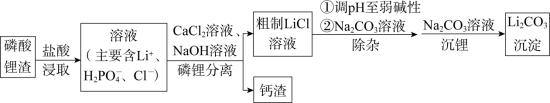
已知:部分物质的溶解性表(20℃)
(1)写出浸取时Li3PO4与盐酸反应的化学方程式:_______ 。
(2)加入盐酸的量不宜过多的原因是_______ 。
(3)钙渣的主要成分是_______ 。
(4)磷锂分离时,需要不断加入适量NaOH溶液以维持溶液的pH基本不变。结合离子方程式解释其原因是_______ 。
(5)沉锂时,反应的离子方程式是_______ 。

已知:部分物质的溶解性表(20℃)
| 阳离子 | 阴离子 | ||
 |  | 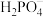 | |
| Li+ | 难溶 | 可溶 | 易溶 |
| Ca2+ | 难溶 | 难溶 | 可溶 |
(2)加入盐酸的量不宜过多的原因是
(3)钙渣的主要成分是
(4)磷锂分离时,需要不断加入适量NaOH溶液以维持溶液的pH基本不变。结合离子方程式解释其原因是
(5)沉锂时,反应的离子方程式是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】二十一世纪世界资源争夺的重点是海洋。海底有石油、可燃冰、石油气、矿砂、锰结核的资源,海水中除有渔业资源外,还有食盐、溴、碘等许多化学资源,所有资源中最丰富的是水资源。
(1)海水中质量分数最高的元素是氧,该元素的原子核外电子占据的轨道共有______ 个,有______ 个未成对电子。
(2)水的沸点为100℃,氟化氢的沸点为19.5℃,水与氟化氢比较,稳定性较强的是________ 。
(3)提取碘是将海带灼烧成灰,溶于水过滤,滤液中通入氯气,反应的离子方程式为_______________________________ ,再用四氯化碳将生成的单质碘________ (填写实验操作名称)出来,最后用_________ (填写实验操作名称)使碘和四氯化碳分离。
(4)海洋元素中的氯、溴、碘统称为海水中的卤素资源,它们的最外层电子排布都可表示为______________ 。
(1)海水中质量分数最高的元素是氧,该元素的原子核外电子占据的轨道共有
(2)水的沸点为100℃,氟化氢的沸点为19.5℃,水与氟化氢比较,稳定性较强的是
(3)提取碘是将海带灼烧成灰,溶于水过滤,滤液中通入氯气,反应的离子方程式为
(4)海洋元素中的氯、溴、碘统称为海水中的卤素资源,它们的最外层电子排布都可表示为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】选择下列实验方法分离物质,将分离方法的字母代号填在横线上。
A.萃取分液 B.分液 C.蒸馏 D.过滤 E.蒸发
(1)分离水和乙酸乙酯的混合物,可采用______________________ 方法。
(2)提取碘水中的碘并获取碘单质,可采用____________________ 方法。
(3)除去食盐溶液中的水,可采用_________________ 方法。
(4)淡化海水,可采用_________________ 方法。
(5)丙酮是一种常用的有机溶剂,可与水以任意体积互溶,密度小于水,沸点约为55℃,分离水和丙酮的混合物时可采用_________________ 方法。
(6)实验室中的石灰水久置,液面上常悬浮有CaCO3结膜,可采用_________________ 方法除去。
A.萃取分液 B.分液 C.蒸馏 D.过滤 E.蒸发
(1)分离水和乙酸乙酯的混合物,可采用
(2)提取碘水中的碘并获取碘单质,可采用
(3)除去食盐溶液中的水,可采用
(4)淡化海水,可采用
(5)丙酮是一种常用的有机溶剂,可与水以任意体积互溶,密度小于水,沸点约为55℃,分离水和丙酮的混合物时可采用
(6)实验室中的石灰水久置,液面上常悬浮有CaCO3结膜,可采用
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】粗盐中含氯化钙、硫酸镁及少量泥沙,粗盐提纯的流程:
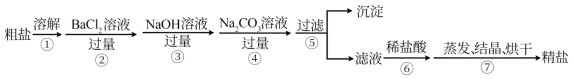
请回答下列问题:
(1)某同学实验过程中将“步骤②”和“步骤③”互换,则对该流程_______ (填“有”或“无”)影响。
(2)“步骤②”中发生反应的化学方程式为_______ ;检验“步骤②”中杂质离子除干净的操作为_______ 。
(3)“步骤③”中发生反应的化学方程式为_______ ;“步骤④”中加入的碳酸钠溶液的作用是_______ 。
(4)不能将“步骤⑥”置于“步骤⑤”前进行的原因是_______ 。

请回答下列问题:
(1)某同学实验过程中将“步骤②”和“步骤③”互换,则对该流程
(2)“步骤②”中发生反应的化学方程式为
(3)“步骤③”中发生反应的化学方程式为
(4)不能将“步骤⑥”置于“步骤⑤”前进行的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某炼锌厂烟道灰含锌废料的主要成分是ZnO,还含有少量CuO、Fe2O3和Fe3O4,用其制备ZnSO4·7H2O的流程图如图,请回答下列问题:
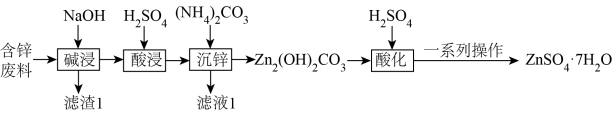
已知: 为两性氧化物,能与
为两性氧化物,能与 溶液反应生成
溶液反应生成 。
。
(1)“碱浸”时,加快碱浸速率的措施有_____ (写出两种即可);“滤渣1”的主要成分为CuO、_____ (填化学式)。
(2)ZnO在“碱浸”时发生反应的离子方程式为_____ ;“酸浸”时,如果加入的硫酸不足,可能生成某种不溶物,该不溶物为_____ (填化学式)。
(3)“沉锌”时,所得的“滤液1”中的溶质有 、
、_____ (填化学式);“沉锌”后洗涤获得的 与稀硫酸反应的化学方程式为
与稀硫酸反应的化学方程式为_____ 。
(4)“一系列操作”包括_____ 、_____ 、过滤、洗涤、干燥。
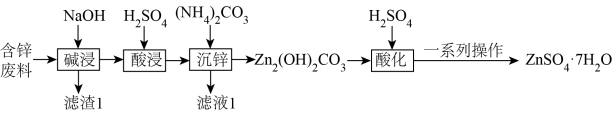
已知:
 为两性氧化物,能与
为两性氧化物,能与 溶液反应生成
溶液反应生成 。
。(1)“碱浸”时,加快碱浸速率的措施有
(2)ZnO在“碱浸”时发生反应的离子方程式为
(3)“沉锌”时,所得的“滤液1”中的溶质有
 、
、 与稀硫酸反应的化学方程式为
与稀硫酸反应的化学方程式为(4)“一系列操作”包括
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】 Ⅰ.
Ⅰ.
(1)下列实验设计或操作合理的是________ 。
A.在催化剂存在的条件下,苯和浓溴水发生反应可生成无色比水重的液体溴苯
B.只用水就能鉴别苯、硝基苯、乙醇
C.实验室制取乙烯时需要控制温度在170℃左右,因此使用水浴加热
D.将10滴溴乙烷加入1mL 10%的烧碱溶液中加热片刻后,再滴加2滴2%的硝酸银溶液,以检验水解生成的溴离子
E.工业酒精制取无水酒精时先加生石灰然后蒸馏,蒸馏必须将温度计的水银球插入反应液中
F.苯酚中滴加少量的稀溴水,可用来定量检验苯酚
G.将铜片放入盛有无水乙醇的试管中加热,完成乙醇氧化为乙醛的实验
H.为了减缓电石和水的反应速率,可用饱和食盐水来代替水进行实验
Ⅱ.某化学小组以苯甲酸和异丙醇为原料,制取苯甲酸异丙酯(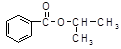 ),已知有关物质的沸点如下表:
),已知有关物质的沸点如下表:
合成苯甲酸异丙酯粗产品在如图圆底烧瓶中加入12.2 g苯甲酸和30 mL异丙醇(密度约为0.79 g·cm-3),再小心加入3mL浓硫酸,混匀后,投入几块碎瓷片,小心加热30分钟,使反应完全,得苯甲酸异丙酯粗产品。
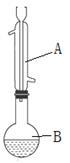
(2)仪器A的名称是______ ;加入碎瓷片的目的是_________________ ;
(3)异丙醇的系统命名法的名称为_______________ ;浓硫酸的作用是_____________ ;
(4)若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式________________ 。
粗产品的精制
(5)苯甲酸异丙酯粗产品中往往含有少量异丙醇、苯甲酸和水等,现拟用下列流程图进行精制,操作①中用到的一种重要仪器是______________ ;操作②的名称是__________
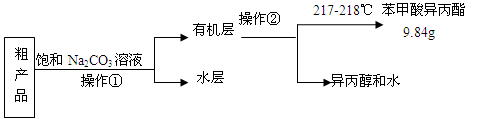
(6)通过计算,苯甲酸甲酯的产率为__________________
(7)该实验中不能用于提高苯甲酸甲酯的产率的措施是__________
A.苯甲酸的质量由12.2g增加至24.4g
B.30ml的异丙醇增加至35mL
 Ⅰ.
Ⅰ.(1)下列实验设计或操作合理的是
A.在催化剂存在的条件下,苯和浓溴水发生反应可生成无色比水重的液体溴苯
B.只用水就能鉴别苯、硝基苯、乙醇
C.实验室制取乙烯时需要控制温度在170℃左右,因此使用水浴加热
D.将10滴溴乙烷加入1mL 10%的烧碱溶液中加热片刻后,再滴加2滴2%的硝酸银溶液,以检验水解生成的溴离子
E.工业酒精制取无水酒精时先加生石灰然后蒸馏,蒸馏必须将温度计的水银球插入反应液中
F.苯酚中滴加少量的稀溴水,可用来定量检验苯酚
G.将铜片放入盛有无水乙醇的试管中加热,完成乙醇氧化为乙醛的实验
H.为了减缓电石和水的反应速率,可用饱和食盐水来代替水进行实验
Ⅱ.某化学小组以苯甲酸和异丙醇为原料,制取苯甲酸异丙酯(
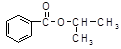 ),已知有关物质的沸点如下表:
),已知有关物质的沸点如下表:| 物质 | 异丙醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 82.4 | 249 | 218 |

(2)仪器A的名称是
(3)异丙醇的系统命名法的名称为
(4)若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学方程式
粗产品的精制
(5)苯甲酸异丙酯粗产品中往往含有少量异丙醇、苯甲酸和水等,现拟用下列流程图进行精制,操作①中用到的一种重要仪器是

(6)通过计算,苯甲酸甲酯的产率为
(7)该实验中不能用于提高苯甲酸甲酯的产率的措施是
A.苯甲酸的质量由12.2g增加至24.4g
B.30ml的异丙醇增加至35mL
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】教材中有两个关于混合物分离的实验,请回答下列有关问题
实验一:通过蒸馏的方法除去自来水中含有的氯离子等杂质制取纯净水,如图所示
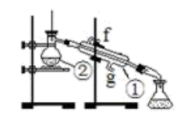
(1)写出下列仪器的名称:①___________ 、②___________
(2)若利用以上装置分离酒精和四氯化碳两种溶液的混合物,还缺少的仪器是___________ ,将仪器补充完整后进行的实验操作的名称是___________ ;①的进水口是___________ (填“f”或“g”)
(3)仪器①中常加入碎瓷片,这样做的目的是___________
实验二:用 从碘水中萃取
从碘水中萃取 并分液漏斗分离两种溶液。
并分液漏斗分离两种溶液。
其实验操作中有如下两步:①将漏斗上口玻璃塞打开或使塞上的凹槽或小孔准漏斗的小孔。
(4)这样做的目的是___________
②静置分层后,旋开活塞,用烧杯接收下层液体
(5)上层液体从___________ 倒出(填“上口”或“下口”)
实验一:通过蒸馏的方法除去自来水中含有的氯离子等杂质制取纯净水,如图所示

(1)写出下列仪器的名称:①
(2)若利用以上装置分离酒精和四氯化碳两种溶液的混合物,还缺少的仪器是
(3)仪器①中常加入碎瓷片,这样做的目的是
实验二:用
 从碘水中萃取
从碘水中萃取 并分液漏斗分离两种溶液。
并分液漏斗分离两种溶液。其实验操作中有如下两步:①将漏斗上口玻璃塞打开或使塞上的凹槽或小孔准漏斗的小孔。
(4)这样做的目的是
②静置分层后,旋开活塞,用烧杯接收下层液体
(5)上层液体从
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】下图是中学化学中常用于混合物的分离和提纯装置,请根据装置回答问题:
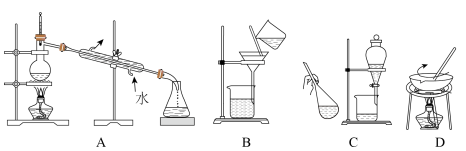
(1)以上四种化学实验操作的名称依次是:_______ 、_______ 、_______ 、_______ 。
(2)分离CCl4(沸点:76.75℃)和苯(沸点:110.6℃)的混合物(互溶)应选用_______ ;(填装置字母)
(3)在使用C进行化学实验操作前,应先_______ ,在分液时为使液体顺利滴下,应进行的操作为_______ 。
(4)青蒿素是从复合花序植物黄花蒿茎叶中提取的有过氧基团的倍半萜内酯的一种无色针状晶体,是一种高效的抗疟疾药,为无色针状晶体,易溶于丙酮、氯仿和苯中,在乙醇、乙醚中可溶解,在水中几乎不溶,熔点为156-157℃,热稳定性差。已知:乙醚沸点为35℃。提取青蒿素的主要工艺为:

若要在实验室模拟上述工艺,操作Ⅰ选择的装置是_______ ,操作Ⅱ的名称是_______ ,操作Ⅲ的主要过程可能是_______ (填字母)。
A.加95%的乙醇,浓缩、结晶、过滤
B.加水溶解,蒸发浓缩、冷却结晶、过滤
C.加入乙醚进行萃取分液

(1)以上四种化学实验操作的名称依次是:
(2)分离CCl4(沸点:76.75℃)和苯(沸点:110.6℃)的混合物(互溶)应选用
(3)在使用C进行化学实验操作前,应先
(4)青蒿素是从复合花序植物黄花蒿茎叶中提取的有过氧基团的倍半萜内酯的一种无色针状晶体,是一种高效的抗疟疾药,为无色针状晶体,易溶于丙酮、氯仿和苯中,在乙醇、乙醚中可溶解,在水中几乎不溶,熔点为156-157℃,热稳定性差。已知:乙醚沸点为35℃。提取青蒿素的主要工艺为:

若要在实验室模拟上述工艺,操作Ⅰ选择的装置是
A.加95%的乙醇,浓缩、结晶、过滤
B.加水溶解,蒸发浓缩、冷却结晶、过滤
C.加入乙醚进行萃取分液
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】观察下列实验装置图,试回答下列问题:
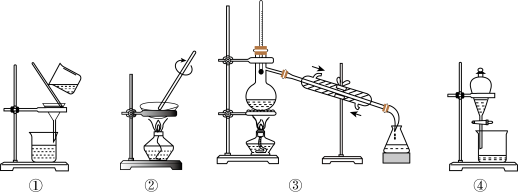
(1)写出图中③实验操作的名称是______
(2)下列实验需要在哪套装置中进行(填序号):
a.从海水中提取蒸馏水:______ ; b.分离氯化钠和水:______ ;
c.分离碳酸钙和水:______ ; d.分离植物油和水:______ ;
(3)装置②中玻璃棒搅拌的目的是_________________________ 。

(1)写出图中③实验操作的名称是
(2)下列实验需要在哪套装置中进行(填序号):
a.从海水中提取蒸馏水:
c.分离碳酸钙和水:
(3)装置②中玻璃棒搅拌的目的是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】海水中含NaBr与MgCl2等化学资源,提取溴的流程如图所示,部分产物省略。液溴的密度为3.1g/cm3,饱和溴水中Br2的浓度为0.36mol/L。

回答以下问题:
(1)操作x的目的是为了分离出海水中的_______ 元素,以获取资源。
(2)“溶液1”中加盐酸的目的是_______ 。
(3)①与②反应相同,其离子方程式为_______ 。“溶液2”通Cl2反应后使用了空气吹出法,该方法利用了溴单质_______ 的性质。
(4)“吸收”反应的离子方程式为_______ 。
(5)“操作y”在实验室中叫做_______ ;1m3“溶液4”中溶解Br2的物质的量为_______ 。

回答以下问题:
(1)操作x的目的是为了分离出海水中的
(2)“溶液1”中加盐酸的目的是
(3)①与②反应相同,其离子方程式为
(4)“吸收”反应的离子方程式为
(5)“操作y”在实验室中叫做
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】实验室制备苯乙酮的化学方程式如图1为:
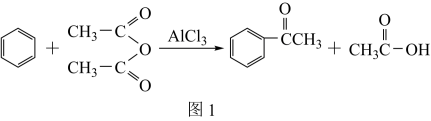
制备过程中还有CH3COOH+AlCl3→CH3COOAlCl2+HCl↑等副反应,主要实验装置和步骤如图2所示:
(I)合成:在三颈瓶中加入20g无水AlCl3和30mL无水苯。为避免反应液升温过快,边搅拌边慢慢滴加6mL乙酸酐和10mL无水苯的混合液,控制滴加速率,使反应液缓缓回流。滴加完毕后加热回流1小时。
(II)分离与提纯:
①边搅拌边慢慢滴加一定量浓盐酸与冰水混合液,分离得到有机层
②水层用苯萃取,分液
③将①②所得有机层合并,洗涤、干燥、蒸去苯,得到苯乙酮粗产品
④蒸馏粗产品得到苯乙酮。回答下列问题:
(1)仪器a的名称:_______ ;装置b的作用:_______ 。
(2)若将乙酸酐和苯的混合液一次性倒入三颈瓶,可能导致_______ 。
A.反应太剧烈 B.液体太多搅不动
C.反应变缓慢 D.副产物增多
(3)分离和提纯操作②的目的是____ 。该操作中是否可改用乙醇萃取?_____ (填“是”或“否”)。
(4)分液漏斗使用前须____ 并洗净备用。萃取时,先后加入待萃取液和萃取剂,经振摇并____ 后,将分液漏斗置于铁架台的铁圈上静置片刻,分层。分离上下层液体时,应先___ ,然后打开活塞放出下层液体,上层液体从上口倒出。
(5)粗产品蒸馏提纯时,如图3装置中温度计位置正确的是___ ,可能会导致收集到的产品中混有低沸点杂质的装置是___ 。

制备过程中还有CH3COOH+AlCl3→CH3COOAlCl2+HCl↑等副反应,主要实验装置和步骤如图2所示:

图2
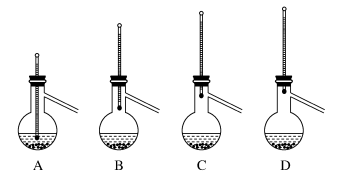
图3
(I)合成:在三颈瓶中加入20g无水AlCl3和30mL无水苯。为避免反应液升温过快,边搅拌边慢慢滴加6mL乙酸酐和10mL无水苯的混合液,控制滴加速率,使反应液缓缓回流。滴加完毕后加热回流1小时。
(II)分离与提纯:
①边搅拌边慢慢滴加一定量浓盐酸与冰水混合液,分离得到有机层
②水层用苯萃取,分液
③将①②所得有机层合并,洗涤、干燥、蒸去苯,得到苯乙酮粗产品
④蒸馏粗产品得到苯乙酮。回答下列问题:
(1)仪器a的名称:
(2)若将乙酸酐和苯的混合液一次性倒入三颈瓶,可能导致
A.反应太剧烈 B.液体太多搅不动
C.反应变缓慢 D.副产物增多
(3)分离和提纯操作②的目的是
(4)分液漏斗使用前须
(5)粗产品蒸馏提纯时,如图3装置中温度计位置正确的是
您最近一年使用:0次



